武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
不止于抗原提呈:CD74如何成为肿瘤与自身免疫病的关键调控者?
213 人阅读发布时间:2026-04-07 10:30
CD74是MHC II类分子的经典伴侣蛋白,在抗原提呈中发挥核心作用。近年研究发现,CD74也是巨噬细胞迁移抑制因子(MIF)的重要受体,参与炎症、免疫调控、细胞增殖及肿瘤进展等多种非经典过程。本文系统综述了CD74的分子特征、经典与非经典功能、关键信号通路及其在恶性肿瘤、自身免疫性疾病和炎症性疾病中的作用。研究表明,CD74不仅参与肿瘤发生、免疫抑制和耐药形成,还与多种疾病的诊断和预后评估相关。靶向CD74的策略,特别是抗体偶联药物和MIF-CD74轴抑制剂,展现出良好的转化前景。尽管该领域仍面临机制复杂性、异构体功能差异及临床分层不足等挑战,但随着单细胞测序、多组学分析和精准治疗技术的发展,CD74有望成为炎症、自身免疫病和肿瘤治疗的重要靶点。
1. 引言
2. CD74 的分子特征与经典功能
3. CD74 的非经典功能与信号通路
4. CD74 在疾病中的作用
5. CD74 靶向药物研究进展
6. CD74 研究工具
1. 引言
CD74,又称不变链(Invariant Chain, Ii),是 MHC II 类分子的关键伴侣蛋白,在抗原提呈过程中具有基础性作用。它通过与 MHC II 类分子结合,阻止内源性肽段过早结合,并引导复合体进入抗原提呈相关胞内区室,最终促进外源性抗原肽装载和 CD4+ T 细胞应答启动。传统上,CD74 被认为是维持 MHC II 类分子成熟、运输和抗原提呈所必需的分子。
随着研究深入,CD74 的功能已不再局限于抗原提呈。研究表明,CD74 还是 MIF 的高亲和力受体,可介导细胞增殖、迁移、存活及炎症因子释放等反应,从而参与先天免疫、获得性免疫、炎症反应、自身免疫性疾病及肿瘤微环境调控 [2]。这种双重身份使 CD74 成为连接抗原提呈通路与炎症/增殖信号通路的重要枢纽,也使其成为基础研究和临床转化中的高关注靶点。
因此,系统梳理 CD74 的分子特征、作用机制、疾病关联及药物研发进展,有助于更全面地理解其生物学意义,并为后续精准干预策略提供理论基础。
2. CD74 的分子特征与经典功能
2.1 结构特征与表达模式
CD74 是一种 II 型跨膜糖蛋白,包含短胞质区、跨膜区和较大的胞外区 [1]。其胞外区包含 CLIP(Class II-associated invariant chain peptide)相关片段,在 MHC II 抗原提呈中具有关键作用,同时也是 MIF 的重要结合位点 [2]。CD74 存在多种异构体,例如 p35 异构体,不同异构体在细胞定位和功能上可能存在差异 [3]。
在正常生理状态下,CD74 主要表达于多种免疫细胞,包括 B 细胞区室和胸腺髓质细胞 [1, 4]。在人 CD4+ T 细胞中,静息状态下 CD74 主要位于胞内,而激活后其表达上调,并可在细胞表面检测到 [2]。这一特征提示,CD74 不仅参与经典抗原提呈,也可能与活化 T 细胞迁移和炎症应答有关 [2]。
除正常免疫细胞外,CD74 在多种肿瘤中也呈高表达。例如,在多发性骨髓瘤中,CD74 mRNA 可在几乎全部新诊断患者的 CD138+ 浆细胞中检测到 [5];在多种淋巴瘤中,CD74 也具有较高表达频率,包括霍奇金淋巴瘤、B 细胞淋巴瘤、结外 NK/T 细胞淋巴瘤和成熟 T 细胞淋巴瘤等 [4]。这种广泛表达使其成为潜在的治疗靶点 [5, 6]。
2.2 作为 MHC II 伴侣分子的经典功能
CD74 在 MHC II 类分子的生物合成和抗原提呈通路中具有核心伴侣作用。其主要功能包括稳定新合成的 MHC II 类分子、阻止内质网内内源性肽段过早占据肽结合槽、引导 MHC II-CD74 复合体进入内涵体/溶酶体区室,并在后续蛋白酶切割及 HLA-DM 或 H2-M 介导下促进 CLIP 解离和外源性抗原肽装载。
这一过程对于外源性抗原提呈至关重要,直接关系到辅助性 T 细胞能否识别抗原并启动适应性免疫应答。研究表明,人源化不变链表达可增强 MHC II 类分子在胸腺上皮细胞中的表达,提高脾脏成熟 B 细胞数量,并提升抗原提呈效率 [1]。此外,CD74 与 MHC II 类基因表达一样,均受 CIITA 严格调控;例如 IL-27 可通过 STAT1/IRF1/CIITA 轴诱导肠上皮细胞中 MHC II 和 CD74 的表达,进一步说明 CD74 是抗原提呈网络中的关键组成部分。
3. CD74 的非经典功能与信号通路
3.1 作为 MIF 受体的结构与结合特性
除经典伴侣作用外,CD74 还是 MIF 的高亲和力受体,在炎症、免疫调控和肿瘤进展中具有重要意义 [2]。MIF 及其超家族成员通过与 CD74 结合,触发多种细胞反应。在急性肺损伤中,CD74 表达于肺巨噬细胞表面,其可溶形式 sCD74 的升高还与肺损伤严重程度及预后相关 [7]。这些发现说明,MIF-CD74 轴不仅是炎症反应的重要调节通路,也可能作为疾病标志物和干预靶点。
3.2 MIF-CD74 轴及下游信号级联
MIF-CD74 轴激活后可启动多条经典信号网络,包括 ERK、PI3K/AKT、mTOR、JAK/STAT 和 NF-κB。研究显示,在肺腺癌中,肿瘤细胞与巨噬细胞间的 MIF-CD74 相互作用增强,且 MIF 表达与患者总生存期相关 [8]。在 RUNX1 相关家族性血小板疾病中,CD74 和 MIF 同时升高,形成炎症和促生存信号的正反馈循环 [9]。在 ADPKD 中,CD74 还可促进 MIF 表达,进一步加重囊肿生长和肾纤维化 [10]。
在功能层面,MIF-CD74 轴能够整合炎症、存活和组织重塑信号。EAE 模型研究表明,阻断 MIF-CD74 相互作用可抑制 ERK 活化,减轻炎症并促进髓鞘修复 [11]。在 FPD 中,MIF-CD74 信号上调 PI3K/mTOR 和 JAK 通路,推动异常造血和炎症放大 [9]。在肠纤维化中,该轴还可通过促进 STAT3 磷酸化和 IL-22 表达而激活成纤维细胞 [12]。这些结果表明,CD74 不仅是 MIF 的受体,也是多条炎症和增殖信号通路的整合节点。
3.3 MIF 非依赖性功能
CD74 的致病作用并不完全依赖 MIF。研究显示,在 ADPKD 中,CD74 可作为转录调节因子,直接结合胶原 I、纤连蛋白和 α-SMA 等纤维化标志物启动子,促进其表达 [10]。此外,CD74 还能调控 MIF 自身转录,形成进一步放大的正反馈环路 [10]。这提示 CD74 还可能通过胞内调控机制直接参与组织重塑和纤维化进程。
3.4 与其他信号通路的交叉调控
CD74 还广泛参与与其他信号通路的交叉调控。例如,在 ADPKD 中,MIF-CD74 轴可与 TGF-β/Smad3 通路联动,促进肾间质纤维化 [10];在活化 CD4+ T 细胞中,CD74 可与 CXCR4 形成异源复合物,参与 MIF 诱导的 T 细胞迁移 [2]。此外,CD74-NRG1 融合蛋白能够结合 ERBB3 并驱动 ERBB2:ERBB3 异二聚化,从而促进肿瘤发生 [13]。这些现象表明,CD74 不是孤立发挥作用,而是在复杂信号网络中与多条关键通路相互耦合,进而决定不同疾病背景下的生物学效应。
4. CD74 在疾病中的作用
4.1 恶性肿瘤中的作用
CD74 在恶性肿瘤中具有多重作用,包括促进肿瘤细胞生存、参与肿瘤微环境塑造、驱动融合基因相关肿瘤发生,以及介导治疗耐药。其在血液系统肿瘤中表达尤为广泛,霍奇金淋巴瘤、B 细胞淋巴瘤、结外 NK/T 细胞淋巴瘤、成熟 T 细胞淋巴瘤和浆细胞骨髓瘤中均可见较高表达 [4]。在多发性骨髓瘤中,CD74 几乎普遍表达,为靶向治疗提供了明确依据 [5, 15]。
在实体瘤中,CD74 同样具有重要意义。例如,在胰腺导管腺癌中,CD74 敲低可抑制肿瘤细胞增殖、迁移和侵袭,并减少 S100A8/S100A9 分泌,从而影响促炎性肿瘤微环境 [14]。在肺癌和胰腺癌中,CD74-NRG1 融合是重要致癌事件,能够激活 ERBB2:ERBB3 信号并驱动肿瘤进展 [13]。此外,在 ROS1 或 ALK 融合阳性肿瘤中,CD74 上调还与 TKI 耐药相关,提示其参与药物耐受细胞维持和肿瘤适应性演化。
在肿瘤微环境层面,MIF-CD74 轴被认为是重要的免疫抑制机制。在宫颈癌中,CD74 上调限制肿瘤相关巨噬细胞吞噬功能并促进 M2 极化 [16];在 LUAD 中,MIF-CD74 相关免疫抑制特征与较差生存显著相关 [8]。但另一方面,高 CD74 表达又与部分实体瘤中更"炎性"的免疫微环境及对 PD-1/CTLA-4 双抗治疗的较好反应相关 [17]。这提示 CD74 在肿瘤免疫中的作用具有明显的背景依赖性。
4.2 自身免疫性与炎症性疾病中的作用
CD74 在多种自身免疫和炎症性疾病中同样扮演重要角色。在 ALI/ARDS 中,sCD74 水平升高与肺通透性增加、炎症加重和不良预后相关 [7]。在多发性硬化症模型 EAE 中,阻断 MIF-CD74 轴可减轻炎症、促进髓鞘修复并改善神经功能 [11, 18, 19]。在实验性自身免疫性葡萄膜炎中,Cd74high Ccl5high 小胶质细胞被鉴定为促炎亚群,阻断 Cd74 或 Ccl5 可减轻疾病表型 [20]。
此外,在强直性脊柱炎中,抗 CD74/CLIP 自身抗体和 B 细胞相关活化通路上调提示 CD74 参与 B 细胞异常免疫反应 [21]。在炎症性肠病相关纤维化中,MIF-CD74 信号通过上调 ILC3 的 IL-22 表达并增强 STAT3 活化,促进肠纤维化进展 [12]。这些结果说明,CD74 在炎症放大、免疫细胞功能失调和组织损伤中具有广泛作用。
5. CD74 靶向药物研究进展
目前,靶向CD74的药物研发呈现多元化趋势,涵盖单克隆抗体、抗体药物偶联物(ADC)、反义寡核苷酸(ASO)及基因治疗等多种类型,适应症涉及自身免疫性疾病(如系统性红斑狼疮、多发性硬化症)、血液肿瘤、恶病质及阿尔茨海默症等。研发阶段方面,多数项目处于临床前研究,少数已进入临床1期和2期。部分在研管线列举如下表:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| 米拉珠单抗 | CD74 | 单克隆抗体 | 系统性红斑狼疮 | Immunomedics, Inc. | 临床2期 |
| Bezetabart debotansine | CD74 x Tubulin | ADC | 血液肿瘤 | Sutro Biopharma, Inc. | 烨辉医药科技(上海)有限公司 | 临床1期 |
| Bud-ADC | CD74 | ADC | 系统性红斑狼疮 | 中国科学院 | 临床前 |
| THOR-213 | CD74 x MIF | ASO | 恶病质 | Thor Therapeutics Inc. | 临床前 |
| S-227928 | CD74 x Mcl-1 | ADC | 急性髓性白血病 | 其他血液系统恶性肿瘤 | Institut de Recherches Servier SAS | Novartis Institutes for Biomedical Research, Inc. | SARL Technologie Servier | 临床前 |
| SY2026 | CD74 | 抗体 | 肿瘤 | 上海祥耀生物科技有限责任公司 | 临床前 |
| AAV-CD74 gene therapy (University of Nebraska Medical Center) | CD74 | 腺相关病毒基因治疗 | 阿尔茨海默症 | uniQure NV | UNeMed Corp. | 临床前 |
| DRalpha1-hMOG-35-55 (Virogenomics Biodevelopment) | CD74 x HLA class II抗原 x MIF | 重组蛋白 | 多发性硬化症 | Virogenomics, Inc. | 临床前 |
(数据截止到2026年3月19日,来源于synapse)
6. CD74 研究工具
CD74 是连接经典抗原提呈功能与非经典炎症/增殖信号的重要分子。作为 MHC II 类分子的伴侣蛋白,它在适应性免疫中发挥基础作用;作为 MIF 受体及信号调节节点,它又广泛参与炎症、自身免疫、纤维化和肿瘤进展。当前证据表明,CD74 不仅是多类疾病的重要生物标志物,也具备较高的靶向治疗潜力。CUSABIO 提供 CD74 重组蛋白、抗体及 ELISA 试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD74 重组蛋白
Recombinant Human HLA class II histocompatibility antigen gamma chain (CD74), partial (Active); CSB-MP004956HU1(F2)
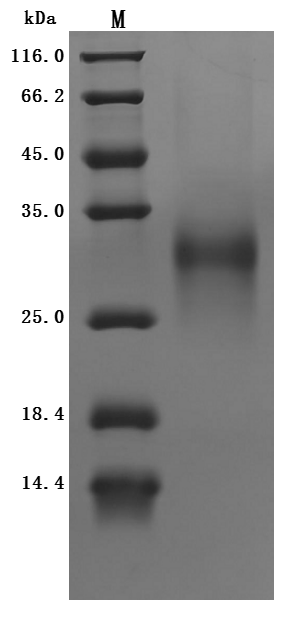
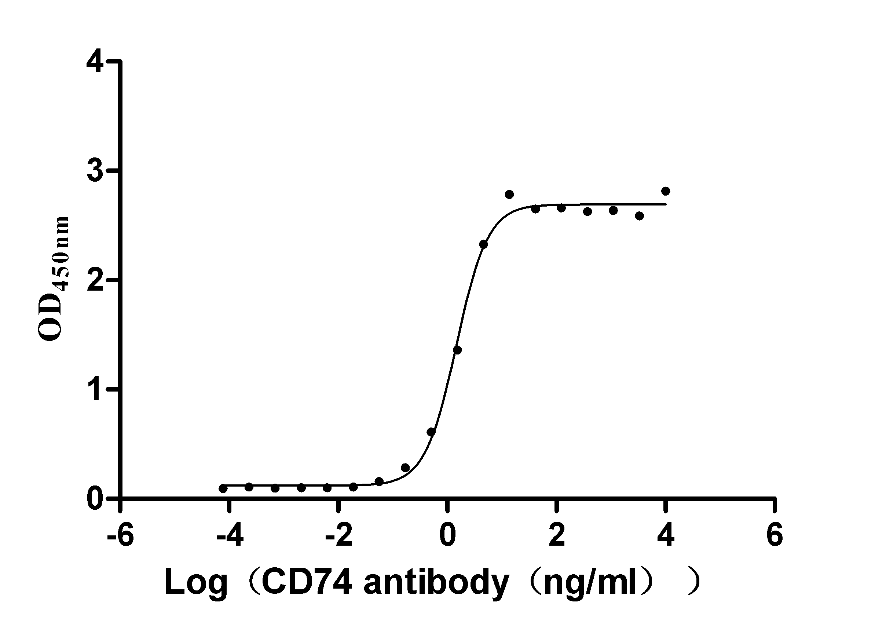
● CD74 抗体
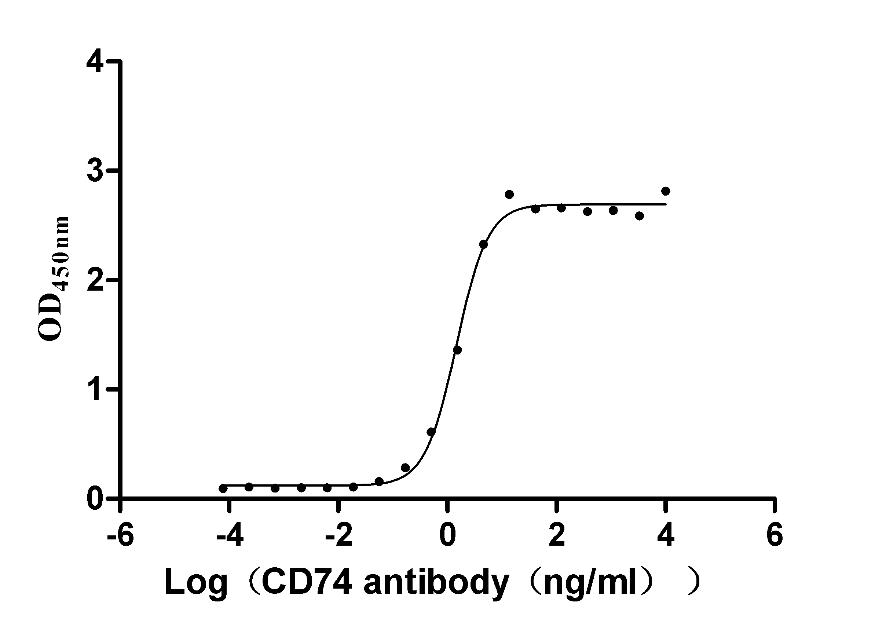
CD74 Recombinant Monoclonal Antibody
CSB-RA004956A1HU
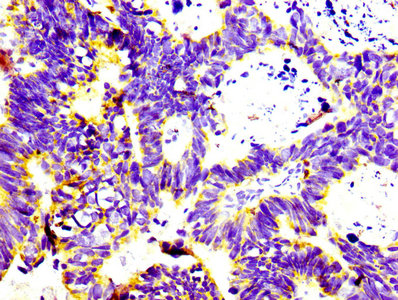
CD74 Recombinant Monoclonal Antibody
CSB-RA004956A0HU
● CD74 ELISA 试剂盒
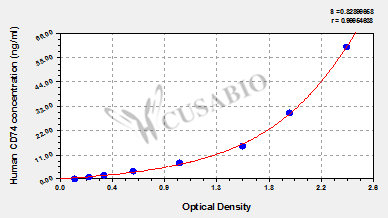
Human HLA class II histocompatibility antigen gamma chain(CD74) ELISA kit; CSB-EL004956HU
[1] L. Romero-Castillo, Taotao Li, Nhu-Nguyen Do, O. Sareila, Bingze Xu, Viktoria Hennings, Zhongwei Xu, Carolin Svensson, Ana Oliveira-Coelho, Zeynep Sener, V. Urbonaviciute, O. Ekwall, Harald Burkhardt, Rikard Holmdahl. (2024). Human MHC Class II and Invariant Chain Knock‐in Mice Mimic Rheumatoid Arthritis with Allele Restriction in Immune Response and Arthritis Association.
[2] Lin Zhang, Iris Woltering, Mathias Holzner, Markus Brandhofer, Carl-Christian Schaefer, Genta Bushati, Simon Ebert, Bishan Yang, Maximilian Muenchhoff, J. Hellmuth, C. Scherer, Christian Wichmann, David Effinger, Max Hübner, O. El Bounkari, Patrick Scheiermann, J. Bernhagen, A. Hoffmann. (2024). CD74 is a functional MIF receptor on activated CD4+ T cells.
[3] H. Bergmann. (2012). Business as usual: the p35 isoform of human CD74 retains function in antigen presentation.
[4] Shuchun Zhao, A. Molina, Abigail S. Yu, J. Hanson, Harry Cheung, Xiaofan Li, Y. Natkunam. (2018). High frequency of CD74 expression in lymphomas: implications for targeted therapy using a novel anti‐CD74.
[5] C. Abrahams, Xiaofan Li, M. Embry, Abigail S. Yu, Stellanie Krimm, S. Krueger, Nancy Y. Greenland, K. Wen, C. Jones, V. Dealmeida, W. Solis, S. Matheny, T. Kline, A. Yam, R. Stafford, Arun P. Wiita, T. Hallam, M. Lupher, A. Molina. (2018). Targeting CD74 in multiple myeloma with the novel, site-specific antibody-drug conjugate STRO-001.
[6] Xiaofan Li, C. Abrahams, Abigail S. Yu, M. Embry, R. Henningsen, V. Dealmeida, S. Matheny, T. Kline, A. Yam, R. Stafford, T. Hallam, M. Lupher, Arturo Molina. (2023). Targeting CD74 in B-cell non-Hodgkin lymphoma with the antibody-drug conjugate STRO-001.
[7] Guosheng Wu, Yu Sun, Kangan Wang, Zhengli Chen, Xingtong Wang, Fei Chang, Ting Li, P. Feng, Z. Xia. (2016). Relationship between elevated soluble CD74 and severity of experimental and clinical ALI/ARDS.
[8] Rossin Erbe, M. Stein, Tim A. Rand, J. Guinney. (2024). Abstract 2281: A tumor-intrinsic signature involving immunosuppression via MIF-CD74 signaling is associated with overall survival in ICT-treated lung adenocarcinoma.
[9] Mona M.Hosseini, Trevor Enright, Adam S. Duvall, Alex Chitsazan, Hsin-Yun Lin, A. Ors, B. Davis, Olga Nikolova, Erica Bresciani, J. Diemer, K. Craft, Catarina Menezes, M. Merguerian, Shawn Chong, Katherine R. Calvo, Shira G Glushakow-Smith, K. Gritsman, Lucy Godley, M. Horwitz, Sioban Keel, Lucio H Castilla, Emek Demir, H. Mohammed, Paul Liu, A. Agarwal. (2024). CD74 Signaling Regulates Inflammatory Stress to Drive Defective Hematopoiesis and Fitness Advantage of Progenitors in RUNX1-Familial Platelet Disorder.
[10] J. Zhou, Alice Shasha Cheng, Li Chen, L. X. Li, Ewud Agborbesong, Vicente E Torres, Peter C. Harris, Xiaogang Li. (2024). CD74 Promotes Cyst Growth and Renal Fibrosis in Autosomal Dominant Polycystic Kidney Disease.
[11] Sarah Zerimech, Hung Nguyen, A. Vandenbark, H. Offner, S. Baltan. (2023). Novel therapeutic for multiple sclerosis protects white matter function in EAE mouse model.
[12] Y. Zhao, Y. Tu, Q. Yang, Y. Zhang, D. Zou. (2025). OP21 MIF-CD74 signaling promotes intestinal LTi-like ILC3s activation and gut fibrosis via upregulating pSTAT3.
[13] Lisa Werr, Dennis Plenker, M. A. Dammert, C. Lorenz, J. Brägelmann, H. Tumbrink, Sebastian Klein, A. Schmitt, R. Büttner, T. Persigehl, K. Shokat, F. Wunderlich, A. Schram, M. Peifer, M. Sos, H. Reinhardt, Roman K. Thomas. (2022). CD74-NRG1 Fusions Are Oncogenic In Vivo and Induce Therapeutically Tractable ERBB2:ERBB3 Heterodimerization.
[14] Woosol Chris Hong, D. Lee, H. Kang, Myeong Jin Kim, Minsoo Kim, J. Kim, S. Fang, H. Kim, Joon Seong Park. (2023). CD74 Promotes a Pro-Inflammatory Tumor Microenvironment by Inducing S100A8 and S100A9 Secretion in Pancreatic Cancer.
[15] J. Burton, S. Ely, P. K. Reddy, R. Stein, D. Gold, Thomas M Cardillo, D. Goldenberg. (2004). CD74 Is Expressed by Multiple Myeloma and Is a Promising Target for Therapy.
[16] Zixiang Wang, Bingyu Wang, Yuan Feng, Jinwen Ye, Zhonghao Mao, Teng Zhang, Meining Xu, Wenjing Zhang, Xinlin Jiao, Qing Zhang, Youzhong Zhang, Baoxia Cui. (2024). Targeting tumor-associated macrophage-derived CD74 improves efficacy of neoadjuvant chemotherapy in combination with PD-1 blockade for cervical cancer.
[17] Jianghua Wang, Xiaoting Li, Guanxi Xiao, Jayesh Desai, S. Frentzas, Z. Wang, Yu Xia, Baiyong Li. (2024). CD74 is associated with inflamed tumor immune microenvironment and predicts responsiveness to PD-1/CTLA-4 bispecific antibody in patients with solid tumors.
[18] A. Ghoochani, M. Schwarz, E. Yakubov, T. Engelhorn, A. Doerfler, M. Buchfelder, R. Bucala, N. Savaskan, I. Eyüpoglu. (2016). MIF-CD74 impedes microglial M1 polarization and facilitates brain tumorigenesis.
[19] R. Meza‐Romero, G. Benedek, Grant Gerstner, G. Kent, Ha Nguyen, H. Offner, A. Vandenbark. (2018). Increased CD74 binding and EAE treatment efficacy of a modified DRα1 molecular construct.
[20] Jiangyi Liu, Xingyun Liao, Na Li, Zongren Xu, Wang Yang, Hongxiu Zhou, Yusen Liu, Zhi Zhang, Guoqing Wang, Shengping Hou. (2024). Single‐cell RNA sequencing reveals inflammatory retinal microglia in experimental autoimmune uveitis.
[21] R. Wilbrink, A. Spoorenberg, F. Kroese, G. Verstappen. (2023). POS0436 INCREASED EXPRESSION OF PATHWAYS INVOLVED IN B CELL ACTIVATION IN PATIENTS WITH ANKYLOSING SPONDYLITIS.



