武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
CD40LG:从免疫缺陷到肿瘤免疫,一文讲透这个关键共刺激分子
79 人阅读发布时间:2026-04-07 10:29
CD40LG(CD154)是TNF超家族中的重要共刺激分子,在T细胞依赖性B细胞活化、抗体类别转换和免疫记忆形成中发挥核心作用。本文系统综述了CD40LG-CD40信号轴的分子机制,重点阐述了其在NF-κB、JAK-STAT通路及非编码RNA调控中的功能,并梳理了该信号异常与X-连锁高IgM综合征(XHIGM)、自身免疫病(如类风湿关节炎、系统性红斑狼疮)、急性肝损伤及动脉粥样硬化等疾病的关系,旨在为CD40LG相关疾病的机制研究与精准治疗提供参考。
1. CD40LG 概述
2. CD40LG 的作用机制与信号通路
3. CD40LG 相关疾病
4. CD40-CD40LG 轴的药物研究进展
5. CD40LG 相关研究工具
1. CD40LG 概述
CD40LG(又称 CD154)是免疫系统中的关键共刺激分子,属于肿瘤坏死因子(TNF)超家族。它通常以三聚体形式与 CD40 结合,在 T 细胞依赖性 B 细胞活化、抗体类别转换和免疫记忆形成中发挥重要作用 [1]。早期研究主要关注其在活化 CD4+ T 细胞中的表达,但后续研究表明,CD40LG 也可见于血小板、B 细胞、内皮细胞和巨噬细胞等多种细胞,其中血小板是循环可溶性 CD40LG 的主要来源 [1,2]。
CD40LG-CD40 轴不仅参与正常免疫应答,也与多种疾病密切相关。CD40LG 功能缺陷可导致 X-连锁高 IgM 综合征(XHIGM),引起抗体类别转换障碍和感染易感性增加 [3,4];该通路的异常激活还参与自身免疫、炎症反应、动脉粥样硬化及肿瘤免疫调控等过程 [1,18,21]。此外,CD40LG 的作用具有明显的细胞类型和疾病背景依赖性,在不同微环境中可表现为促炎、免疫支持或免疫抑制效应 [6,7]。因此,系统梳理 CD40LG 的分子特征、信号机制、疾病关联及药物研究进展,对于理解其生物学功能和临床转化价值具有重要意义。
2. CD40LG 的作用机制与信号通路
2.1 经典信号通路:NF-κB 与 JAK-STAT
CD40-CD40LG 结合后可激活多条经典下游通路,其中最重要的是 NF-κB 和 JAK-STAT。该信号轴可参与细胞增殖、分化、细胞因子产生及凋亡调控。研究表明,CD40 可通过激活 JAK-STAT 通路抑制乙肝病毒复制和转录,并进一步调节 BST2 等干扰素刺激基因的表达,提示其在抗病毒免疫中具有重要作用 [8]。此外,NF-κB 与凋亡相关信号也与 CD40LG 密切相关;在肺炎治疗机制研究中,CD40LG 被确定为 NF-κB 和凋亡通路中的关键靶点 [9]。
2.2 miRNA 调控:影响炎症、血管生成与白血病信号应答
除经典蛋白信号外,miRNA 也是调控 CD40/CD40LG 轴的重要层面。研究发现,miR-424 和 miR-503 可直接靶向 CD40 的 3'UTR,抑制其在内皮细胞中的表达 [10]。在促炎刺激下,这两种 miRNA 下调,导致 CD40 表达上升,从而促进炎症相关血管生成。进一步来看,miR-424 和 miR-503 又受 PPARγ 直接调控,因此形成了 PPARγ 依赖的 miR-424/503-CD40 轴 [10]。
在慢性淋巴细胞白血病中,miR-29 家族也参与 CD40 信号调节。miR-29a、miR-29b 和 miR-29c 的下调,可通过直接靶向 TRAF4,增强 CLL 细胞对 CD40 激活及其下游 NF-κB 信号的反应 [11]。同时,BCR 信号可通过 MYC 抑制 miR-29 表达,进而强化 CD40-NF-κB 信号,这一调控过程可被伊布替尼和 Idelalisib 等 BCR 抑制剂干预 [11]。
2.3 lncRNA 与 ceRNA 机制:扩展 CD40 调控网络
长链非编码 RNA 也参与 CD40 轴调控。例如,lncRNA MSTRG.22719.16 可通过 ceRNA 机制与 ocu-miR-326-5p 相互作用,进而调控 CD40 表达。在 PMMA 骨水泥诱导的局部血栓形成中,MSTRG.22719.16/ocu-miR-326-5p/CD40 轴的活化可减少血栓形成,提示其具有潜在干预价值 [12]。总体来看,CD40-miRNA 轴在细胞命运决定和病理状态调节中具有重要意义 [13],但其系统性机制仍有待进一步研究。
3. CD40LG 相关疾病
CD40LG 功能异常与多种疾病相关,包括原发性免疫缺陷、自身免疫与炎症性疾病,以及肿瘤。不同疾病中,该分子的作用方向和强度受细胞来源与微环境影响明显。
3.1 X-连锁高 IgM 综合征(XHIGM)
XHIGM 是 CD40LG 缺陷最典型的疾病类型。患者常出现反复感染,病原体既包括常见细菌,也包括卡氏肺孢子虫、隐孢子虫、马尔尼菲篮状菌、巨细胞病毒和腺病毒等机会性感染或病毒感染 [3,14,15]。呼吸道和胆道系统是常见受累部位,部分患者还可能以间质性肺炎或肺泡蛋白沉积症为首要表现 [16, 17]。此外,患者还可伴随自身免疫和炎症性并发症,增加预后风险 [18]。
CD40LG 基因突变类型与临床表型密切相关。部分错义突变可保留 CD40L 表达,但削弱其与 CD40 的结合能力,从而形成相对较轻或非典型表型 [4];而截短突变通常提示更严重的功能缺陷 [17]。诊断上,XHIGM 并不能仅依赖免疫球蛋白谱,因为部分患者可呈现非典型血清学特征。结合基因检测、流式细胞术及 CD40 结合功能分析,才能更准确地识别这类患者 [4, 15]。
3.2 自身免疫与炎症性疾病
在类风湿关节炎中,CD40LG 被认为具有潜在生物标志物价值。研究显示,RA 患者血清中 CD40LG 抗体水平升高,尤其在伴有间质性肺病或严重骨破坏者中更为明显,提示其可能与疾病活动度和并发症风险相关 [19]。在系统性红斑狼疮中,CD40LG-CD40 轴异常活化可促进 B 细胞活化和自身抗体生成,是重要的致病机制之一 [20]。针对该通路的阻断策略已在动物模型中显示出缓解狼疮性肾炎和整体自身免疫症状的潜力 [20]。
在急性肝损伤中,IFNγ-CD40 轴与肝内微循环障碍密切相关。IFNγ 可上调内皮细胞 CD40 表达,促进其与 CD40LG 相互作用,诱导组织因子表达并加重凝血和肝损伤 [21]。在动脉粥样硬化中,CD40LG 的作用则表现出细胞来源差异:T 细胞来源的 CD40L 更影响斑块形成和稳定性,而血小板来源的 CD40L 对血栓形成更重要 [1]。此外,在 HBV 清除、局部血栓形成及过敏原耐受等场景中,CD40/CD40LG 轴也发挥重要调节作用 [6,8,12]。
3.3 肿瘤发生与进展
CD40LG 在肿瘤中的作用具有双重性。以乳腺癌为例,其在肿瘤组织中的低表达与更晚期分期和更差预后相关,同时与多种免疫细胞浸润显著相关,提示其可能参与肿瘤免疫微环境塑造 [21]。在泛癌种分析中,CD40LG 还被视为 T 细胞启动标志物,其表达与 MSI-H、高 TMB 和 PD-L1 高表达等免疫治疗相关特征呈正相关 [22]。
在特定肿瘤中,CD40LG 还参与疾病进展机制。例如,在 T-ALL 中,BACH2 可通过抑制 CD28 和 CD40LG 表达影响肿瘤细胞存活和增殖 [23];在 Waldenström 巨球蛋白血症中,CD40/CD40L 轴可支持 Treg 介导的免疫抑制微环境 [7];在部分 T 细胞淋巴瘤及口腔鳞癌相关研究中,CD40LG 也被提示参与肿瘤维持或药物响应 [24-26]。
4. CD40-CD40LG 轴的药物研究进展
围绕 CD40-CD40LG 轴的药物开发主要分为两类:一类是抑制该通路,用于自身免疫病、移植排斥等场景;另一类是激活该通路,以增强抗肿瘤免疫。目前,靶向CD40L的药物研发进展迅速,多种药物类型(包括融合蛋白、单克隆抗体、溶瘤病毒、小分子化药及治疗性疫苗等)已在自身免疫性疾病、器官移植排斥反应及多种恶性肿瘤等领域进入临床研究阶段,部分候选药物已推进至临床3期。下表汇总了代表性在研管线的相关信息:
| 药物 | 靶点 | 药物类型 | 在研适应症(疾病名) | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| Dazodalibep | CD40L | 融合蛋白 | 干燥综合征 | 狼疮性肾炎 | 局灶性节段性肾小球硬化症 | Amgen, Inc. | The Ohio State University Wexner Medical Center | Horizon Therapeutics Ltd. (Ireland) | 临床3期 |
| Dapirolizumab pegol | CD40L | 单克隆抗体 | 系统性红斑狼疮 | Biogen, Inc. | UCB Biopharma SRL | 优时比贸易(上海)有限公司 | UCB SA | 临床3期 |
| Frexalimab | CD40L | 单克隆抗体 | 多发性硬化症 | 继发进展型多发性硬化 | 复发性多发性硬化 | 肾移植排斥反应等 | Sanofi | Sanofi-Aventis Recherche & Développement SA | ImmuNext, Inc. | 临床3期 |
| Tegoprubart | CD40L | 单克隆抗体 | 免疫球蛋白a肾病 | 肾移植排斥反应 | 肌萎缩侧索硬化 | 心脏移植排斥反应 | ALS Therapy Development Foundation, Inc. | Eledon Pharmaceuticals, Inc. | 临床2期 |
| Delolimogene mupadenorepvec | 4-1BBL x CD40L | 溶瘤病毒 | 胆道癌 | 胰腺导管腺癌 | Uppsala University Hospital | Lokon Pharma AB | 临床2期 |
| OPT-101 | CD40L | 小分子化药 | 社区获得性肺炎 | 脓毒症 | OP LLC | 临床2期 |
| TriMixDC | CD40L x CD70 x TLR4 | 治疗性疫苗 | 树突状细胞疫苗 | 黑色素瘤 | - | 临床2期 |
| TNX-1500 | CD40L | 单克隆抗体 | 免疫抑制 | 肾移植排斥反应 | 自身免疫性疾病 | 器官移植排斥 | Tonix Pharmaceuticals Holding Corp. | Tonix Pharmaceuticals, Inc. | 临床2期 |
| Bria-OTS | CD40L x CD80 x CD86 x CSF-3R x Type I IFN Receptor x IL-12R x IL-7Rα | 治疗性疫苗 | 复发性乳腺癌 | 乳腺癌 | BriaCell Therapeutics Corp. | 临床1/2期 |
| Adze1.C(Adze Biotechnology) | CD40L | 溶瘤病毒 | 黑色素瘤 | 转移性黑色素瘤 | 膀胱癌 | 胶质母细胞瘤 | 肝癌 | 三阴性乳腺癌 | Adze Biotechnology, Inc. | Adze Biotechnology Australia Pty Ltd | 临床1期 |
(数据截止到2026年3月19日,来源于synapse)
5. CD40LG 相关研究工具
CD40LG 是适应性免疫调控中的关键分子,在 B 细胞活化、抗体类别转换和免疫记忆形成中发挥核心作用。其功能异常与 XHIGM、自身免疫病、炎症性疾病和肿瘤密切相关 [3,18,21]。同时,CD40LG 兼具疾病标志物和治疗靶点的双重潜力,在精准医学中的价值正不断受到重视。CUSABIO 提供 CD40LG 重组蛋白、抗体及 ELISA 试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD40LG 重组蛋白
Recombinant Human CD40 ligand (CD40LG), partial (Active); CSB-MP004937HU3
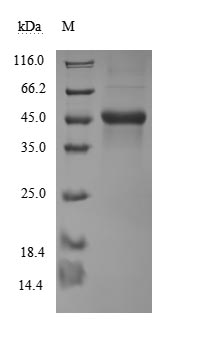
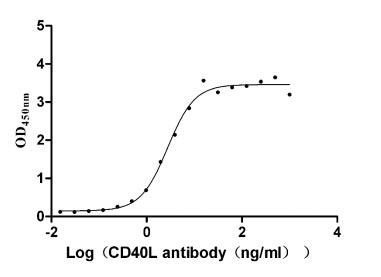
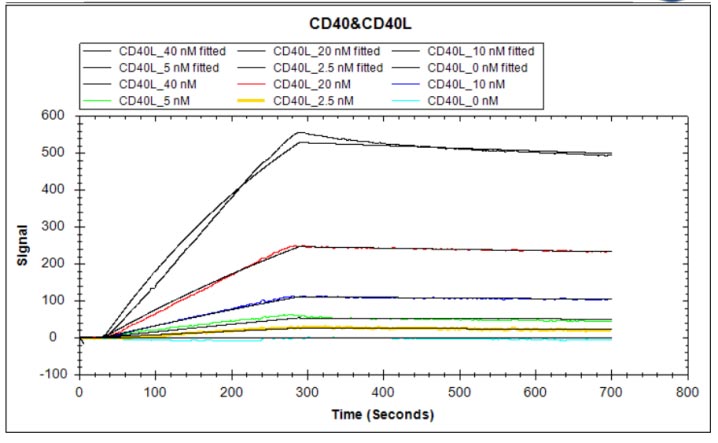
Recombinant Mouse CD40 ligand (Cd40lg), partial (Active); CSB-MP004937MO1

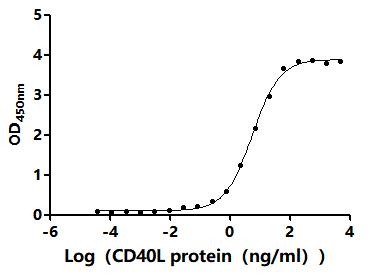
● CD40LG 抗体
CD40LG Antibody
CSB-PA06005A0Rb
CD40LG Antibody
CSB-PA004937GA01HU
● CD40LG ELISA 试剂盒
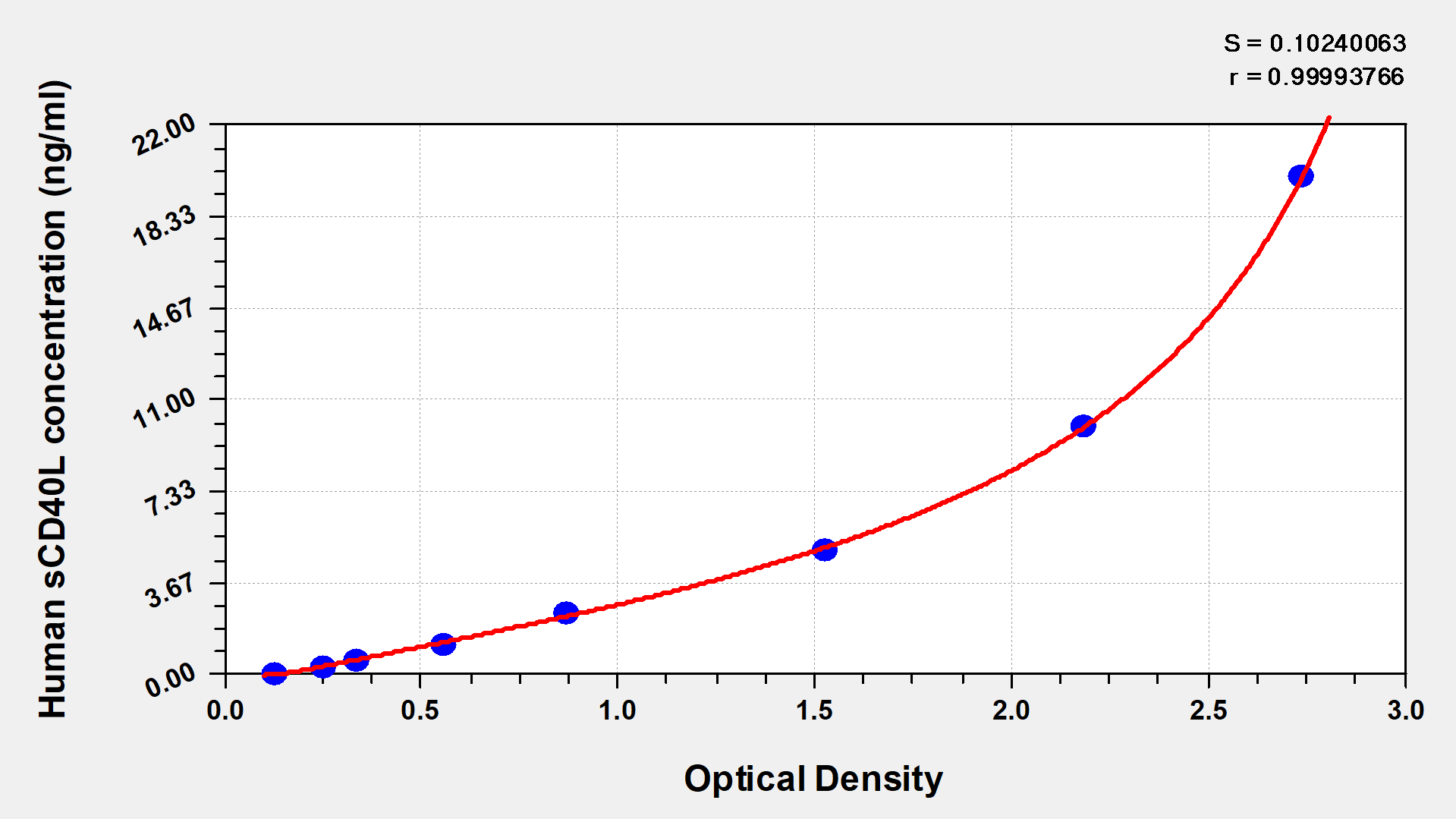
Human Soluble Cluster of differentiation 40 ligand,sCD40L ELISA Kit
CSB-E04716h
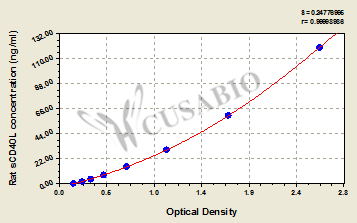
Rat Soluble Cluster of differentiation 40 ligand,sCD40L ELISA Kit
CSB-E07395r
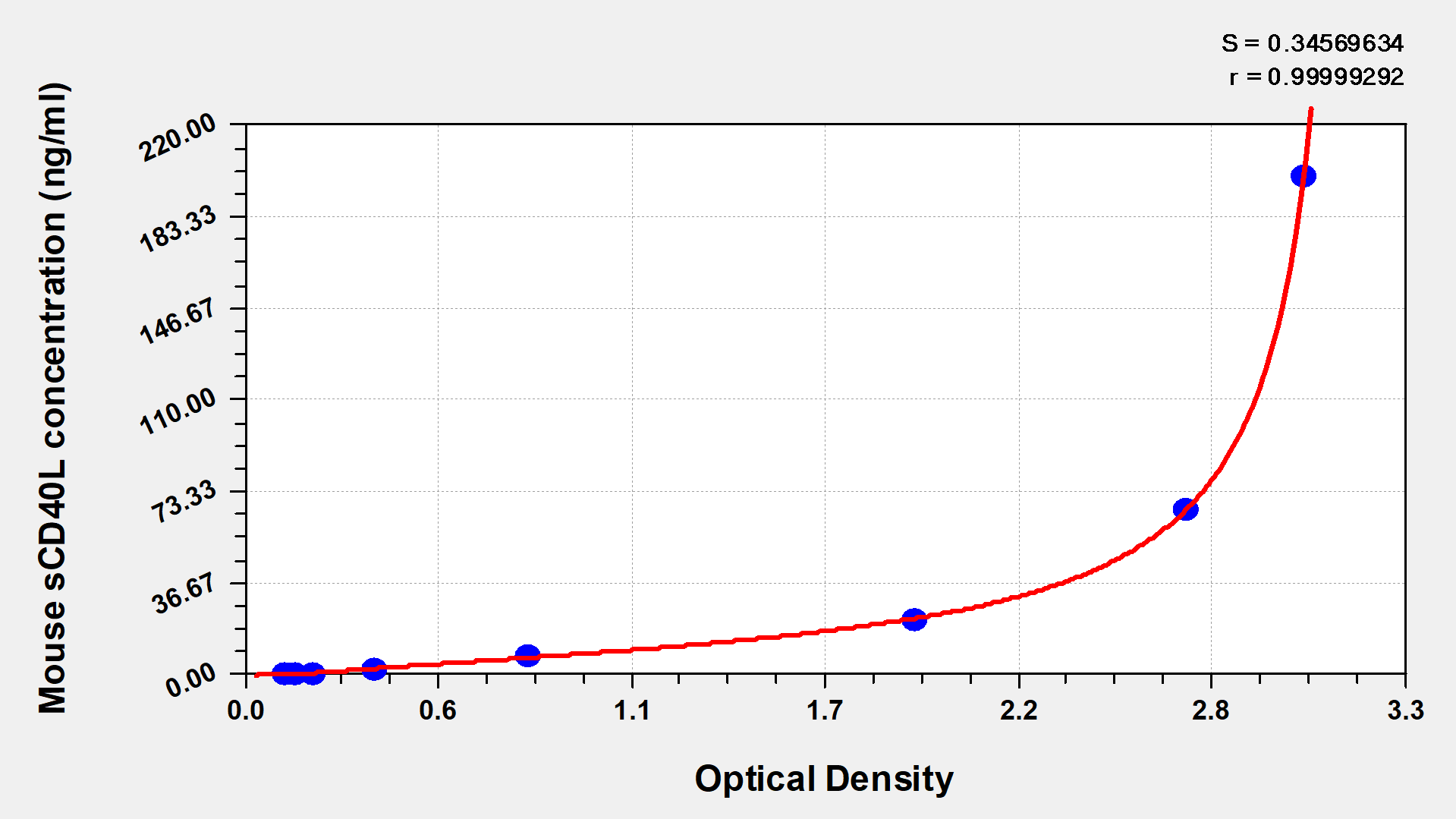
Mouse Soluble Cluster of differentiation 40 ligand,sCD40L ELISA Kit
CSB-E04717m
[1] M. Lacy, C. Bürger, Annelie Shami, M. Ahmadsei, H. Winkels, K. Nitz, C. van Tiel, T. Seijkens, Pascal J. H. Kusters, Ela Karshovka, K. Prange, Yuting Wu, S. Brouns, Sigrid Unterlugauer, Marijke J. E. Kuijpers, M. Reiche, S. Steffens, A. Edsfeldt, R. Megens, J. Heemskerk, I. Gonçalves, C. Weber, N. Gerdes, D. Atzler, E. Lutgens. (2021). Cell-specific and divergent roles of the CD40L-CD40 axis in atherosclerotic vascular disease.
[2] C. Aloui, Antoine Prigent, S. Tariket, C. Sut, Jocelyne Fagan, F. Cognasse, T. Chakroun, O. Garraud, S. Laradi. (2016). Levels of human platelet-derived soluble CD40 ligand depend on haplotypes of CD40LG-CD40-ITGA2.
[3] B. Neven, F. Ferrua. (2020). Hematopoietic Stem Cell Transplantation for Combined Immunodeficiencies, on Behalf of IEWP-EBMT.
[4] T. Nishikawa, Dan Tomomasa, Atsushi Hijikata, Hiroshi Kasabata, Yasuhiro Okamoto, H. Ochs, H. Kanegane. (2025). Case Report: CD40LG Arg203Ile variant underlies atypical phenotype of X-linked hyper IgM syndrome.
[5] K. Antoniou, F. Ender, T. Vollbrandt, Y. Laumonnier, Franziska Rathmann, C. Pasare, Harinder Singh, J. Köhl. (2020). Allergen-Induced C5a/C5aR1 Axis Activation in Pulmonary CD11b+ cDCs Promotes Pulmonary Tolerance through Downregulation of CD40.
[6] A. Sacco, V. Desantis, J. Celay, V. Giustini, Fabio Rigali, Francesco D Savino, M. Cea, D. Soncini, A. Cagnetta, Antonio Giovanni Solimando, D. D'Aliberti, S. Spinelli, Daniele Ramazzotti, C. Almici, K. Todoerti, A. Neri, A. Anastasia, A. Tucci, M. Motta, M. Chiarini, Y. Kawano, Jose-Al Martinez-Climent, R. Piazza, A. Roccaro. (2023). Targeting the immune microenvironment in Waldenström Macroglobulinemia via halting the CD40/CD40-ligand axis.
[7] Jiaxuan Chen, Haitao Chen, Haoming Mai, Shuang Lou, Mengqi Luo, Haisheng Xie, Bin Zhou, J. Hou, Deke Jiang. (2022). A functional variant of CD40 modulates clearance of hepatitis B virus in hepatocytes via regulation of the ANXA2/CD40/BST2 axis.
[8] Liping Sun, Dandan Wang, Yan Xu, Wenxiu Qi, Yanbo Wang. (2020). Evidence of TCM Theory in Treating the Same Disease with Different Methods: Treatment of Pneumonia with Ephedra sinica and Scutellariae Radix as an Example.
[9] . (2017). A PPARγ-dependent miR-424/503-CD40 axis regulates inflammation mediated angiogenesis.
[10] Sonali Sharma, G. Pavlasová, V. Seda, K. Černá, E. Vojáčková, D. Filip, L. Ondrisova, Veronika Šandová, L. Košťálová, P. F. Zeni, M. Borsky, J. Oppelt, K. Lišková, L. Křen, A. Janíková, Š. Pospíšilová, S. Fernandes, M. Shehata, U. Jaeger, M. Doubek, M. Davids, Jennifer R. Brown, J. Mayer, T. Kipps, M. Mraz. (2020). miR-29 Modulates CD40 Signaling in Chronic Lymphocytic Leukemia by Targeting TRAF4: an Axis Affected by BCR inhibitors.
[11] Linchao Sang, Luobin Ding, Kangning Hao, Ce Zhang, Xiaoyu Shen, Hui Sun, Dehao Fu, Xiangbei Qi. (2023). LncRNA MSTRG.22719.16 mediates the reduction of enoxaparin sodium high-viscosity bone cement-induced thrombosis by targeting the ocu-miR-326-5p/CD40 axis.
[12] S. Salunkhe, Tushar Vaidya. (2020). CD40-miRNA axis controls prospective cell fate determinants during B cell differentiation.
[13] H. Fan, Li Huang, Diyuan Yang, Changhao Zhang, Q. Zeng, G. Yin, G. Lu, Kunling Shen. (2022). Respiratory infections in X-linked hyper-IgM syndrome with CD40LG mutation: a case series of seven children in China.
[14] A. Khojah, L. Gunderman, Mohammad Binhussein, A. Bukhari, Imad Khojah. (2023). A Case Report of Hyper-IgM Syndrome Patient with Normal Serum IgA Level.
[15] Tianliu Wang, Li-Fang Wu, Junguo Chen, Wen Zhu, Hua Wang, Xiao-Lin Liu, Yi-qun Teng. (2019). X-linked hyper-IgM syndrome complicated with interstitial pneumonia and liver injury: a new mutation locus in the CD40LG gene.
[16] Hong-bo Xu, Maolin Tian, Yong-hua Bai, X. Ran, Lei Li, Yan Chen. (2023). CD40LG-associated X-linked Hyper-IgM Syndrome (XHIGM) with pulmonary alveolar proteinosis: a case report.
[17] W. Rae, D. Ward, C. Mattocks, Yifang Gao, R. Pengelly, Sanjay Patel, S. Ennis, S. Faust, Anthony P. Williams. (2017). Autoimmunity/inflammation in a monogenic primary immunodeficiency cohort.
[18] Chuanhui Yao, Hui Xu, Xun Gong, Xieli Ma, Yuchen Yang, Dan Dou, Qiu-wei Peng, Juan Jiao, Xiaopo Tang, Quan Jiang, Congmin Xia. (2025). CD40LG as a Biomarker in Rheumatoid Arthritis: Links to Bone Destruction and Interstitial Lung Disease ‐ A Bioinformatic Analysis With Clinical Validation.
[19] Tian-Liang Fang, Baoqi Li, Meng Li, Yu-long Zhang, Zhang Jing, Yuan Li, Tianyuan Xue, Zhirang Zhang, Wen-li Fang, Zhongda Lin, Fanqiang Meng, Liyan Li, Yang Yang, Xingding Zhang, Xin Liang, Shu-Na Chen, Jun Chen, Xudong Zhang. (2023). Engineered Cell Membrane Vesicles Expressing CD40 Alleviate System Lupus Nephritis by Intervening B Cell Activation.
[20] M. Kurokawa, T. Goya, M. Kohjima, Masatake Tanaka, Sadahiro Iwabuchi, Shigeyuki Shichino, S. Ueha, Tomonobu Hioki, Tomomi Aoyagi, Masaki Kato, Kouji Matsushima, Yoshihiro Ogawa. (2024). Microcirculatory disturbance in acute liver injury is triggered by IFNγ-CD40 axis.
[21] Manqiu Yuan, Jianying Pei, Ruihao Li, Lirong Tian, Xin-bin He, Yanping Li. (2021). CD40LG as a Prognostic Molecular Marker Regulates Tumor Microenvironment Through Immune Process in Breast Cancer.
[22] H. Miyashita, R. Kurzrock, N. Bevins, Kartheeswaran Thangathurai, Suzanna Lee, S. Pabla, M. Nesline, S. Glenn, J. Conroy, P. DePietro, E. Rubin, J. Sicklick, S. Kato. (2023). T-cell priming transcriptomic markers: implications of immunome heterogeneity for precision immunotherapy.
[23] Min Feng, Bailing Zhang, Guilan Li, Yan Yang, Jiangyuan Liu, Ziting Zhang, Bing Zhou, Han Zhang. (2024). BACH2-mediated CD28 and CD40LG axes contribute to pathogenesis and progression of T-cell lymphoblastic leukemia.
[24] M. Fujisawa, Tran Bich Nguyen, Yoshiaki Abe, Y. Suehara, K. Fukumoto, S. Suma, K. Makishima, C. Kaneko, Yen Thi Minh Nguyen, K. Usuki, K. Narita, K. Matsue, N. Nakamura, S. Ishikawa, F. Miura, Takashi Ito, A. Suzuki, Yutaka Suzuki, S. Mizuno, Satoru Takahashi, S. Chiba, M. Sakata-Yanagimoto. (2022). Clonal germinal center B cells function as a niche for T-cell lymphoma.
[25] Sofia Papadakos, Hawraa Issa, Abdulaziz Alamri, Abdullah Alamri, A. Semlali. (2024). Rapamycin as a Potential Alternative Drug for Squamous Cell Gingiva Carcinoma (Ca9-22): A Focus on Cell Cycle, Apoptosis and Autophagy Genetic Profile.
[26] E. Fukutani, P. I. Ramos, J. I. Kasprzykowski, L. G. Azevedo, M. Rodrigues, J. Lima, Helton Fábio Santos de Araújo Junior, K. Fukutani, A. T. D. de Queiroz. (2019). Meta-Analysis of HTLV-1-Infected Patients Identifies CD40LG and GBP2 as Markers of ATLL and HAM/TSP Clinical Status: Two Genes Beat as One.



