武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
FGF2:从细胞增殖到肿瘤耐药,一文读懂这个多效性生长因子的临床转化潜力
151 人阅读发布时间:2026-04-07 10:31
成纤维细胞生长因子2(FGF2)是一种多功能生长因子,广泛参与细胞增殖、血管生成、组织修复及肿瘤进展等过程。本文系统综述了FGF2的分子结构、信号通路(如PI3K/AKT/mTOR、MAPK/ERK)及其在肿瘤、神经系统疾病、视网膜病变和骨骼疾病中的作用机制,旨在为FGF2相关疾病的机制研究与精准治疗提供参考。
1. FGF2概述及其生物学意义
2. FGF2的分子生物学特性与作用机制
3. FGF2信号转导通路与调控网络
4. FGF2与相关疾病的病理生理学
5. FGF2靶向药物研究进展
6. FGF2研究工具
1. FGF2概述及其生物学意义
成纤维细胞生长因子2(FGF2),又称碱性成纤维细胞生长因子(bFGF),是FGF家族的重要成员,在细胞增殖、分化、迁移、血管生成和组织修复等过程中发挥关键作用。FGF家族属于结构较为保守的肽类生长因子,主要通过与成纤维细胞生长因子受体(FGFRs)及肝素硫酸(HS)蛋白聚糖结合,激活下游信号通路并调控细胞行为 [1, 2]。研究表明,FGF2可促进FGFR构象改变并增强其激活水平,而HS及其修饰在FGF2/FGFR信号调控中也具有重要作用 [1-3]。
FGF2参与多种关键生物学过程。在细胞增殖方面,YAP可通过上调FGFR表达增强神经干细胞对FGF2的响应;在ER+乳腺癌中,FGF2还能激活ERα和PR信号,促进肿瘤细胞增殖并诱导内分泌治疗耐药 [4, 5]。在血管生成方面,FGF2是重要的促血管生成因子,常与VEGF等分子共同参与血管形成与重塑,并在心肌损伤修复、视网膜病变和缺血性卒中等过程中发挥作用 [6-10]。在分化调控中,FGF2与成骨、成牙本质分化密切相关,同时在组织修复和抗纤维化中也表现出积极作用 [11-15]。
FGF2还存在低分子量(LMW)和高分子量(HMW)等不同亚型,两者在细胞内定位和功能上存在差异,并可能在疾病过程中发挥不同作用 [16]。同时,FGF2异常表达或信号失衡与多种疾病密切相关,尤其涉及肿瘤进展、治疗耐药及部分炎症相关疾病 [17-21]。总体来看,FGF2兼具重要的基础研究价值和临床转化潜力,深入研究其作用机制、信号通路及疾病关联,对于理解相关疾病发生发展并探索新的治疗策略具有重要意义。
2. FGF2的分子生物学特性与作用机制
2.1 FGF2的结构、亚型与非经典分泌
FGF2是FGF家族中功能多样的重要成员,其蛋白结构具有家族共同特征,即高度保守的中央β-折叠桶结构,该结构域对其与FGFR及硫酸肝素相关分子的结合至关重要。FGF2的生物学复杂性在很大程度上来源于其多种蛋白亚型。Fgf2基因可通过不同起始密码子翻译生成低分子量(约18 kDa)和高分子量(约22--24 kDa)异构体 [16, 23]。其中,LMW FGF2主要定位于细胞质和细胞核,而HMW FGF2则更多集中于细胞核。不同亚型在细胞内定位和功能上的差异,使FGF2在不同组织和疾病背景下呈现出更复杂的调控模式。
值得注意的是,FGF2缺乏经典信号肽,因此其分泌并不依赖传统的内质网-高尔基体途径,而是通过非经典分泌方式释放到细胞外。这一特性决定了FGF2在细胞外基质中的沉积、局部浓度形成及旁分泌/自分泌调控均具有独特性,也为其在发育、修复和疾病中的时空特异性作用提供了基础。
2.2 FGF2与受体(FGFRs)及共受体(HSPGs)的结合与活化
FGF2信号转导始于其与细胞表面FGFRs的特异性结合,这一过程通常依赖肝素硫酸蛋白聚糖(HSPGs)的协同作用。FGF2、FGFR和HSPG共同形成功能性三元复合物,被认为是FGF2发挥生物学活性的基础。FGF2与受体结合后可促进FGFR二聚化,并引发胞内酪氨酸激酶结构域的磷酸化,继而启动一系列下游信号级联反应。
不过,FGF2与HS/HSPGs的作用并非简单的"有或无"关系。已有研究显示,降低FGF2与HS的结合能力并不会完全消除FGFR1信号 [2],说明共受体的贡献可能具有情境依赖性。与此同时,特定类型的HS修饰,如2-O硫酸化,则对FGF2/FGFR1/Erk1/2通路的有效激活仍然至关重要 [3]。因此,FGF2受体复合体的形成与激活并不是单一分子事件,而是受到配体、受体及糖胺聚糖微环境共同调控的精细过程。
2.3 FGF2调控的细胞生物学过程
FGF2参与调控多种关键细胞行为,包括细胞增殖、迁移、分化、抗凋亡及血管生成等。在干细胞维持与增殖方面,FGF2对于骨髓间充质干细胞等细胞群体的干性维持具有重要意义;在神经系统中,YAP通过增强细胞对FGF2的响应促进神经干细胞扩增 [4]。在肿瘤环境中,FGF2则可推动肿瘤细胞增殖并促进治疗耐受形成 [5, 17]。
在分化方面,FGF2对成骨和成牙本质分化的调控尤其突出。它既可通过ERK-Runx2轴增强成骨分化 [13],也可在特定细胞背景下通过抑制PI3K/AKT通路促进SCAP成骨/成牙本质分化 [11]。在组织修复和血管生成中,FGF2可通过与VEGF等因子协同,增强血管新生、改善局部供血,并促进损伤组织修复 [6, 8, 10, 14]。因此,FGF2并非仅仅是单一功能生长因子,而是贯穿多类细胞过程的重要调控节点。
3. FGF2信号转导通路与调控网络
3.1 经典的PI3K/AKT/mTOR信号通路
FGF2通过与FGFR结合激活多条细胞内信号通路,其中PI3K/AKT/mTOR通路是其核心下游之一。FGFR激活后可招募并激活PI3K,促使PIP2转化为PIP3,从而进一步激活AKT。活化的AKT可调节mTOR及其他下游效应分子,最终影响细胞生长、代谢、存活和抗凋亡等过程。
在不同疾病和组织背景下,FGF2对PI3K/AKT/mTOR通路的调控具有多样性。例如,在病理性血管生成中,PIK3IP1下调可增强PI3K-AKT信号,并提升FGF2等促血管生成因子的表达,从而加重异常血管生成 [9]。在组织修复中,CXCR4/Akt/FGF2轴可促进FGF2分泌并增强组织再生 [14]。但在某些分化场景中,FGF2又可能通过抑制PI3K/AKT通路发挥促分化作用,如在SCAP成骨/成牙本质分化中所见 [11]。这说明FGF2与PI3K/AKT/mTOR通路之间并非单向激活关系,而是具有明显的细胞类型和生物学情境依赖性。
3.2 MAPK/ERK及其相关信号通路
MAPK/ERK通路是FGF2介导细胞效应的另一条经典通路。FGF2与FGFR结合后,通过适配蛋白和Ras-Raf-MEK级联反应激活ERK,进而调控细胞生长、分化、迁移和应激反应。YAP可通过上调FGFR1-4表达增强细胞对FGF2的响应,并进一步激活MAPK和AKT信号,从而促进胚胎神经干细胞增殖 [4]。在骨形成过程中,FGF2激活ERK后可增强Runx2蛋白稳定性和转录活性,对成骨细胞分化和骨骼形成发挥积极作用 [13]。
然而,MAPK/ERK通路也是FGF2参与肿瘤耐药的重要机制之一。在KIT突变型黑色素瘤中,FGF2轴通过MAPK通路抑制BIM表达,促进对奈洛替尼的耐药 [18]。在胶质瘤中,放疗诱导的YAP激活可上调FGF2并进一步增强MAPK-ERK信号,形成放射抵抗 [19]。因此,FGF2-MAPK/ERK轴既是正常生理调控的重要通路,也是肿瘤进展和治疗失败的重要分子基础。
3.3 FGF2信号的交叉对话与复杂调控机制
FGF2信号网络并非独立运行,而是与VEGF/VEGFR、Src、YAP、CXCR4等多条信号通路发生复杂交叉调控。以血管生成为例,FGF2与VEGF常共同参与血管形成与重塑,在缺血修复和视网膜病变中均表现出明显协同作用 [6, 7, 8, 10]。在病理性环境中,Src通路激活可伴随FGF2及其受体表达升高,增强促血管生成效应 [8]。此外,YAP既可通过上调FGFR增强细胞对FGF2的反应,也可在放疗后促进FGF2分泌,从而形成促存活和耐药环路 [4, 19]。
这种交叉调控进一步说明,FGF2并不是单一通路中的线性因子,而是多层级调控网络中的关键枢纽。也正因如此,针对FGF2的治疗策略通常难以通过单一环节实现理想效果,联合阻断多个节点往往更具潜力。
4. FGF2与相关疾病的病理生理学
4.1 FGF2在肿瘤发生发展及耐药性中的作用
FGF2在多种肿瘤的发生发展中具有重要促癌作用,其机制涉及细胞增殖、迁移、侵袭、血管生成以及多种治疗耐药。ER+乳腺癌中,FGF2可通过激活雌激素非依赖性ER信号促进肿瘤生长,并导致内分泌治疗耐药 [5, 17]。在KIT突变型黑色素瘤中,FGF2轴参与奈洛替尼耐药形成,而MEK抑制剂可部分逆转该过程 [18]。在非小细胞肺癌、乳腺癌和黑色素瘤中,FGF2/FGFR1高表达与TKI治疗后的DTP形成相关,提示FGFR信号代偿性激活是肿瘤获得耐药的重要机制之一。
除耐药外,FGF2还与肿瘤侵袭性密切相关。其全身水平在部分胃癌和食管癌患者中升高,可能反映更强的疾病进展倾向 [20]。在胶质瘤中,FGF2参与放疗抵抗形成,使其成为潜在的放疗增敏靶点 [19]。因此,FGF2不仅是肿瘤生长相关因子,更是影响治疗反应和临床结局的重要分子。
4.2 FGF2在神经系统疾病与视网膜病变中的作用
FGF2在神经系统中兼具促进增殖、营养支持和组织保护等多重作用。研究显示,YAP可通过增强神经干细胞对FGF2的响应来促进其增殖 [4]。此外,FGF2在帕金森病模型中表现出神经营养和神经保护作用,可支持多巴胺能神经元存活,并减轻MPP+或鱼藤酮诱导的神经损伤。
在视网膜病变中,FGF2既参与组织修复,也与病理性血管生成密切相关。缺氧条件下,YY1乳酸化可增强FGF2转录并促进血管新生 [7];PIK3IP1下调和miRNA-15a/16-1簇缺失也均可通过不同机制提升FGF2相关信号,推动异常血管生成 [8,9]。与此同时,A1-PEG则可通过提升FGF2表达,在抑制病理性新生血管形成的同时促进血管修复和视网膜功能改善 [10]。这表明FGF2在神经和视网膜疾病中具有明显的双重性,其作用方向高度依赖具体病理背景。
4.3 FGF2与骨骼、牙齿及结缔组织疾病
FGF2在骨骼形成、重塑和维持中发挥重要作用。其通过激活ERK MAP激酶增强Runx2稳定性和转录活性,从而促进成骨细胞分化和骨骼形态发生 [13]。在牙齿相关组织中,FGF2还能增强SCAP的成骨/成牙本质分化能力,这为牙髓-牙本质修复研究提供了重要依据 [11]。
另一方面,FGF2信号失衡也与骨代谢异常相关。例如,苯甲酸钠可通过抑制FGF2/p38/RUNX2通路导致成骨受阻和骨量流失 [12]。此外,FGF2在结缔组织修复和抗纤维化中也具有重要意义,其衍生短肽P5可在肺纤维化模型中减轻EMT和胶原沉积 [15]。因此,FGF2在骨骼、牙齿及结缔组织疾病中既是病理变化的重要调节因子,也是潜在干预靶点。
4.4 FGF2在炎症、感染、心血管及代谢性疾病中的作用
FGF2在炎症、感染、心血管和代谢性疾病中的作用同样复杂。在心血管损伤修复中,FGF2与VEGF等因子共同参与血管新生,可改善梗死心肌供血并促进功能恢复 [6]。在放射性肠损伤中,CXCR4/Akt/FGF2轴有助于促进肠道再生 [14]。在心肌梗死模型中,不同FGF2亚型对长期心功能和血管生成的影响并不一致,提示亚型差异可能影响疾病结局 [16]。
在炎症和感染相关疾病中,FGF2的作用也逐渐受到关注。蛋白质组学研究提示FGF2与牙周炎存在因果关联 [21]。在代谢相关病理性血管生成中,如糖尿病视网膜病变早期,FGF2与VEGF等因子共同参与病变进展。总体而言,FGF2在这些疾病中的作用并非单纯有益或有害,而是具有明显的环境依赖性和阶段依赖性。
5. FGF2靶向药物研究进展
目前靶向bFGF及相关信号通路的在研药物类型多样,包括Fc融合蛋白、小分子化药及基因疗法等,适应症覆盖糖尿病性黄斑水肿、肝细胞癌、胰腺癌及脱髓鞘疾病等多个领域,研发阶段从申请上市到临床1期不等,涉及荣昌生物、基亚生物科技及深圳未知君生物等多家机构。部分在研管线列举如下:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| 伊立芙普α | VEGF x bFGF | Fc融合蛋白 | 糖尿病性黄斑水肿 | 湿性年龄相关性黄斑变性 | 荣昌生物制药(烟台)股份有限公司 | 申请上市 |
| 磺酸化单磷酸甘露寡聚糖 | VEGF-A x aFGF x bFGF | 聚合物 | 肝细胞癌 | 基亚生物科技股份有限公司 | 临床3期 |
| AUP1602-C | M-CSF x bFGF | 工程菌 | 糖尿病足溃疡 | 糖尿病足 | 静脉曲张溃疡 | 褥疮 | 深圳未知君生物科技有限公司 | Aurealis Oy | Aurealis Therapeutics AG | 临床2期 |
| Curcumin C3 complex | NF-κB x bFGF x mTOR | 小分子化药 | 宫颈上皮内瘤样病变 | 人瘤病毒相关性宫颈癌 | 皮肤鳞状细胞癌 | Emory University | Lsu Health Shreveport | 临床2期 |
| Umedaptanib pegol | bFGF | 适配体 | 软骨发育不全 | 糖尿病性黄斑水肿 | Ribomic, Inc. | 临床2期 |
| Oleandrin | AP-1 x FLI1 x Na/K-ATPase x RPS6KB1 x bFGF x mTOR | 小分子化药 | 胰腺癌 | 肿瘤 | U.S. Army Medical Research Institute for Infectious Diseases | Nerium Biotechnology, Inc. | The University of Texas MD Anderson Cancer Center | 临床2期 |
| 绿原酸 | Akt x DNMT1 x LAG3 x SLC37A4 x TGF-β1 x bFGF | 小分子化药 | 复发性胶质瘤 | 晚期肺腺癌 | 晚期小细胞肺癌 | 晚期鳞状细胞肺癌 | 肾肿瘤 | 肝癌等 | 四川九章生物科技有限公司 | 湖南中医药大学 | Universiti Putra Malaysia | Brawijaya University | 临床2期 |
| 成纤维细胞生长因子2基因疗法(Id Pharma Co., Ltd.) | bFGF | 基因疗法 | 间歇性跛行 | 外周动脉疾病 | 围手术期缺血 | Kyushu University | Id Pharma Co., Ltd. | 临床2期 |
| rHIgM22 | PDGFRs x bFGF | 单克隆抗体 | 脱髓鞘疾病 | Mayo Clinic | 临床1期 |
(数据截止到2026年3月19日,来源于synapse)
6. FGF2研究工具
FGF2是一种具有广泛生物学功能的多效性生长因子,在细胞增殖、分化、迁移、血管生成和组织修复等方面发挥核心作用。其通过与FGFRs结合,激活MAPK/ERK、PI3K/AKT以及其他多条信号通路,形成复杂而精细的调控网络。与此同时,FGF2异常表达或信号失调又与多种疾病密切相关,尤其在肿瘤进展、治疗耐药、视网膜病变、神经系统疾病、骨代谢异常和纤维化等领域表现突出。CUSABIO提供FGF2重组蛋白、抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● FGF2 重组蛋白
Recombinant Bovine Fibroblast growth factor 2 (FGF2) (Active); CSB-EP008625BOe1
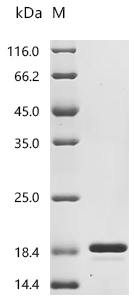
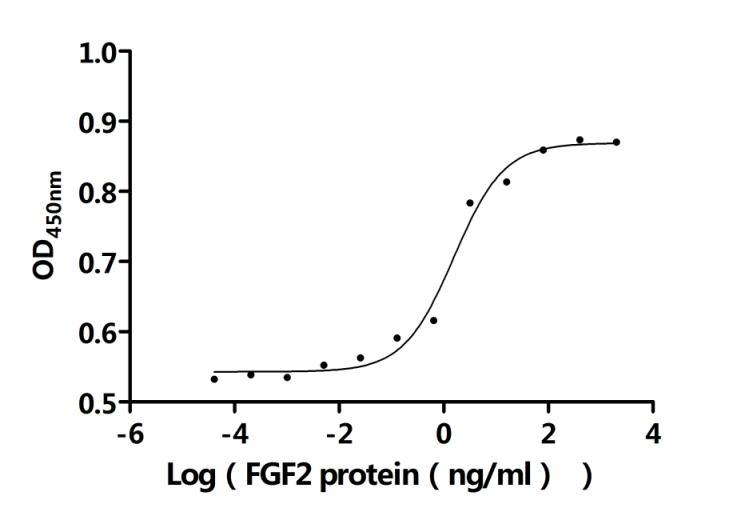
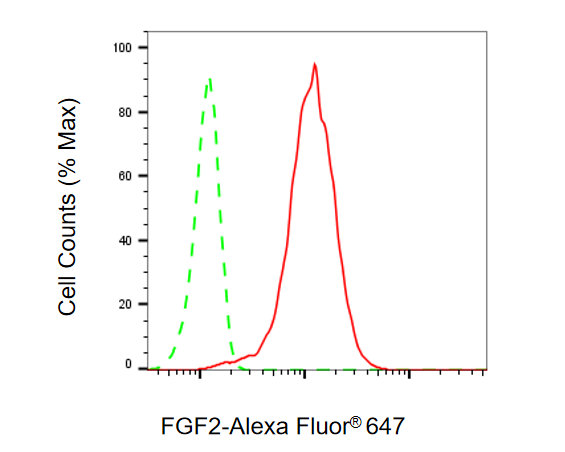
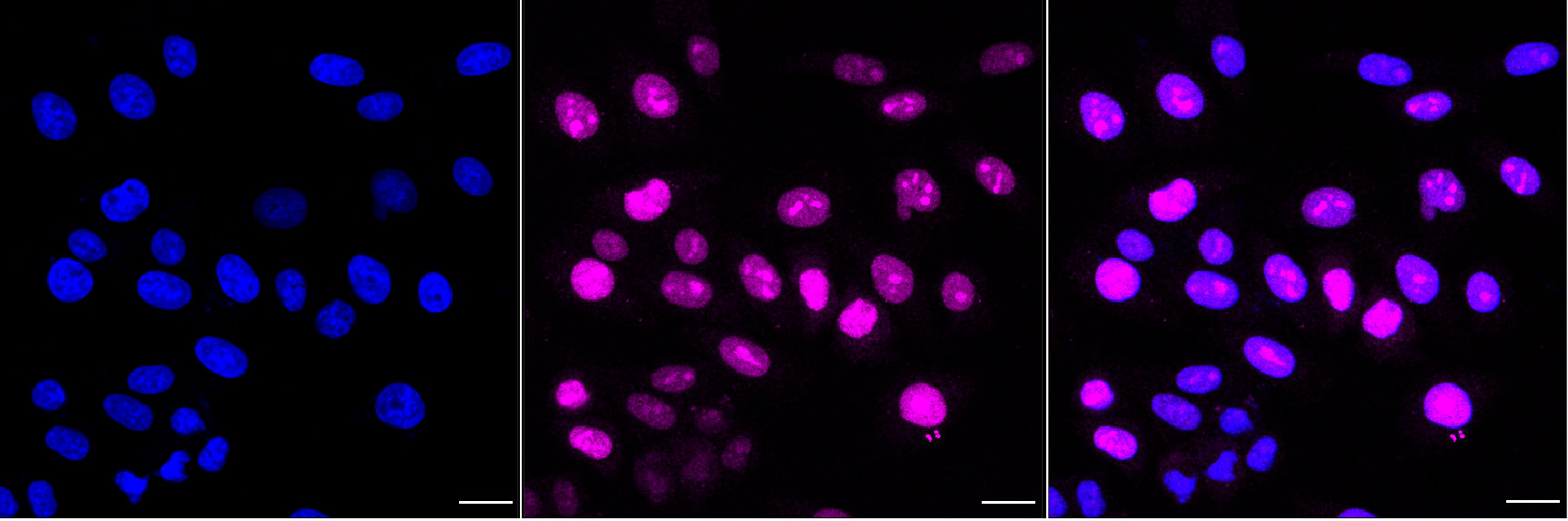
● FGF2 抗体
FGF2 Recombinant Monoclonal Antibody; CSB-RA927794A0HU
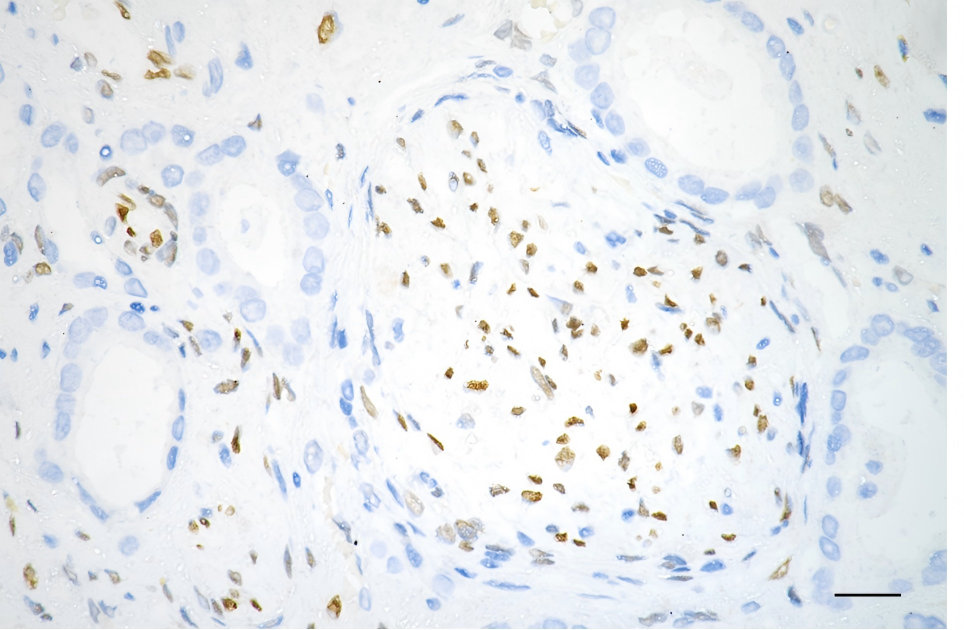
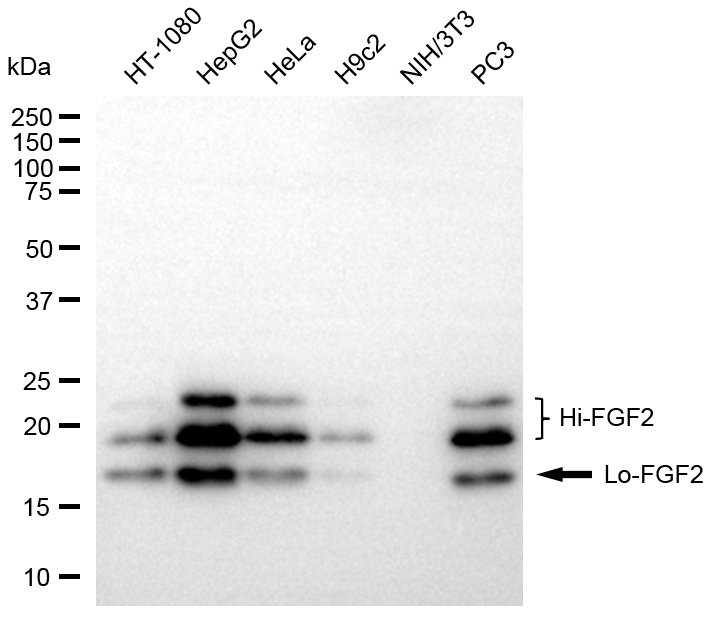
● FGF2 ELISA 试剂盒
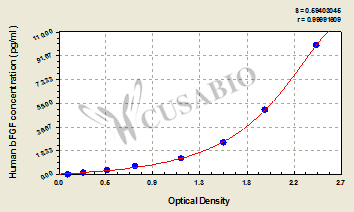
Human basic fibroblast growth factor,bFGF ELISA Kit
CSB-E08000h
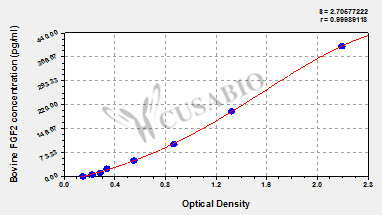
Bovine Heparin-binding growth factor 2(FGF2) ELISA kit
CSB-EL008625BO
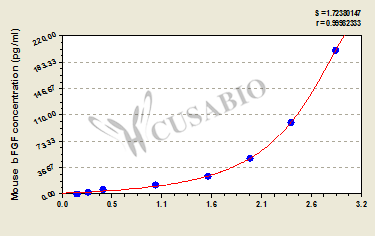
Mouse basic fibroblast growth factor,bFGF ELISA Kit
CSB-E08001m
[1] S. Sarabipour, K. Hristova. (2016). Mechanism of FGF receptor dimerization and activation.
[2] Yuga Okada, Akihiro Eguchi, Daisuke Kuroda, Kouhei Tsumoto, Ryosuke Ueki, Shinsuke Sando. (2025). Developing FGF2 Mutants with Selectively Reduced Heparan Sulfate Affinity to Explore Their Impact on FGFR1 Signaling.
[3] W. Chan, K. Howe, James M. Clegg, S. Guimond, D. Price, J. Turnbull, T. Pratt. (2015). 2-O Heparan Sulfate Sulfation by Hs2st Is Required for Erk/Mapk Signalling Activation at the Mid-Gestational Mouse Telencephalic Midline.
[4] Dasol Han, S. Lee, Mookwang Kwon, Hogyun Noh, J. H. Lee, Y. Yoon, J. Cho, K. Yoon. (2020). YAP enhances FGF2-dependent neural stem cell proliferation by induction of fibroblast growth factor receptor expression.
[5] Sebastián Giulianelli, Marina Riggio, Tomás Guillardoy, C. Pérez Piñero, M. Gorostiaga, G. Sequeira, Gabriela Pataccini, M. F. Abascal, Maria F. Toledo, B. Jacobsen, Ana C. L. Guerreiro, António S. Barros, V. Novaro, F. Monteiro, Francisco Amado, H. Gass, M. Abba, L. Helguero, C. Lanari. (2019). FGF2 induces breast cancer growth through ligand‑independent activation and recruitment of ERα and PRBΔ4 isoform to MYC regulatory sequences.
[6] Bin Zeng, Guosheng Lin, X. Ren, Yan Zhang, Honglei Chen. (2010). Over-expression of HO-1 on mesenchymal stem cells promotes angiogenesis and improves myocardial function in infarcted myocardium.
[7] Xiaotang Wang, W. Fan, Na Li, Yan Ma, Mudi Yao, Guoqing Wang, Siyuan He, Wanqian Li, J. Tan, Qingjun Lu, Shengping Hou. (2021). YY1 lactylation in microglia promotes angiogenesis through transcription activation-mediated upregulation of FGF2.
[8] P. Sun, Feifei Ma, Yang Xu, Chao Zhou, R. A. Stetler, K. Yin. (2021). Genetic deletion of endothelial microRNA-15a/16-1 promotes cerebral angiogenesis and neurological recovery in ischemic stroke through Src signaling pathway.
[9] Lushu Chen, Yuan Cao, Yaming Shen, Huan Li, Rong Ye, Jin Yao. (2023). Downregulation of PIK3IP1 in retinal microglia promotes retinal pathological neovascularization via PI3K-AKT pathway activation.
[10] A. Fouda, Zhimin Xu, J. Suwanpradid, M. Rojas, E. Shosha, Tahira Lemtalsi, C. Patel, Ji Xing, Sumbal Zaidi, W. Zhi, Brain K Stansfield, P. Cheng, S. Narayanan, R. Caldwell, R. Caldwell. (2022). Targeting proliferative retinopathy: Arginase 1 limits vitreoretinal neovascularization and promotes angiogenic repair.
[11] Zijie Wang, Chuying Chen, Liying Sun, Mei He, Ting Huang, Jiji Zheng, Jiayuan Wu. (2024). Fibroblast growth factor 2 promotes osteo/odontogenic differentiation in stem cells from the apical papilla by inhibiting PI3K/AKT pathway.
[12] Zhonghao Wang, Yexin Wang, Yu Tang, Xiaoyan Guo, Qize Gao, Yiming Shao, Jingxuan Wang, Ronghua Tian, Yingxu Shi. (2025). Sodium Benzoate Inhibits Osteoblast Differentiation and Accelerates Bone Loss by Regulating the FGF2/p38/RUNX2 Pathway.
[13] Ok-Jin Park, Hyun-Jung Kim, K. Woo, J. Baek, H. Ryoo. (2009). FGF2-activated ERK Mitogen-activated Protein Kinase Enhances Runx2 Acetylation and Stabilization.
[14] Yang Jiao, Jing Xu, Bingtan Song, Ailing Wu, L. Pan, Ying Xu, Fenghao Geng, Xiaoqian Li, Congzhao Zhao, Min Hong, Xuanyu Meng, Judong Luo, Peng Liu, Ming Li, Wei Zhu, Jianping Cao, Shuyu Zhang. (2022). Interferon regulatory factor 1‐triggered free ubiquitin protects the intestines against radiation‐induced injury via CXCR4/FGF2 signaling.
[15] Mengwei Wang, Yuanmeng Sun, Yanzhi Zhao, Xinyi Jiang, Teng Wang, Junye Xie, Xiuling Yu, Shujun Guo, Yibo Zhang, Xiaojia Chen, An Hong. (2025). An FGF2-Derived Short Peptide Attenuates Bleomycin-Induced Pulmonary Fibrosis by Inhibiting Collagen Deposition and Epithelial--Mesenchymal Transition via the FGFR/MAPK Signaling Pathway.
[16] R. Harris, A. Adeyemo, J. Redfield, Cha-hua Huang, Min Jiang, Xiaoping Ren, W. Jones, Jack Rubinstein, J. J. Schultz. (2016). Long‐term Biological Functions of Fibroblast Growth Factor‐2 (FGF2) in Mouse Hearts Following Myocardial Infarction.
[17] Josh W DiGiacomo, Inês Godet, Michael Trautmann-Rodriguez, Daniele M. Gilkes. (2020). Extracellular Matrix--Bound FGF2 Mediates Estrogen Receptor Signaling and Therapeutic Response in Breast Cancer.
[18] P. Têtu, J. Delyon, J. André, Coralie Reger de Moura, Malak Sabbah, G. Ghanem, M. Battistella, S. Mourah, C. Lebbé, N. Dumaz. (2020). FGF2 Induces Resistance to Nilotinib through MAPK Pathway Activation in KIT Mutated Melanoma.
[19] Yu Zhang, Yan Wang, Di Zhou, Kai Wang, Xu Wang, Xiang Wang, Yang Jiang, Min Zhao, Rutong Yu, Xiuping Zhou. (2021). Radiation-induced YAP activation confers glioma radioresistance via promoting FGF2 transcription and DNA damage repair.
[20] Iwona Bednarz-Misa, Paulina Fortuna, D. Diakowska, Natalia Jamrozik, M. Krzystek-Korpacka. (2020). Distinct Local and Systemic Molecular Signatures in the Esophageal and Gastric Cancers: Possible Therapy Targets and Biomarkers for Gastric Cancer.
[21] Z. Alayash, S. Baumeister, B. Holtfreter, Thomas Kocher, H. Baurecht, B. Ehmke, D. Hagenfeld, S. L. Reckelkamm, M. Nolde. (2025). Proteome-Guided Drug Target Discovery for Periodontitis.



