武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
从共受体到治疗靶点:CD4分子如何调控免疫、影响疾病
408 人阅读发布时间:2026-03-27 10:34
CD4是辅助性T细胞表面的关键分子,在适应性免疫应答中发挥核心作用。本文系统梳理了CD4的结构功能、CD4⁺ T细胞亚群分化及其调控机制,重点介绍了TCR、JAK/STAT、TGF-β/SMAD等信号通路在免疫调控中的作用和CD4在HIV/AIDS、自身免疫病、肿瘤等疾病中的研究进展,以及靶向CD4的药物开发现状。
1. CD4在免疫系统中的核心地位与研究价值
2. CD4的分子特性与基础功能
3. CD4+ T细胞生物学:亚群、分化与调控机制
4. 调控CD4+ T细胞功能的关键信号通路
5. CD4+ T细胞在疾病发生发展中的作用
6. CD4靶向药物最近研究进展
7. CD4研究工具
1. CD4在免疫系统中的核心地位与研究价值
CD4是适应性免疫系统中的关键跨膜糖蛋白,主要表达于辅助性T细胞(CD4+ T细胞)、单核细胞、巨噬细胞和树突状细胞表面。其中,在CD4+ T细胞上,CD4作为T细胞受体(TCR)的共受体,通过与主要组织相容性复合体II类(MHC-II)分子结合,协同介导T细胞活化,是适应性免疫应答启动与调节的重要枢纽。
CD4+ T细胞具有显著的功能多样性,可分化为Th1、Th2、Th17和Treg等多个亚群,在免疫辅助、炎症调控和免疫耐受维持中发挥不可替代的作用 [1]。近年来,随着成像技术、单细胞分析和计算模型的发展,研究者对CD4分子的认识不断深化。例如,超分辨成像研究揭示了CD4在静息T细胞质膜上的纳米尺度分布及其受棕榈酰化影响的特征 [2];肿瘤免疫微环境研究表明,对CD4+ T细胞的自动识别和分类有助于预后评估与治疗反应分析 [3];人工智能驱动的成像分析也显示出区分CD4和CD8细胞的潜力 [4]。
与此同时,针对CD4的药物开发也不断推进。以人源化抗CD4单克隆抗体Zanolimumab为例,其可通过抑制TCR信号转导、诱导Fc依赖性效应机制及下调细胞表面CD4表达等方式抑制CD4+ T细胞,目前正用于皮肤和淋巴结T细胞淋巴瘤相关研究 [5]。这些进展表明,CD4不仅是理解免疫调控机制的关键分子,也具有重要的疾病研究与药物开发价值。
2. CD4的分子特性与基础功能
2.1 CD4的结构与细胞表面表达
CD4分子通常为单链跨膜糖蛋白,由四个免疫球蛋白样胞外结构域(D1-D4)、一个跨膜区及较短的胞内区组成。其胞外D1和D2结构域主要参与与MHC II类分子的结合,而胞内区则与Lck酪氨酸激酶密切关联,从而参与TCR信号启动与调节。
除经典的CD4+ T细胞外,CD4还表达于巨噬细胞、树突状细胞和单核细胞等免疫细胞表面,因此其功能并不限于T细胞活化,也与抗原提呈、病毒感染及免疫微环境调控等过程密切相关。近年来,基于TIRF和SOFI的定量成像方法提高了对CD4膜表面纳米尺度分布的解析能力,进一步证实了棕榈酰化对CD4分布模式的重要影响 [2]。此外,人工智能辅助的无标记成像技术也提示,CD4作为细胞表面标志物在细胞识别与分类中具有较高应用潜力 [4]。
2.2 CD4作为TCR共受体的作用机制
在T细胞介导的免疫应答中,CD4的核心作用是协助TCR识别由抗原提呈细胞表面MHC II类分子呈递的抗原肽。CD4通过与MHC II结合增强TCR-pMHC复合物的稳定性,从而提升T细胞抗原识别的效率与特异性。
除稳定识别复合物外,CD4还可通过胞内区招募并调节p56lck活性。活化后的p56lck可磷酸化TCR复合体中CD3链的ITAM基序,进而启动T细胞早期信号级联反应。值得注意的是,针对CD4的抗体研究提示,CD4不仅参与激活,也与抑制性调控有关。研究显示,Zanolimumab可快速抑制早期TCR信号,同时激活CD4相关的p56lck,这提示其可能通过改变p56lck与TCR复合体的耦联状态,转而激活Dok-1、SHIP-1等抑制性信号分子,从而实现对T细胞功能的抑制 [5]。这说明,CD4不仅是简单的共受体,也是连接识别、激酶招募和信号调控的重要节点。
3. CD4+ T细胞生物学:亚群、分化与调控机制
3.1 CD4+ T细胞亚群及其功能多样性
CD4+ T细胞具有高度异质性,可根据转录因子表达和细胞因子分泌谱分化为不同亚群。经典亚群包括Th1、Th2、Th17和Treg:
- Th1细胞主要分泌IFN-γ,介导抗细胞内病原体和抗肿瘤免疫 [6]
- Th2细胞以IL-4、IL-5和IL-13为特征,主要参与抗寄生虫免疫和过敏反应
- Th17细胞分泌IL-17A和IL-17F,在抗细胞外病原体感染中发挥作用,但过度活化可促进自身免疫性炎症 [7]
- Treg细胞则通过Foxp3、IL-10和TGF-β维持免疫耐受并抑制过度免疫反应 [8]
除了经典Th亚群外,Tfh和CD4 CTL也是近年来受到高度关注的重要类型:
- Tfh细胞在B细胞活化、抗体亲和力成熟和生发center反应中具有关键作用,在慢性感染和慢性移植物抗宿主病中均表现出重要意义 [11-12]
- CD4 CTL则突破了传统"辅助性T细胞"的概念,具备穿孔素和颗粒酶介导的直接细胞毒性功能,可参与感染细胞或肿瘤细胞清除 [1]
- 此外,一些研究还识别出具有干细胞样特征的CD4+ T细胞亚群,其可持续补充效应细胞,在慢性炎症维持中发挥类似"疾病干细胞"的作用 [14]
3.2 CD4+ T细胞分化与可塑性的调控
CD4+ T细胞的分化受抗原强度、细胞因子环境和转录因子网络共同调控:
- 抗原亲和力与剂量是决定初始T细胞命运的重要早期信号 [15]
- 外源和内源细胞因子的种类、浓度及比例,则决定分化是呈现突变式还是渐进式变化 [16]
- 例如,IL-2可调节Foxp3 expression,从而影响诱导型Treg的形成 [17]
在细胞内调控层面,Bcl6、Maf、ThPOK、Runx3、Eomes等转录因子参与塑造不同CD4+ T细胞亚群的命运与功能 [13], [18-19]。这些因子相互拮抗或协同,使CD4+ T细胞能够根据感染、炎症或肿瘤等不同微环境进行动态重塑,从而体现出较强的可塑性。这种可塑性既是免疫应答灵活性的基础,也增加了疾病研究和治疗干预的复杂性。
3.3 CD4+ T细胞的增殖、存活与代谢重编程
CD4+ T细胞在活化后需要经历快速增殖,并通过代谢重编程满足效应功能需求。其增殖与存活受IL-7等细胞因子支持,同时也受代谢途径、线粒体状态及细胞内能量平衡调控 [27]。不同亚群在代谢模式上存在差异,例如炎症性效应T细胞通常偏向糖酵解,而调节性T细胞则更多依赖氧化代谢。代谢状态不仅影响细胞生存,也决定其分化方向和功能输出,因此代谢调控已成为理解CD4+ T细胞稳态与疾病关联的重要切入点。
4. 调控CD4+ T细胞功能的关键信号通路
4.1 TCR近端信号与钙调神经磷酸酶-NFAT通路
TCR近端信号是CD4+ T细胞活化的起点。CD4通过协助MHC II识别并招募Lck,促进CD3链ITAM磷酸化,进而激活ZAP-70等下游信号分子。随后,钙离子信号与钙调神经磷酸酶-NFAT通路被激活,驱动效应基因表达并调节T细胞分化与功能输出。该通路对T细胞早期命运决定具有基础性作用。
4.2 JAK/STAT信号通路
JAK/STAT通路是细胞因子调控CD4+ T细胞分化的核心通路之一。不同细胞因子可通过激活不同STAT成员,促进Th1、Th17或Treg等亚群形成。相关研究表明,某些天然产物或免疫调节因子可通过抑制STAT1、STAT3 or STAT5活性,改变Th1/Th17与Treg之间的平衡,从而在炎症和自身免疫性疾病中发挥治疗潜力 [9-10]。
4.3 TGF-β/SMAD与Notch信号通路
TGF-β/SMAD通路在Treg形成、免疫耐受维持及炎症调控中具有重要地位;Notch信号则在T细胞发育、分化和功能塑造中发挥辅助调节作用。这两类通路并非孤立存在,而是与JAK/STAT等通路交互作用,共同参与CD4+ T细胞命运调控。
4.4 cGAS/STING通路与免疫代谢关联
cGAS/STING通路最初主要被认为参与胞质DNA感知与先天免疫激活,但近年来研究提示,该通路同样会影响肿瘤免疫环境和T细胞功能状态。代谢应激、线粒体DNA释放等事件可激活该通路,进而诱导I型干扰素反应,并影响肿瘤浸润免疫细胞组成及CD4+ T细胞功能 [29]。
4.5 cAMP及其他相关通路
cAMP信号在CD4+ T细胞免疫调控中同样具有重要意义。相关研究显示,Forskolin等cAMP通路激活剂能够调节自身免疫性炎症中的CD4+ T cell反应,并与中枢神经系统炎症缓解相关 [32]。此外,多条信号通路之间存在广泛串扰,共同决定CD4+ T cell在不同疾病背景下的功能状态 [28]。
5. CD4+ T细胞在疾病发生发展中的作用
5.1 HIV/AIDS发病机制
HIV感染最典型地体现了CD4在疾病中的核心地位。CD4既是免疫功能评估的重要指标,也是HIV入侵宿主细胞的重要相关分子。CD4+ T cell数量下降直接反映免疫系统受损程度,而病毒载量、宿主个体差异及免疫重建能力等因素共同决定疾病进展速度。因此,CD4计数长期以来一直是HIV感染管理与疗效评估的重要参数。
5.2 自身免疫性疾病与炎症
在类风湿关节炎、系统性红斑狼疮、实验性自身免疫性脑脊髓炎等疾病中,CD4+ T cell亚群失衡是关键病理机制之一。尤其是Th17/Treg失衡,常与慢性炎症放大和组织损伤相关 [9-10]。多种代谢干预、细胞疗法及信号通路调节策略,均显示出通过重塑CD4+ T cell功能来缓解疾病的潜力 [26], [30]。
5.3 癌症免疫与免疫治疗
在肿瘤免疫中,CD4+ T cell既能辅助CD8+ T cell发挥杀伤作用,也可独立介导抗肿瘤免疫,甚至作为疗效预测生物标志物。这说明,CD4+ T cell不仅是肿瘤免疫中的"辅助者",在一定条件下也可能是关键"执行者"。
5.4 其他感染性疾病
除HIV外,CD4+ T cell在流感等急慢性感染中同样发挥重要作用。特别是CD4 CTL的发现,提示CD4+ T cell在抗病毒过程中不仅负责调控,也可直接参与感染细胞清除 [1]。这拓展了对CD4+ T cell在感染免疫中功能边界的理解。
6. CD4靶向药物最近研究进展
目前,靶向CD4的药物类型多样,涵盖单抗、双抗、CAR-T及小分子药物;在研适应症以HIV感染为主,并拓展至特应性皮炎、肿瘤等领域;研发阶段覆盖已上市品种至临床早期,部分在研管线列举如下。
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| 艾巴利珠单抗 | CD4 x Viral fusion proteins | 双特异性抗体 | HIV感染 | Theratechnologies, Inc. | 批准上市 |
| Semzuvolimab | CD4 | 单克隆抗体 | HIV感染 | 聯生藥大中華控股有限公司 | 联合生物制药股份有限公司 | 联亚药业股份有限公司 | 临床3期 |
| Mosedipimod | CD4 x CD8 | 小分子化药 | 中度特应性皮炎 | 重度特应性皮炎 | 代谢功能障碍相关脂肪性肝炎 | ENZYCHEM LIFESCIENCES Corp. | 临床2期 |
| Iotivibart | CD4 x HIV envelope protein gp120 | 单克隆抗体 | HIV感染 | ViiV Healthcare UK Ltd. | ViiV Healthcare Ltd. | 临床2期 |
| TMB-365 | CD4 | 单克隆抗体 | HIV感染 | 中裕新药股份有限公司 | 临床2期 |
| IB-MS | CD4 x CD8 | 小分子化药 | 多发性硬化症 | INNOBIOSCIENCE LLC | 临床2期 |
| CD4 CAR T cell therapy (iCell Gene Therapeutics) | CD4 | 自体CAR-T | 慢性粒单核细胞白血病 | T细胞白血病 | T细胞淋巴瘤 | iCell Gene Therapeutics, Inc. | 临床1期 |
| IT-1208(Kyowa Hakko Kirin Pharma, Inc.) | CD4 | 单克隆抗体 | 肿瘤 | IDAC Theranostics, Inc. | Ono Pharmaceutical Co., Ltd. | Kyowa Kirin Co., Ltd. | 临床1期 |
| Autologous CD4 CAR T-cells(Indiana University) | CD4 | 自体CAR-T | 难治性急性髓细胞白血病 | 复发性急性髓细胞白血病 | iCell Gene Therapeutics, Inc. | 临床1期 |
| VRCHIVMAB0115-00-AB | CD4 | 单克隆抗体 | HIV感染 | National Institute of Allergy & Infectious Diseases | 临床1期 |
| BG-8962 | CD4 | 生物药 | HIV感染 | National Institute of Allergy & Infectious Diseases | 临床1期 |
| LM49 | CD4 | 小分子化药 | 糖尿病肾病 | 山西医科大学 | 山西中医药大学 | 临床1期 |
(数据截止到2026年3月16日,来源于synapse)
7. CD4研究工具
CD4不仅是辅助性T细胞的重要表面分子,更是连接抗原识别、信号转导、细胞分化和疾病进程的关键枢纽。围绕CD4及CD4+ T cell的研究,已经从传统的"辅助功能"拓展到细胞毒性、代谢调控、组织微环境适应和疾病持续化机制等多个层面。华美生物提供CD4重组蛋白、抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD4 重组蛋白
Recombinant Human T-cell surface glycoprotein CD4 (CD4), partial (Active); CSB-MP004935HU1
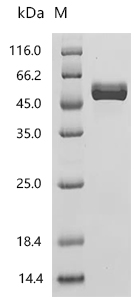
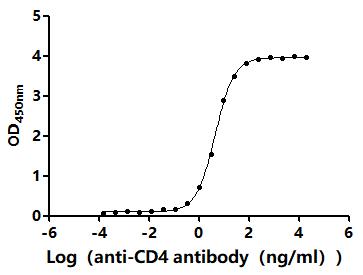
Recombinant Macaca mulatta T-cell surface glycoprotein CD4 (CD4), partial (Active); CSB-MP6740MOW
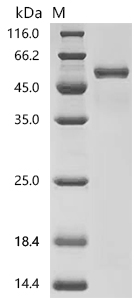
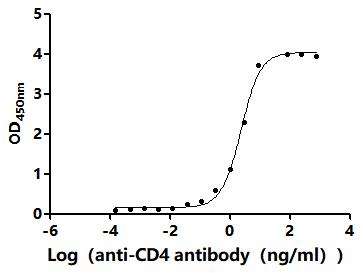
● CD4 抗体
CD4 Recombinant Monoclonal Antibody; CSB-RA004935A0HU
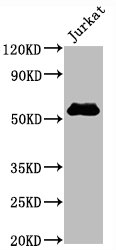
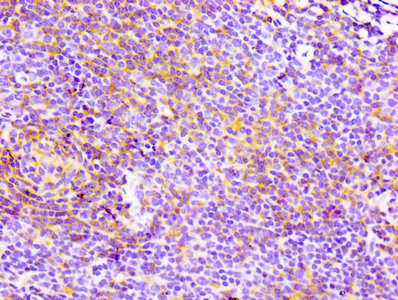
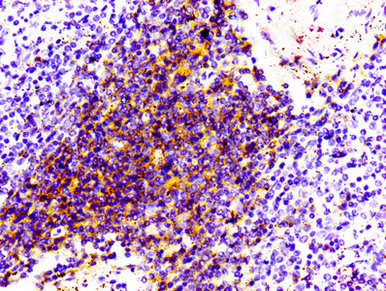
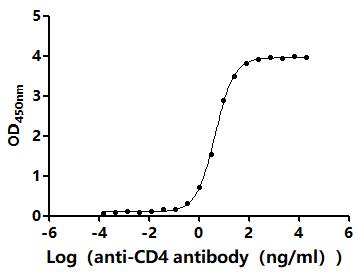
CD4 Recombinant Monoclonal Antibody; CSB-RA004935MA3HU
● CD4 ELISA 试剂盒
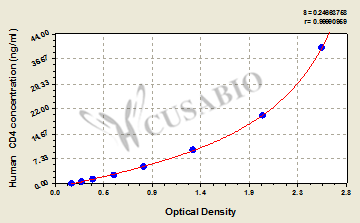
Human cluster of differentiation 4,CD4 ELISA Kit
CSB-E08956h
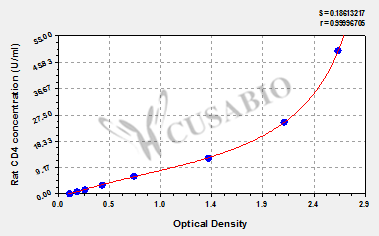
Rat cluster of differentiation 4,CD4 ELISA Kit
CSB-E12928r
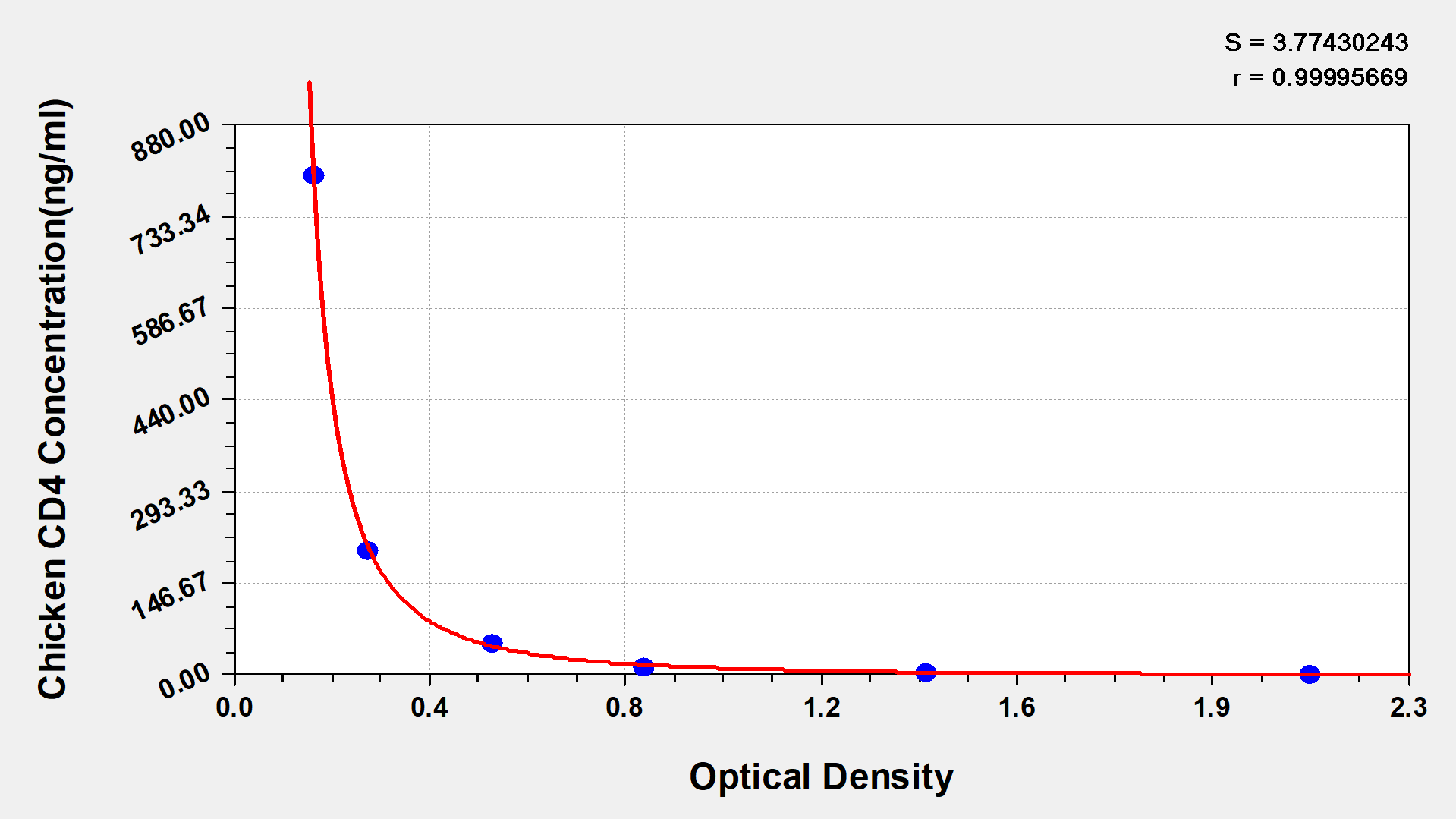
Chicken Cluster of Differentiation 4(CD4) ELISA Kit
CSB-E13114C
[1] Deborah M. Brown, Anna T. Lampe, Aspen M. Workman. (2016). The Differentiation and Protective Function of Cytolytic CD4 T Cells in Influenza Infection.
[2] Tomas Lukes, Daniela Glatzova, Zuzana Kvicalova, Florian Levet, Ales Benda, Tomas Brdicka, Theo Lasser, Marek Cebecauer. (2017). Quantifying protein densities on cell membranes using super-resolution optical fluctuation imaging.
[3] Mikaël Simard, Zhuoyan Shen, Konstantin Bräutigam, Rasha Abu-Eid, Maria A. Hawkins, Charles-Antoine Collins-Fekete. (2024). Immunocto: a massive immune cell database auto-generated for histopathology.
[4] Xin Shu, Sameera Sansre, Di Jin, Xiangxiang Zeng, Kai-Yu Tong, Rishikesh Pandey, Renjie Zhou. (2020). Artificial Intelligence Enabled Reagent-free Imaging Hematology Analyzer.
[5] D. Rider, C. Havenith, R. De Ridder, J. Schuurman, C. Favre, J. Cooper, S. Walker, O. Baadsgaard, S. Marschner, Jan G J vandeWinkel, J. Cambier, P. Parren, D. Alexander. (2007). A human CD4 monoclonal antibody for the treatment of T-cell lymphoma combines inhibition of T-cell signaling by a dual mechanism with potent Fc-dependent effector activity.
[6] J. T. Ulrich-Lewis, K. Draves, Kelsey Roe, M. O'Connor, E. Clark, D. Fuller. (2022). STING Is Required in Conventional Dendritic Cells for DNA Vaccine Induction of Type I T Helper Cell- Dependent Antibody Responses.
[7] Constance Renault, N. Veyrenche, F. Mennechet, A. Bedin, J. Routy, P. Van de Perre, J. Reynes, E. Tuaillon. (2022). Th17 CD4+ T-Cell as a Preferential Target for HIV Reservoirs.
[8] Rong Wang, Keliang Huang. (2020). CCL11 increases the proportion of CD4+CD25+Foxp3+ Treg cells and the production of IL-2 and TGF-β by CD4+ T cells via the STAT5 signaling pathway.
[9] Jiaxu Qin, Xiangwei Zheng, Yancheng He, Yang Hong, Shuang Liang, X. Fang. (2022). The regulation of T helper cell polarization by the diterpenoid fraction of Rhododendron molle based on the JAK/STAT signaling pathway.
[10] Fanping Wang, Yonghui Yang, Zhixin Li, Yan Wang, Zhenchao Zhang, Wei Zhang, Yonghui Mu, Jing-ke Yang, Lili Yu, Mingyong Wang. (2022). Mannan-Binding Lectin Regulates the Th17/Treg Axis Through JAK/STAT and TGF-β/SMAD Signaling Against Candida albicans Infection.
[11] R. Deng, C. Hurtz, Qingxiao Song, Chanyu Yue, G. Xiao, Hua Yu, Xiwei Wu, M. Muschen, S. Forman, P. Martin, D. Zeng. (2017). Extrafollicular CD4+ T-B interactions are sufficient for inducing autoimmune-like chronic graft-versus-host disease.
[12] Laura M. Fahey, Elizabeth B. Wilson, Heidi J. Elsaesser, Chris Fistonich, D. McGavern, D. Brooks. (2011). Viral persistence redirects CD4 T cell differentiation toward T follicular helper cells.
[13] A. Dejean, Emeline Joulia, T. Walzer. (2018). The role of Eomes in human CD4 T cell differentiation: A question of context.
[14] Yuki Sato, Abhinav Jain, Shozo Ohtsuki, Hirohisa Okuyama, Ines Sturmlechner, Yoshinori Takashima, Kevin-Phu C. Le, Melanie C. Bois, Gerald J. Berry, K. Warrington, J. Goronzy, C. Weyand. (2023). Stem-like CD4+ T cells in perivascular tertiary lymphoid structures sustain autoimmune vasculitis.
[15] S. Keck, M. Schmaler, S. Ganter, Lena Wyss, Susanne G. Oberle, E. Huseby, D. Zehn, C. King. (2014). Antigen affinity and antigen dose exert distinct influences on CD4 T-cell differentiation.
[16] M. Martínez-Sánchez, L. Huerta, E. Álvarez-Buylla, Carlos Villarreal Luján. (2018). Role of Cytokine Combinations on CD4+ T Cell Differentiation, Partial Polarization, and Plasticity: Continuous Network Modeling Approach.
[17] E. Zorn, E. Nelson, M. Mohseni, F. Porcheray, Haesook T. Kim, Despina Litsa, R. Bellucci, E. Raderschall, C. Canning, R. Soiffer, D. Frank, J. Ritz. (2006). IL-2 regulates FOXP3 expression in human CD4+CD25+ regulatory T cells through a STAT-dependent mechanism and induces the expansion of these cells in vivo.
[18] M. Kroenke, D. Eto, M. Locci, Michael Cho, T. Davidson, E. Haddad, S. Crotty. (2012). Bcl6 and Maf Cooperate To Instruct Human Follicular Helper CD4 T Cell Differentiation.
[19] Megan A. Luckey, M. Kimura, A. Waickman, L. Feigenbaum, A. Singer, Jung-Hyun Park. (2014). The transcription factor ThPOK suppresses Runx3 and imposes CD4+ lineage fate by inducing the SOCS suppressors of cytokine signaling.
[20] Qingtian Li, Jia Zou, Mingjun Wang, Xilai Ding, I. Chepelev, Xikun Zhou, Wei Zhao, Gang Wei, J. Cui, K. Zhao, Helen Y Wang, Rong-Fu Wang. (2014). Critical role of histone demethylase Jmjd3 in the regulation of CD4+ T-cell differentiation.
[21] Y. Shu, Qinghua Hu, H. Long, Christopher Chang, Q. Lu, R. Xiao. (2017). Epigenetic Variability of CD4+CD25+ Tregs Contributes to the Pathogenesis of Autoimmune Diseases.
[22] Sarah A. LaMere, Ryan C. Thompson, Xiangzhi Meng, H. Komori, Adam M. Mark, D. Salomon. (2017). H3K27 Methylation Dynamics during CD4 T Cell Activation: Regulation of JAK/STAT and IL12RB2 Expression by JMJD3.
[23] M. Martínez-Sánchez, L. Mendoza, C. Villarreal, E. Álvarez-Buylla. (2015). A Minimal Regulatory Network of Extrinsic and Intrinsic Factors Recovers Observed Patterns of CD4+ T Cell Differentiation and Plasticity.
[24] B. L. Puniya, R. G. Todd, Akram Mohammed, Deborah M. Brown, Matteo Barberis, T. Helikar. (2018). A Mechanistic Computational Model Reveals That Plasticity of CD4+ T Cell Differentiation Is a Function of Cytokine Composition and Dosage.
[25] V. Proserpio, A. Piccolo, Liora Haim-Vilmovsky, G. Kar, T. Lönnberg, Valentine Svensson, J. Pramanik, K. Natarajan, Weichao Zhai, Xiuwei Zhang, G. Donati, M. Kayikci, J. Kotar, A. McKenzie, Ruddy Montandon, O. Billker, S. Woodhouse, P. Cicuta, M. Nicodemi, S. Teichmann. (2016). Single-cell analysis of CD4+ T-cell differentiation reveals three major cell states and progressive acceleration of proliferation.
[26] S. Tullius, H. Biefer, Suyan Li, A. Trachtenberg, K. Edtinger, M. Quante, Felix Krenzien, H. Uehara, Xiaoyong Yang, H. Kissick, W. Kuo, I. Ghiran, M. A. de la Fuente, M. Arredouani, Virginia Camacho, J. Tigges, Vasilis Toxavidis, Rachid El Fatimy, Brian D. Smith, A. Vasudevan, A. Elkhal. (2014). NAD+ protects against EAE by regulating CD4+ T-cell differentiation.
[27] Nizar Chetoui, M. Boisvert, S. Gendron, F. Aoudjit. (2010). Interleukin‐7 promotes the survival of human CD4+ effector/memory T cells by up‐regulating Bcl‐2 proteins and activating the JAK/STAT signalling pathway.
[28] M. S. Alam, Y. Maekawa, A. Kitamura, K. Tanigaki, T. Yoshimoto, K. Kishihara, K. Yasutomo. (2010). Notch signaling drives IL-22 secretion in CD4+ T cells by stimulating the aryl hydrocarbon receptor.
[29] Shengpan Wu, Baojun Wang, Hong-zhao Li, Hanfeng Wang, Songliang Du, Xing Huang, Yang Fan, Yu Gao, L. Gu, Qingbo Huang, Jianjun Chen, Xu Zhang, Yan Huang, Xin Ma. (2024). Targeting STING elicits GSDMD-dependent pyroptosis and boosts anti-tumor immunity in renal cell carcinoma.
[30] Dongmei Li, Idalia Cruz, Yahui Feng, Maha Moussa, Jie Cheng, Digvijay Patil, Alexander Kroemer, Joseph A. Bellanti. (2025). Divergent Immunomodulatory Roles of Fungal DNA in Shaping Treg and Inflammatory Responses.
[31] C. Elsner, Aparna Ponnurangam, J. Kazmierski, T. Zillinger, Jenny Jansen, D. Todt, K. Döhner, Shuting Xu, A. Ducroux, Nils Kriedemann, Angelina Malassa, P. Larsen, G. Hartmann, W. Barchet, E. Steinmann, U. Kalinke, B. Sodeik, C. Goffinet. (2020). Absence of cGAS-mediated type I IFN responses in HIV-1--infected T cells.
[32] Tatyana Veremeyko, Amanda W. Y. Yung, M. Dukhinova, Inna S. Kuznetsova, I. Pomytkin, A. Lyundup, T. Strekalova, N. Barteneva, E. Ponomarev. (2018). Cyclic AMP Pathway Suppress Autoimmune Neuroinflammation by Inhibiting Functions of Encephalitogenic CD4 T Cells and Enhancing M2 Macrophage Polarization at the Site of Inflammation.



