武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
CD33:从白血病靶点到阿尔茨海默病关键分子,这个免疫"刹车"如何影响多种疾病?
595 人阅读发布时间:2026-03-27 10:36
CD33(Siglec-3)是Siglec家族的重要成员之一,主要表达于单核细胞、巨噬细胞和树突状细胞等髓系细胞表面。作为一种抑制性免疫受体,CD33通过胞内免疫受体酪氨酸抑制基序(ITIM)介导信号转导,在调节免疫稳态和炎症反应中发挥重要作用。近年来研究表明,CD33不仅在急性髓系白血病(AML)中作为重要靶向抗原,还在阿尔茨海默病(AD)、慢性病毒感染及肿瘤免疫微环境调控中发挥关键作用。特别是在神经系统中,CD33通过调控小胶质细胞吞噬功能影响β-淀粉样蛋白的清除能力,从而参与神经退行性疾病的发生发展。随着免疫治疗及基因组学研究的不断推进,CD33逐渐成为免疫调控研究和疾病靶向治疗的重要分子。本文综述了CD33的分子特征、主要信号通路及其在多种疾病中的作用,以期为急性髓系白血病、阿尔茨海默病等疾病的机制研究及靶向治疗策略开发提供参考。
1. CD33在免疫调控中的研究背景:从Siglec家族到疾病靶点
2. CD33的分子生物学特征:结构、功能与剪接变异
3. CD33相关信号通路:ITIM介导的免疫调控机制
4. CD33相关疾病:从血液肿瘤到神经退行性疾病
5. CD33靶点药物最近研究进展:从ADC到CAR-T的多平台治疗策略
6. CD33相关研究工具:重组蛋白、抗体与ELISA试剂盒
1. CD33在免疫调控中的研究背景:从Siglec家族到疾病靶点
CD33(Sialic acid-binding immunoglobulin-like lectin-3,Siglec-3)属于Siglec家族成员,该家族蛋白能够识别唾液酸修饰的糖链结构,在免疫系统中发挥重要的负调控作用 [1,2]。CD33主要表达于髓系细胞,包括单核细胞、巨噬细胞、树突状细胞及髓系祖细胞等,在调节先天免疫反应和维持免疫稳态中具有重要意义。
CD33的胞内结构域含有典型的免疫受体酪氨酸抑制基序(ITIM)。当CD33与其配体结合后,该结构域发生磷酸化并招募含SH2结构域的磷酸酶,例如SHP-1和SHP-2,从而抑制多种细胞信号通路的激活 [3]。这一抑制性信号机制使CD33成为髓系细胞免疫反应的重要调节因子。
近年来,随着免疫学、神经生物学以及肿瘤研究的发展,CD33在多种疾病中的作用逐渐受到关注。研究发现,在急性髓系白血病(AML)中约80%--90%的白血病细胞表达CD33,因此该分子成为重要的治疗靶点 [4]。同时,全基因组关联研究表明CD33基因多态性与阿尔茨海默病风险显著相关,其作用机制与小胶质细胞功能调控密切相关 [5]。此外,在慢性病毒感染和肿瘤免疫微环境中,CD33也参与调控髓系细胞的免疫抑制功能。因此,系统研究CD33的信号机制及其疾病相关性,对于理解免疫调控网络及开发新的治疗策略具有重要意义。
2. CD33的分子生物学特征:结构、功能与剪接变异
CD33是一种I型跨膜糖蛋白,其结构主要由胞外区、跨膜区和胞内区组成。胞外区包含两个免疫球蛋白样结构域,即远端IgV结构域和近膜IgC2结构域。其中IgV结构域能够识别唾液酸化糖链配体,是CD33发挥配体识别功能的关键结构。跨膜区则将CD33固定在细胞膜上,并维持其空间构象稳定。
CD33的胞内结构域含有保守的ITIM序列。当CD33与配体结合并被激活后,该序列中的酪氨酸残基发生磷酸化,随后招募SHP-1、SHP-2等磷酸酶,从而抑制多种细胞信号通路的激活 [3]。这种抑制性信号机制在免疫系统中具有重要意义,可防止过度炎症反应并维持免疫平衡。
在转录后调控层面,CD33基因还存在多种剪接异构体。其中最常见的是全长CD33-FL和缺失外显子2的CD33-Δ2形式。由于外显子2编码IgV结构域,其缺失会导致CD33无法有效结合唾液酸配体,从而改变受体功能。研究表明,与阿尔茨海默病保护相关的遗传变异能够促进CD33-Δ2的表达,从而降低功能性CD33水平并增强小胶质细胞吞噬能力 [5]。
CD33主要表达于髓系细胞,其表达水平在造血分化过程中呈动态变化。早期髓系祖细胞表达水平较高,而在成熟粒细胞中表达相对较低。这种表达模式反映了CD33在髓系细胞分化及免疫调控中的重要作用。
3. CD33相关信号通路:ITIM介导的免疫调控机制
3.1 CD33的ITIM介导抑制性信号通路
CD33最经典的信号转导机制是通过胞内ITIM结构域介导的抑制性信号。当CD33识别细胞表面的唾液酸化配体后,其胞内ITIM序列被Src家族激酶磷酸化。随后,含SH2结构域的蛋白质磷酸酶SHP-1或SHP-2被招募至该结构域,并通过去磷酸化作用抑制多种下游信号分子的活化 [3]。这种机制能够降低免疫细胞的激活程度,从而避免过度炎症反应。
在髓系细胞中,该信号通路可抑制多种炎症相关信号分子,例如Src激酶、MAPK通路以及NF-κB信号通路。通过这种方式,CD33能够调节巨噬细胞和树突状细胞的炎症反应水平,从而维持免疫系统的稳态。
3.2 CD33与小胶质细胞信号调控:阿尔茨海默病中的关键机制
在中枢神经系统中,CD33主要表达于小胶质细胞。小胶质细胞是脑内主要的免疫细胞,负责清除病原体及异常蛋白质。研究表明,CD33在小胶质细胞中主要发挥抑制性调控作用。当CD33表达升高时,小胶质细胞的吞噬活性明显下降,从而降低其清除β-淀粉样蛋白的能力。
在这一过程中,CD33与TREM2信号通路之间存在功能拮抗关系。TREM2能够促进小胶质细胞活化并增强吞噬功能,而CD33则通过抑制信号转导降低细胞活性。当CD33表达增加或信号增强时,小胶质细胞吞噬功能受到抑制,从而促进β-淀粉样蛋白沉积并加速神经退行性病变的进展。
3.3 CD33在肿瘤免疫微环境中的信号作用:髓源性抑制细胞的功能调控
近年来研究表明,CD33还在肿瘤免疫微环境中发挥重要作用。肿瘤组织中常富集大量髓源性抑制细胞(MDSC),这些细胞通过抑制T细胞活性促进肿瘤免疫逃逸。MDSC通常高表达CD33,其信号通路能够增强免疫抑制功能并抑制抗肿瘤免疫反应。
CD33信号的激活可调节多种免疫调控因子的表达,例如抑制性细胞因子和免疫检查点分子,从而进一步强化肿瘤免疫抑制环境。因此,CD33被认为是调控肿瘤免疫微环境的重要分子之一。
4. CD33相关疾病:从血液肿瘤到神经退行性疾病
4.1 急性髓系白血病(AML):CD33作为重要治疗靶点
急性髓系白血病是CD33研究最深入的疾病之一。AML是一类来源于髓系祖细胞的恶性血液肿瘤,其特征是异常白血病细胞在骨髓和外周血中大量增殖。研究表明,绝大多数AML患者的白血病细胞表面均表达CD33分子 [4]。这一特征使CD33成为AML诊断、分型以及靶向治疗的重要分子标志物。
在AML的发生过程中,CD33不仅作为表面抗原存在,还可能参与调控白血病细胞的增殖与分化。通过靶向CD33的抗体或免疫治疗手段,可以将细胞毒性药物选择性递送至白血病细胞,从而提高治疗效果。然而,由于正常髓系细胞同样表达CD33,这也可能导致骨髓抑制等副作用。
4.2 阿尔茨海默病(AD):CD33基因多态性与疾病风险
阿尔茨海默病是一种常见的神经退行性疾病,其主要病理特征包括β-淀粉样蛋白沉积和神经元退行性变。近年来的基因组学研究表明,CD33是与晚发型阿尔茨海默病相关的重要风险基因之一 [5]。
在神经系统中,CD33主要表达于小胶质细胞。研究发现,CD33能够抑制小胶质细胞对β1-淀粉样蛋白的吞噬能力,从而影响其清除效率。当CD33表达水平升高时,小胶质细胞吞噬功能降低,β-淀粉样蛋白沉积增加,从而促进神经退行性病变的发展。
此外,CD33基因的剪接变异也与疾病风险密切相关。一些遗传变异能够促进CD33-Δ2形式的表达,从而减少功能性CD33的产生并增强小胶质细胞清除能力,这被认为是其对阿尔茨海默病产生保护作用的重要机制。
4.3 慢性病毒感染:CD33在免疫调控中的作用
在慢性乙型肝炎等病毒感染性疾病中,CD33同样参与免疫调控过程。研究发现,CD33能够抑制树突状细胞的抗原呈递功能并降低T细胞活化水平,从而促进病毒持续感染。阻断CD33信号可以在一定程度上恢复免疫细胞活性并增强抗病毒免疫反应。
4.4 肿瘤免疫调控:CD33与髓源性抑制细胞的协同作用
在多种实体瘤中,CD33还参与肿瘤免疫微环境的形成。肿瘤组织中常富集髓源性抑制细胞,这些细胞通过分泌免疫抑制因子以及抑制T细胞功能来促进肿瘤生长。由于这些细胞通常高表达CD33,因此该分子被认为是调控肿瘤免疫抑制的重要靶点。
5. CD33靶点药物最近研究进展:从ADC到CAR-T的多平台治疗策略
目前,靶向CD33的药物研发已进入一个多元化、平台化的高速发展阶段。该靶点被证实在急性髓系白血病(AML)及其相关亚型(如难治/复发性急性髓细胞白血病、骨髓增生异常综合征等)的治疗中具有核心价值。从技术路径看,该领域已不再局限于传统的抗体偶联药物(ADC),而是全面布局了CAR-T、CAR-NK、双特异性抗体、DARPin、免疫刺激抗体偶联物(ISAC)及定向降解抗体等新一代治疗模式。研发策略也呈现出从单一靶点向双靶点甚至多靶点(如CD33联合CD123、CLL-1等)协同攻击的演进趋势,旨在提升治疗效果并克服肿瘤异质性导致的耐药。尽管已有药物获批上市,但绝大多数在研管线仍集中于临床1期及2期阶段。这表明CD33作为一个经典靶点,当前正经历着一轮以技术创新为核心驱动力的临床再开发热潮,未来有望通过更精准、高效的免疫治疗和基因修饰细胞疗法,进一步改善血液恶性肿瘤患者的临床预后。部分在研管线列举如下:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| 吉妥珠单抗 | CD33 x DNA | ADC | CD33阳性急性髓性白血病 | 急性髓性白血病 | 急性早幼粒细胞白血病等 | Pfizer Inc. | Pfizer Japan, Inc. | Wyeth Pharmaceuticals LLC | Pfizer Europe MA EEIG | The Children's Mercy Hospital | Pfizer Canada ULC | 批准上市 |
| BL-M11D1 | CD33 x Top I | ADC | 急性髓性白血病 | 难治性急性髓细胞白血病 | 复发性急性髓细胞白血病 | 骨髓增生异常综合征 | 四川百利药业有限责任公司 | Systimmune, Inc. | 临床2/3期 |
| VCAR-33(National Cancer Institute) | CD33 | 自体CAR-T | 难治性急性髓细胞白血病 | 复发性急性髓细胞白血病 | Center for International Blood & Marrow Transplant Research | 临床1/2期 |
| CD123/CD33 CART(Essen Biotech) | CD123 x CD33 | CAR-T | 成人急性髓性白血病 | 难治性急性髓细胞白血病 | Essen BioTech, LLC. | 临床1/2期 |
| CD33/CD123/CLL-1 CAR-T Cells(Hebei Taihe Chunyu Biotechnology) | CD123 x CD33 x CLL-1 | CAR-T | - | 河北泰禾春雨生物科技有限公司 | 临床1/2期 |
| Lintuzumab Ac-225 | CD33 | 抗体偶联核素 | 治疗用放射药物 | 成人急性髓性白血病 | CD33阳性急性髓性白血病 | 难治性急性髓细胞白血病等 | National Cancer Institute | Actinium Pharmaceuticals, Inc. | 临床1/2期 |
| Anti-CLL1-CD33-NKG2D Bicephali CAR-T(Yake) | CD33 x CLL-1 x NKG2D | CAR-T | 难治性急性髓细胞白血病 | 上海雅科生物科技有限公司 | 临床1/2期 |
| Universal donor derived CD33 CAR-NK(Nationwide Children's Hospital) | CD33 | CAR-NK | - | Nationwide Children's Hospital | 临床1/2期 |
| MP-0533 | CD123 x CD3 x CD33 x CD70 | DARPin | 骨髓增生异常综合征 | 难治性急性髓细胞白血病 | Molecular Partners AG | 临床1/2期 |
| CLL1+CD33 CAR-T(Zhejiang University) | CD33 x CLL-1 | CAR-T | 急性髓性白血病 | 浙江大学 | 临床1期 |
(数据截止到2026年3月16日,来源于synapse)
6. CD33相关研究工具:重组蛋白、抗体与ELISA试剂盒
CD33是Siglec家族的重要成员,在髓系细胞免疫调控中发挥关键作用。其通过ITIM介导的抑制性信号通路能够调节炎症反应、细胞吞噬功能以及免疫稳态。近年来研究表明,CD33不仅在急性髓系白血病中具有重要的临床价值,还在阿尔茨海默病、慢性病毒感染以及肿瘤免疫调控中发挥重要作用。华美生物提供CD33重组蛋白、抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD33 重组蛋白
Recombinant Human Sialic acid-binding Ig-like lectin 15 (SIGLEC15), partial (Active); CSB-MP761623HU
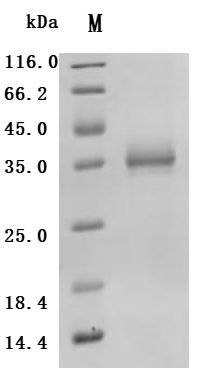
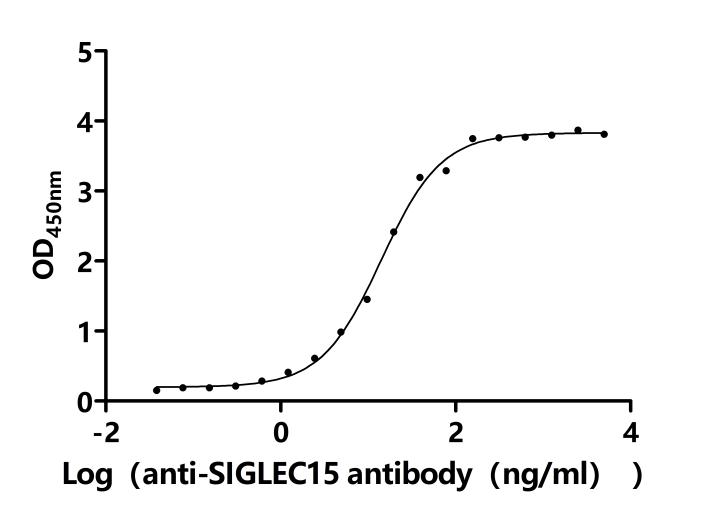
Recombinant Human Myeloid cell surface antigen CD33 (CD33), partial (Active); CSB-MP004925HU

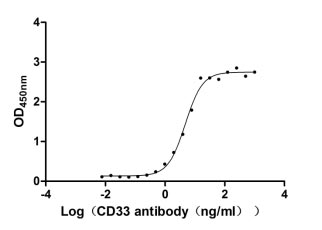
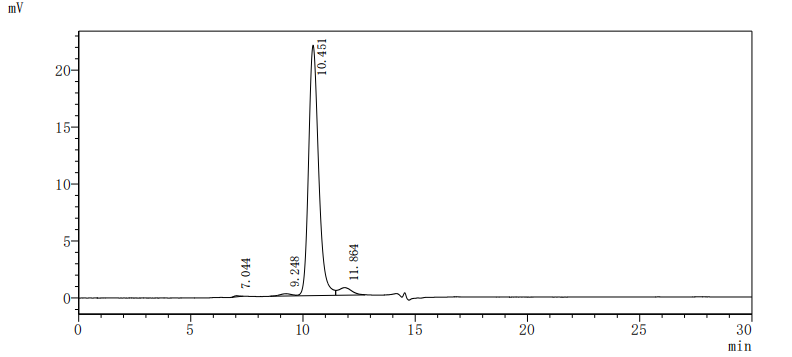
● CD33 抗体
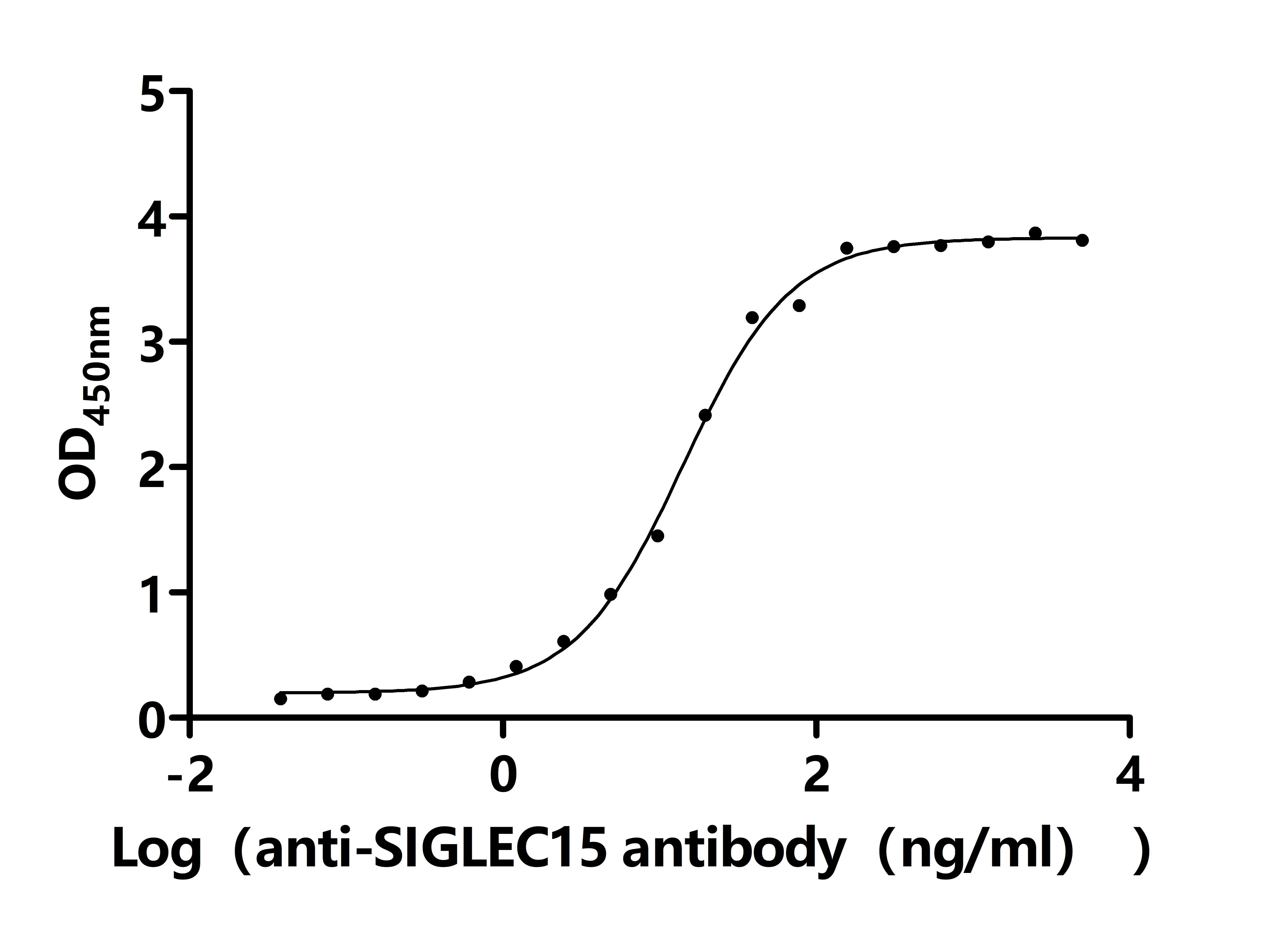
SIGLEC15 Recombinant Monoclonal Antibody
CSB-RA761623MA3HU
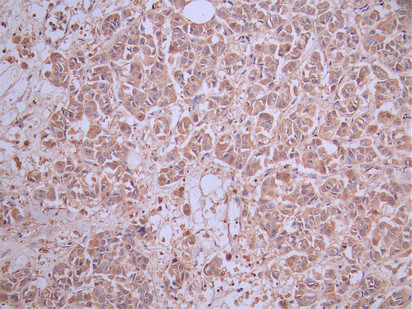
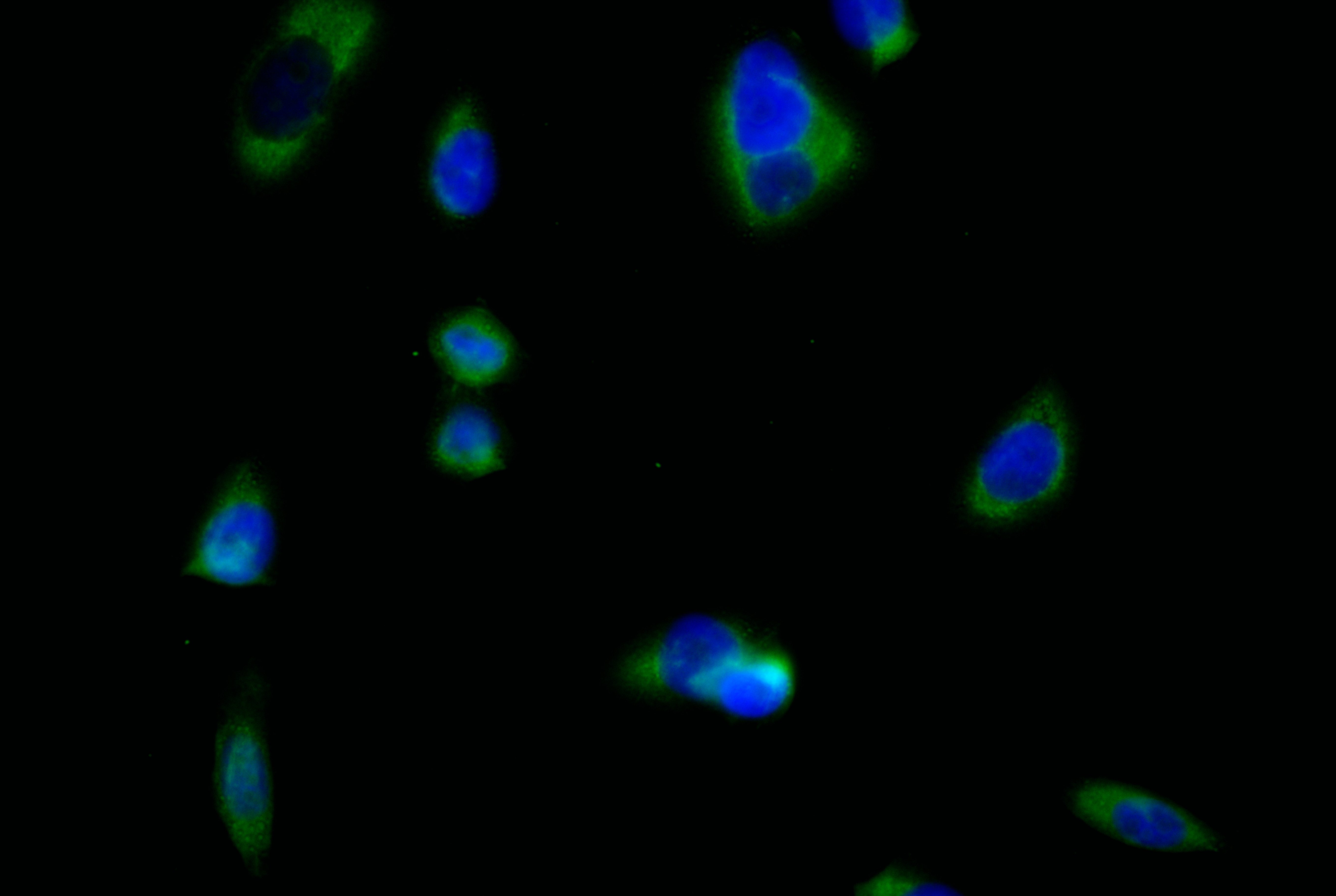
SIGLEC15 Recombinant Monoclonal Antibody
CSB-RA761623MA2HU
● CD33 ELISA 试剂盒
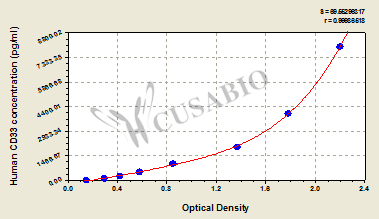
Human Myeloid cell surface antigen CD33(CD33) ELISA kit; CSB-EL004925HU
[1] E. B. D. Brinkman-van der Linden, T. Angata, S. Reynolds, L. Powell, S. Hedrick, A. Varki.(2003). CD33/Siglec-3 Binding Specificity, Expression Pattern, and Consequences of Gene Deletion in Mice.
[2] Gena S. Whitney, Shulin Wang, Han Chang, Ke-Yi Cheng, Pin Lu, Xia D. Zhou, Wen-Pin Yang, Murray McKinnon, Malinda Longphre.(2001). A new siglec family member, siglec-10, is expressed in cells of the immune system and has signaling properties similar to CD33.
[3] Yi-Jyun Lin, Pei-Shan Sung, Shie-Liang Hsieh.(2024). SIGLEC-3 (CD33) serves as an effective target in tumor progression.
[4] Mara Gilardi, Garima Kaushik, Brandon Walling, V. Sambandam, Paolo Schiavini, Stefano Cairo, Marianna Zipeto, Michael Ritchie.(2023). Correlation Revealed between Gemtuzumab-Ozogamicin Efficacy and CD33+ Expression in AML Primary Samples through a Novel AML in Vitro Model.
[5] Yoon-Chi Han, Jennifer Kahler, Nicole Piché-Nicholas, Wenyue Hu, S. Thibault, Fan Jiang, M. Leal, M. Katragadda, A. Maderna, R. Dushin, Nadira Prashad, M. Charati, T. Clark, L. N. Tumey, X. Tan, A. Giannakou, E. Rosfjord, H. Gerber, Lioudmila Tchistiakova, F. Loganzo, Christopher J. O'Donnell, P. Sapra.(2020). Development of Highly Optimized Antibody--Drug Conjugates against CD33 and CD123 for Acute Myeloid Leukemia.



