武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
BTN3A1:γδ T细胞识别肿瘤的秘密开关,免疫治疗新靶点潜力几何?
52 人阅读发布时间:2026-03-23 16:19
BTN3A1(又称CD277)是人类Vγ9Vδ2 T细胞识别磷酸抗原(pAg)的关键分子,也是连接代谢异常感知、免疫活化与治疗转化的重要节点。现有研究表明,BTN3A1的B30.2胞内结构域可选择性识别pAg,并诱导构象变化;随后,BTN3A1与BTN2A1形成功能相关复合体,将细胞内信号转化为可被Vγ9Vδ2 TCR识别的膜表结构状态。除经典的γδ T细胞激活功能外,BTN3A1还参与NK细胞调控、T细胞抑制以及TBK1-IRF3相关天然免疫信号,提示其具有明显的情境依赖性和功能双向性。围绕BTN3A1的药物开发已拓展至激动抗体、双特异性分子、γδ TCR衔接器、代谢调控剂和ADC等方向。总体来看,BTN3A1具有明确的生物学与转化价值,但其跨膜信号传导、复合体动态重构、疾病特异性功能及临床分层策略仍有待进一步厘清。
1. BTN3A1(CD277)的研究背景与生物学功能
2. BTN3A1的结构特征与磷酸抗原(pAg)识别机制
3. BTN3A1介导Vγ9Vδ2 T细胞活化的分子调控机制
4. BTN3A1的免疫调节双向性与多通路功能
5. BTN3A1在肿瘤与自身免疫病中的作用机制
6. BTN3A1靶向药物研发与肿瘤免疫治疗转化进展
7. BTN3A1研究工具:重组蛋白与抗体产品
1. BTN3A1(CD277)的研究背景与生物学功能
BTN3A1最早因其在Vγ9Vδ2 T细胞识别磷酸抗原(pAg)过程中的核心作用而受到关注。研究发现,抗CD277抗体20.1可模拟细胞内pAg累积所引发的Vγ9Vδ2 T细胞活化,而103.2则可阻断pAg或氨基双_膦_酸_盐处理后靶细胞对Vγ9Vδ2 T细胞的激活;结合siRNA敲低和结构域替换实验,相关功能最终被定位到BTN3A1亚型 [1]。同时,FRAP实验表明,细胞内pAg累积会降低BTN3A1的膜迁移率,且这一变化与后续T细胞活化密切相关,为“代谢异常—膜蛋白动力学变化—γδ TCR识别”这一模型提供了直接证据 [1]。此外,ABCA1可介导代表性pAg——异戊烯基焦磷酸(IPP)外排,而apoA-I与BTN3A1之间的相互作用可能参与这一过程,提示溶解性IPP也可能参与靶细胞与Vγ9Vδ2 T细胞之间的信号传递,但其具体识别方式仍不清楚 [2]。随着研究深入,BTN3A1的功能定位被进一步细化。BTN2A1被证明可直接结合Vγ9链相关区域,构成γδ TCR识别的初始接触,而BTN3A1则通过其胞内结构域调节与BTN2A1的空间邻近性,稳定细胞接触并放大pAg依赖性信号 [3]。在肿瘤免疫中,BTN3A1与BTN2A1的协同作用也已被证实可被抗体利用,以增强γδ T细胞对肿瘤细胞的杀伤并改善肿瘤特异性αβ T细胞的功能 [4]。不过,对CD277/BTN3家族的功能解读仍需谨慎,因为常用CD277抗体并不能区分BTN3各亚型,而不同细胞类型对BTN3A1、BTN3A2、BTN3A3的表达并不相同,这可能影响早期阻断或激动实验的结论 [5]。在炎症性疾病中,银屑病患者单核细胞表面BTN3A1上调并伴随Vγ9Vδ2 T细胞功能异常,也提示BTN3A1不仅是pAg感知分子,还是免疫调节的重要节点 [6]。
2. BTN3A1的结构特征与磷酸抗原(pAg)识别机制
BTN3A1的结构特点决定了其作为胞内pAg感知分子的功能。其关键区域是胞内B30.2(PRY/SPRY)结构域,该结构域形成一个带正电的结合口袋,可容纳带负电的_异_戊_二_烯_焦磷酸类分子,如HMBPP和IPP;生化分析、定点突变和结合实验均表明,H381等关键残基对配体识别至关重要 [7,8]。然而,现有证据显示,单纯“结合”并不足以解释BTN3A1的抗原感知功能。NMR、晶体学和分子动力学研究进一步表明,真正具有抗原性的pAg不仅进入B30.2口袋,还会诱导该结构域发生全局性构象变化,这种变构响应比单纯结合更能解释γδ T细胞的功能性激活 [9,10]。此外,部分配体虽然具有相近的结合亲和力,却无法有效诱导T细胞反应,说明“结合能力”与“致活能力”之间并不完全等同 [7]。进一步的结构研究还发现,B30.2邻近区域及近膜段可能参与二聚体形成,并将胞内构象变化传递至膜区和胞外区域,从而为后续信号扩增提供基础 [10-12]。胞内识别如何转化为胞外可识别结构,是BTN3A1研究的核心问题之一。生化重组、ITC和活细胞BRET实验表明,pAg可诱导BTN3A1与BTN2A1胞内区域发生相互作用,而BTN2A1近膜段的完整性对这一过程和后续IFNγ反应都至关重要 [13]。最近冷冻电镜研究进一步提示,pAg诱导的BTN3A1/BTN2A1复合体重构可促使BTN分子形成适于Vγ9Vδ2 TCR识别的构象架构 [14]。与此同时,抗体阻断和工程化Fab间距实验也提示,信号触发并不依赖简单聚集,而是依赖精细的几何构型与表位暴露状态 [15]。因此,当前更合理的理解是:BTN3A1并非仅是一个被动的“配体结合器”,而是一个将胞内代谢异常转译为膜表可识别信号的构象传感器。
3. BTN3A1介导Vγ9Vδ2 T细胞活化的分子调控机制
3.1 pAg促进BTN3A1/BTN2A1复合体形成
在Vγ9Vδ2 T细胞识别过程中,pAg并非只是可溶性代谢物,更像一种“分子胶水”。它首先被BTN3A1胞内域感知,随后促进BTN3A1与BTN2A1形成异源复合体,并推动信号由胞内向胞外传递。结构学和动力学研究显示,pAg可位于BTN3A1–BTN2A1复合界面的关键位置,稳定两者的胞内接触并推动有利于外向构象显现的动态变化 [16]。遗传学和细胞学研究也进一步证实,BTN2A1是pAg感知通路中不可缺少的组分,并可直接接触Vγ9相关区域,因此BTN3A1–BTN2A1复合体应被视为功能整体,而非彼此独立的两个分子 [17]。不过,当前大部分证据仍来自截短构建体或体外体系,对全长膜蛋白在天然膜环境中的动态行为仍缺少直接观测 [18]。
3.2 复合体识别、inside-out传导与调控因素
研究显示,BTN2A1和BTN3A1共同构成Vγ9Vδ2 TCR识别所需的复合配体:BTN2A1侧向接触TCR,而BTN3A1则提供另一识别表位,二者形成的复合体及其动力学状态决定了识别效率 [19]。从信号路径上看,pAg与BTN3A1胞内B30.2(PRY/SPRY)结构域结合后,可通过“inside-out”方式触发胞外构象变化;这种刺激与抗BTN3A抗体诱导的激活在ZAP70、PLCγ2、Akt、NFκB、p38和Erk等下游磷酸化事件上具有高度一致性 [20,21]。此外,BTN3A1的蛋白稳定性、膜定位和亚细胞转运也会影响该过程。相关研究提示,ABCG2等转运蛋白与BTN3A依赖性激活存在相关性,而BTN3A2则可能调节BTN3A1的转运和最佳活性 [22,23]。因此,BTN3A1介导的Vγ9Vδ2 T细胞激活并不是单一配体结合事件,而是一个受复合体组装、膜定位和细胞内递送共同调控的过程 [19-23]。
4. BTN3A1的免疫调节双向性与多通路功能
BTN3A1并不只服务于Vγ9Vδ2 T细胞识别。研究发现,经pAg刺激的γδ T细胞可通过BTN3A1依赖、细胞接触依赖的方式抑制NK细胞对“missing-self”靶标的反应,并伴随NKG2D和NKp44下调,提示BTN3A1可能参与先天免疫效应细胞之间的负向调节 [24]。另一方面,LSECtin与BTN3A1结合可抑制人T细胞增殖及炎症因子产生,且该抑制可被抗BTN3A1抗体部分逆转,说明BTN3A1还可作为细胞表面的负信号受体 [25]。与此相对,BTN3A1在天然免疫中又具有正向作用。已有研究表明,BTN3A1可与TBK1组成复合体,在核酸刺激下通过MAP4控制的dynein依赖运输重定位至近核区域,促进TBK1与IRF3相互作用并增强IFN-β产生;敲减BTN3A1会削弱细胞对胞质DNA或RNA的I型干扰素应答 [26]。这说明BTN3A1具有明显的功能双向性:它既可参与抑制性细胞间接触信号,也可作为胞内支架促进抗病毒通路激活。正因如此,未来任何针对BTN3A1的治疗设计,都必须充分考虑其结构域分工、刺激情境和细胞类型差异。
5. BTN3A1在肿瘤与自身免疫病中的作用机制
在肿瘤免疫中,BTN3A1具有显著的双重作用。一方面,BTN3A1与BTN2A1的协同、以及相关近膜调控事件,是Vγ9Vδ2 T细胞识别并清除早期异常细胞的重要基础;蛋白互作组学还提示PHLDB2、SYNJ2、CARMIL1等因子可调节BTN2A1/BTN3A1表面动力学,从而影响抗肿瘤监视 [27]。另一方面,在宫颈癌等模型中,肿瘤细胞高表达BTN3A1又可直接驱动Vδ2 T细胞耗竭,诱导NR4A2/3上调并降低效应分子分泌;同时,Vδ2 T细胞产生的IFN-γ反过来又可促进肿瘤细胞上调BTN3A1和PD-L1,形成负反馈的免疫抑制环路 [28]。因此,尽管靶向BTN3A1的抗体在模型中显示出增强抗肿瘤反应的潜力,但如何平衡“促活化”与“防耗竭”仍是转化中的关键问题 [29]。不同癌种中BTN3A1与预后的关系也并不一致。在部分乳腺癌队列中,BTN3A1高表达与更好的生存结局及更高的免疫浸润相关 [30];而在胶质瘤中,BTN3A1高表达则更多与免疫抑制特征和不良预后相关 [31]。这说明单一表达量不足以作为稳定的预后或治疗生物标志物,还必须结合细胞类型、伴侣分子和信号修饰状态来综合判断。除肿瘤外,BTN3A1还可能参与自身免疫疾病。孟德尔随机化、共定位和多组学分析显示,BTN3A1血浆蛋白水平与IgA肾病风险存在显著相关,在干燥综合征研究中也被识别为候选相关基因 [32,33]。不过,这类遗传和多组学证据仍需要进一步的组织和功能验证,才能明确其真实因果作用及药物开发价值。
6. BTN3A1靶向药物研发与肿瘤免疫治疗转化进展
针对BTN3A1靶点的药物研发已进入早期临床验证阶段,目前全球进度最快的候选药(ICT-01)已在急性髓系白血病及晚期实体瘤中推进至临床1/2期。整体来看,该靶点吸引了国内外多家机构布局,药物形式涵盖单抗、小分子及TCR融合蛋白等,适应症以肿瘤为主,同时向感染、自身免疫病等领域拓展,但绝大多数项目仍处于临床前或药物发现阶段。
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| ICT-01 | BTN3A1 | 单克隆抗体 | 急性髓性白血病 | 急性淋巴细胞白血病 | 晚期癌症 | 晚期恶性实体瘤等 | Imcheck Therapeutics SAS | 临床1/2期 |
| ICT-41 | BTN3A1 | 单克隆抗体 | 细菌感染 | 病毒感染 | Imcheck Therapeutics SAS | 临床前 |
| CD20-targeted GADLEN(Shattuck Labs) | BTN2A1 x BTN3A1 x CD20 x CD3 | TCR融合蛋白 | T细胞结合器 | 抗体融合蛋白 | 肿瘤 | Shattuck Labs, Inc. | 临床前 |
| CD19GADLEN | BTN2A1 x BTN3A1 x CD19 | 抗体融合蛋白 | 淋巴瘤 | Shattuck Labs, Inc. | 临床前 |
| BTN3A1 ligand Compound 26b(University of Iowa) | BTN3A1 | 化学药 | 肿瘤 | University of Iowa | 临床前 |
| B7-H3 GADLEN | BTN2A1 x BTN3A1 x CD20 x CD276 | 抗体融合蛋白 | 肿瘤 | Shattuck Labs, Inc. | 临床前 |
| BSI-093 | BTN3A1 | 单克隆抗体 | 胆道癌 | 食管癌 | 头颈部鳞状细胞癌 | 博奥信生物技术(南京)有限公司 | 临床前 |
| POM2-C-HMBP | BTN3A1 | 小分子化药 | 肿瘤 | University of Iowa | University of Connecticut | 药物发现 |
| WO2024146627 | BTN3A1 | 小分子化药 | 自身免疫性疾病 | 心血管疾病 | 感染 | 肿瘤 | 北京清辉联诺生物科技有限责任公司 | 药物发现 |
| Compound 6e(MIT-World Peace University) | BTN3A1 | 小分子化药 | - | University of Connecticut | 药物发现 |
| US20230285527 | BTN3A1 | 单克隆抗体 | 免疫系统疾病 | Université d'Aix-Marseille | Nantes Universite | Centre National de la Recherche Scientifique | Institut Jean Paoli & Irene Calmettes | 药物发现 |
| CN117295505 | BTN3A1 | 细胞疗法 | 免疫系统疾病 | 肿瘤 | The Regents of the University of California | The J. David Gladstone Institutes | 药物发现 |
| WO2024146629 | BTN3A1 | 小分子化药 | 自身免疫性疾病 | 心血管疾病 | 感染 | 肿瘤 | 北京清辉联诺生物科技有限责任公司 | 药物发现 |
(数据截止到2026年3月12日,来源于synapse)
7. BTN3A1研究工具:重组蛋白与抗体产品
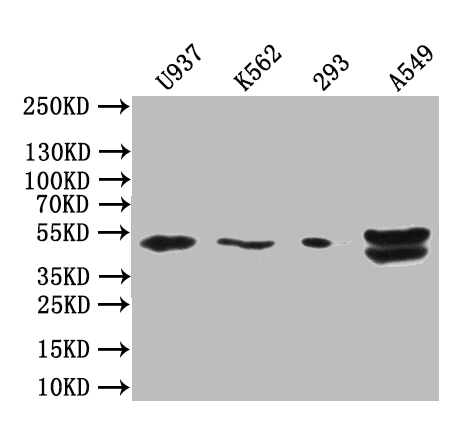
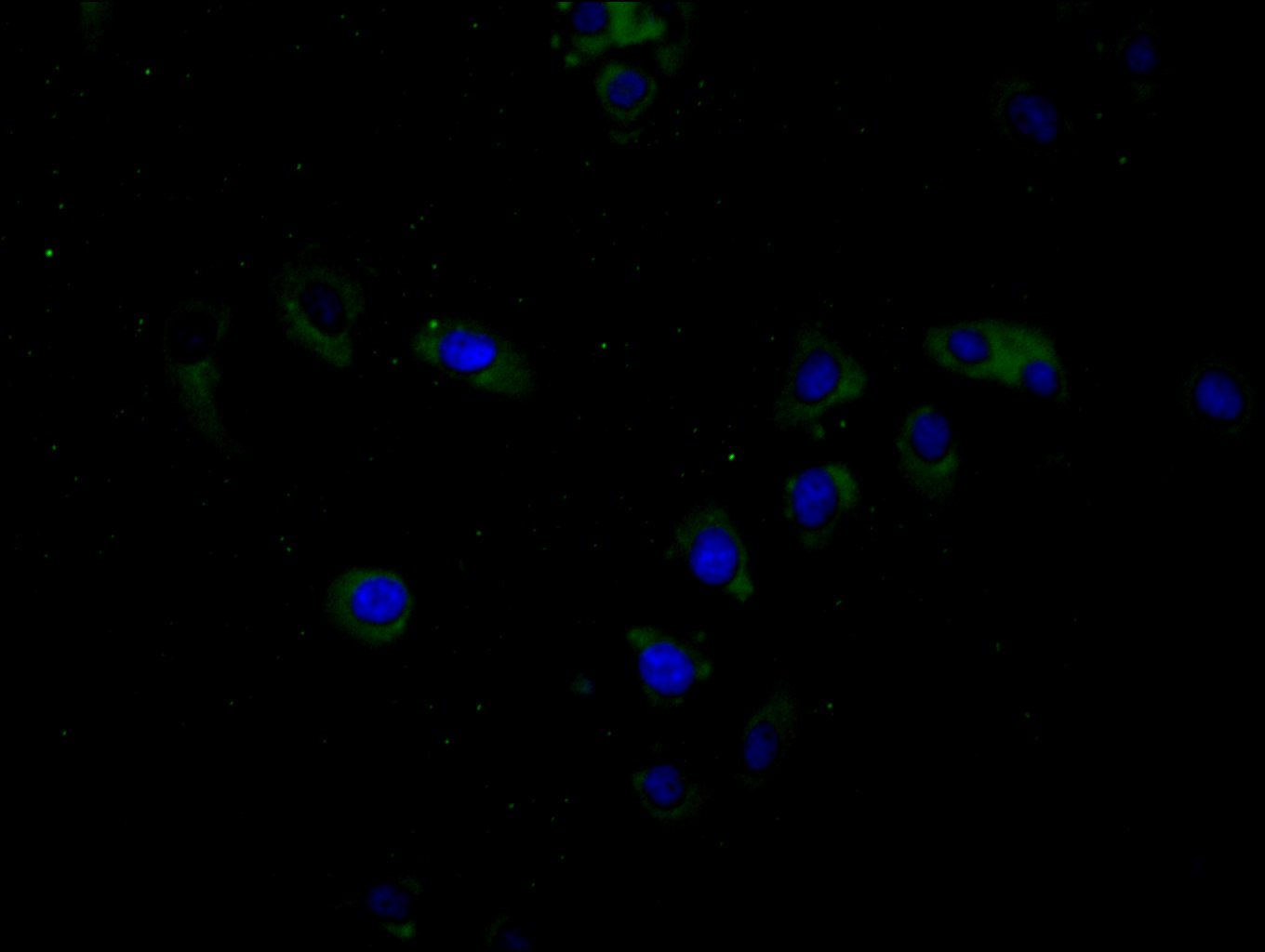
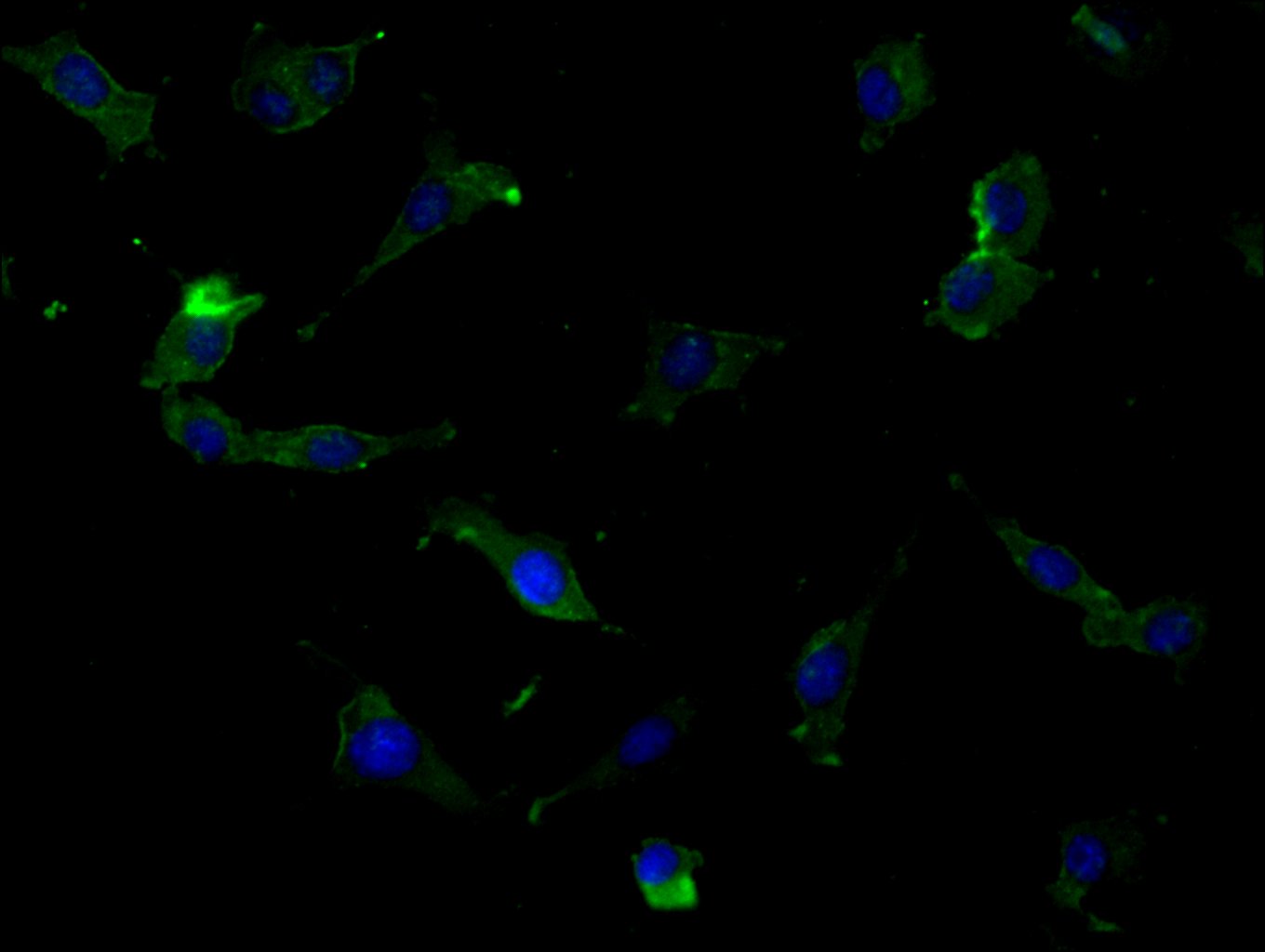
目前,BTN3A1已从一个家族成员注释分子,发展为解释人类Vγ9Vδ2 T细胞识别磷酸抗原(pAg)机制的核心节点。华美生物提供BTN3A1重组蛋白和抗体产品,助力您进行相关机制研究及靶向药物开发。
● BTN3A1 重组蛋白
Recombinant Human Butyrophilin subfamily 3 member A1 (BTN3A1), partial
CSB-MP002873HU
Recombinant Human Butyrophilin subfamily 3 member A1 (BTN3A1), partial
CSB-EP002873HUb0
● BTN3A1 抗体
BTN3A1 Recombinant Monoclonal Antibody; CSB-RA002873MA2HU
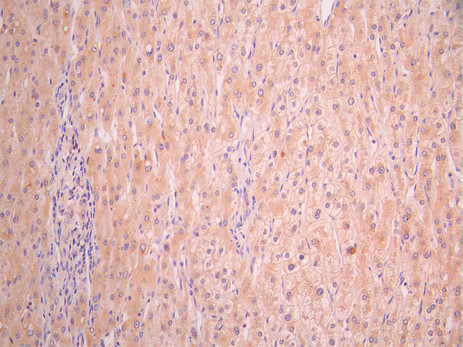
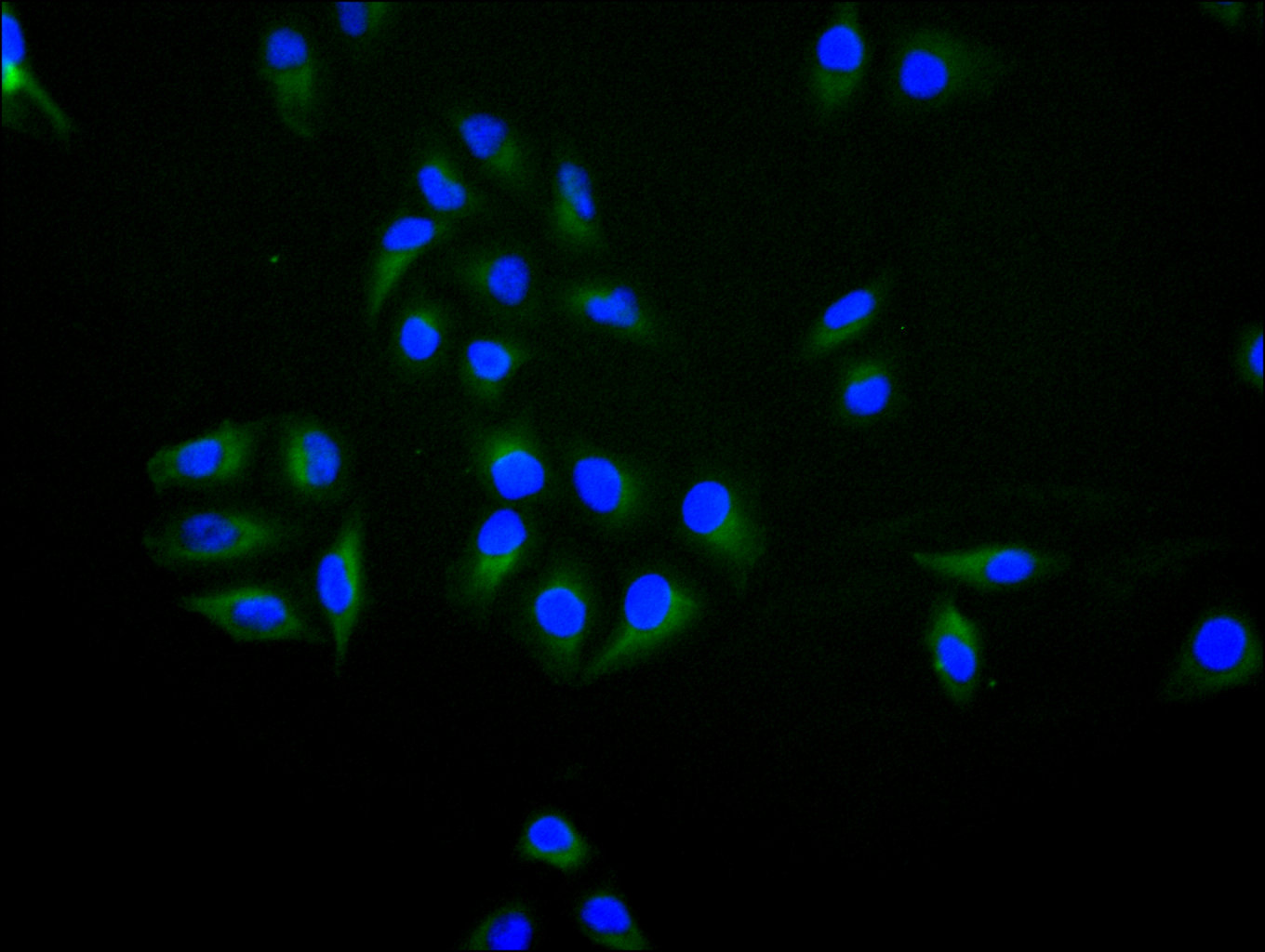
BTN3A1 Antibody; CSB-PA002873LA01HU
[1] Harly C, Guillaume Y, Nedellec S, et al. Key implication of CD277/butyrophilin-3 (BTN3A) in cellular stress sensing by a major human γδ T-cell subset. Blood. 2012;120(11):2269-2279.
[2] Riganti C, Castella B, Massaia M. ABCA1, apoA-I, and BTN3A1: A Legitimate Ménage à Trois in Dendritic Cells. Front Immunol. 2018;9:2802.
[3] Vyborova A, Beringer DX, Fasci D, et al. γ9δ2T cell diversity and the receptor interface with tumor cells. Nat Commun. 2020;11(1):6296.
[4] Kelly PN. BTN3A1 governs antitumor responses. Science. 2020;369(6503):504-505.
[5] Messal N, Mamessier E, Sylvain A, et al. Differential role for CD277 as a co‐regulator of the immune signal in T and NK cells. Eur J Immunol. 2011;41(11):3234-3244.
[6] Zhou J, Zhang J, Tao L, et al. Up-regulation of BTN3A1 on CD14+ monocytes in psoriasis patients contributes to Vγ9Vδ2 T cell activation. J Dermatol Sci. 2022;108(3):179-187.
[7] Poe MM, Agabiti SS, Liu C, et al. Probing the Ligand-Binding Pocket of BTN3A1. ACS Chem Biol. 2019;14(12):2681-2691.
[8] Wang H, Morita CT. Sensor Function for Butyrophilin 3A1 in Prenyl Pyrophosphate Stimulation of Human Vγ2Vδ2 T Cells. J Immunol. 2015;195(5):2359-2368.
[9] Salim M, Knowles TJ, Baker AT, et al. BTN3A1 Discriminates γδ T Cell Phosphoantigens from Nonantigenic Small Molecules via a Conformational Sensor in Its B30.2 Domain. J Biol Chem. 2017;292(16):6662-6673.
[10] Gu S, Sachleben JR, Boughter CT, et al. Phosphoantigen-induced conformational change of butyrophilin 3A1 (BTN3A1) and its implication on Vγ9Vδ2 T cell activation. Proc Natl Acad Sci U S A. 2017;114(30):E6119-E6128.
[11] Peigné CM, Léger A, Gesnel MC, et al. The Juxtamembrane Domain of Butyrophilin BTN3A1 Controls Phosphoantigen-Mediated Activation of Human Vγ9Vδ2 T Cells. Cell Rep. 2017;19(13):2773-2785.
[12] Nguyen K, Hsiao CHC, Jin Y, Wiemer AJ, Vinogradova O. Investigation of structural and dynamic properties of the Butyrophilin BTN3A1/BTN2A1 cytoplasmic complex by NMR spectroscopy. J Biomol NMR. 2025;79(1):1-14.
[13] Hsiao CHC, Nguyen K, Jin Y, Vinogradova O, Wiemer AJ. Ligand-induced interactions between butyrophilin 2A1 and 3A1 internal domains in the HMBPP receptor complex. J Biol Chem. 2022;298(12):102684.
[14] Zhang M, Wang Y, Cai N, et al. Cryo-EM structural insights into Vγ9Vδ2 TCR activation via multiple butyrophilins. Cell Res. 2024;34(2):128-141.
[15] Ramesh A, Roy S, Slezak T, et al. Mapping the extracellular molecular architecture of the pAg-signaling complex with α-Butyrophilin antibodies. Cell Rep. 2025;48(3):113568.
[16] Yuan L, Ma X, Yang Y, et al. Phosphoantigens glue butyrophilin 3A1 and 2A1 to activate Vγ9Vδ2 T cells. Nature. 2023;621(7980):649-656.
[17] Rigau M, Ostrouska S, Fulford TS, et al. Butyrophilin 2A1 is essential for phosphoantigen reactivity by γδ T cells. Science. 2020;367(6477):eaay5516.
[18] Yuan L, Ma X, Yang Y, et al. Phosphoantigens are Molecular Glues that Promote Butyrophilin 3A1/2A1 Association Leading to Vγ9Vδ2 T Cell Activation. bioRxiv. 2022:2022.07.25.501389.
[19] Fulford TS, Soliman C, Castle RG, et al. Vγ9Vδ2 T cells recognize butyrophilin 2A1 and 3A1 heteromers. Nat Immunol. 2023;24(3):424-435.
[20] Gu S, Nawrocka WI, Adams EJ. Sensing of Pyrophosphate Metabolites by Vγ9Vδ2 T Cells. J Immunol. 2015;195(5):2049-2056.
[21] Decaup E, Duault C, Bezombes C, et al. Phosphoantigens and butyrophilin 3A1 induce similar intracellular activation signaling in human TCRVγ9+ γδ T lymphocytes. Eur J Immunol. 2014;44(11):3323-3333.
[22] Rhodes DA, Chen HC, Williamson JC, et al. Regulation of Human γδ T Cells by BTN3A1 Protein Stability and ATP-Binding Cassette Transporters. Cell Rep. 2018;24(6):1548-1560.e6.
[23] Vantourout P, Laing A, Woodward MJ, et al. Heteromeric interactions regulate butyrophilin (BTN) and BTN-like molecules governing γδ T cell biology. Proc Natl Acad Sci U S A. 2018;115(5):1039-1044.
[24] Walwyn-Brown K, Pugh J, Cocker ATH, et al. Phosphoantigen-Stimulated γδ T Cells Suppress Natural Killer–Cell Responses to Missing-Self. Front Immunol. 2022;13:864704.
[25] Wang J, Manick B, Renelt M, et al. LSECtin interacts with BTN3A1 to inhibit T cell activation. Mol Immunol. 2020;126:120-128.
[26] Seo M, Lee SO, Kim JH, et al. MAP4-regulated dynein-dependent trafficking of BTN3A1 controls the TBK1-IRF3 signaling axis. Proc Natl Acad Sci U S A. 2016;113(29):8266-8271.
[27] Cleven A, Meringa AD, Brázda P, et al. Sensitivity to Vγ9Vδ2TCR T cells is imprinted after single mutations during early oncogenesis. Cell. 2024;187(1):182-198.e24.
[28] Liu J, Wu M, Yang Y, et al. BTN3A1 expressed in cervical cancer cells promotes Vγ9Vδ2 T cells exhaustion through upregulating transcription factors NR4A2/3 downstream of TCR signaling. J Immunother Cancer. 2024;12(4):e008795.
[29] Payne KK, Mine JA, Biswas S, et al. BTN3A1 governs antitumor responses by coordinating αβ and γδ T cells. Science. 2020;369(6503):593-599.
[30] Ren H, Li S, Liu X, et al. Multi-omics analysis of the expression and prognostic value of the butyrophilins in breast cancer. Cancer Cell Int. 2021;21(1):619.
[31] Kone AS, Ghouzlani A, Qandouci A, et al. High expression of BTN3A1 is associated with clinical and immunological characteristics and predicts a poor prognosis in advanced human gliomas. J Neurooncol. 2024;166(2):387-398.
[32] Xu X, Miao C, Yang S, et al. Investigating potential drug targets for IgA nephropathy and membranous nephropathy through multi-queue plasma protein analysis: a Mendelian randomization study based on SMR and co-localization analysis. Front Immunol. 2024;15:1372489.
[33] Bai Y, Wang J, Feng X, et al. Identification of drug targets for Sjögren's syndrome: multi-omics Mendelian randomization and colocalization analyses. Front Immunol. 2024;15:1357177.
[34] Oberg HH, Deseke M, Krohn S, et al. Tumor-restricted activation of Vγ9Vδ2 T cells via bispecific Evobodies: a novel strategy for safe and potent immunotherapy in ovarian cancer. Cancer Immunol Immunother. 2025;74(3):689-702.



