武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
CD28:T细胞免疫的"开关"——从分子机制到肿瘤免疫治疗
119 人阅读发布时间:2026-03-23 16:17
遵循双信号模型是T细胞活化的经典理论:T细胞受体(TCR)识别抗原后,还需要来自共刺激分子的第二信号,才能使初始T细胞摆脱静息状态并形成有效免疫应答。在这一过程中, CD28 是最关键的共刺激受体之一 [1]。
作为免疫球蛋白超家族成员,CD28通过与抗原提呈细胞表面的B7家族分子结合,为T细胞提供有效活化所必需的信号。它不仅放大TCR输入,更会独立塑造下游生物学结果,包括细胞骨架重塑、IL-2等细胞因子产生、增殖增强、存活提升以及分化程序启动 [1]。更重要的是,CD28介导的信号还可引发表观遗传、转录和翻译后层面的改变,而这些变化并不能单靠TCR刺激复制出来 [1]。
1. CD28的生物学意义
2. CD28的分子结构、配体识别与信号转导机制
3. CD28在免疫调节与疾病发生发展中的作用
4. CD28靶向药物研究进展
5. CD28研究工具
1. CD28的生物学意义
CD28的意义并不限于初始和效应T细胞。它同样是调节性T细胞(Treg)维持和功能稳定的重要分子,这使其同时处于免疫激活和免疫耐受的交汇点 [1]。也正因为如此,CD28既具有明显的治疗开发价值,也带来更高的调控复杂性。
既往针对CD28家族相互作用的临床干预既有成功经验,也存在明显挫折,这说明CD28虽然是强有力的免疫调控靶点,但其作用并非简单的"增强"或"抑制"即可概括 [1]。不同T细胞亚群中的功能差异、鼠与人的网络差异,以及CD28家族内部的受体—配体串扰,都提示其 CD28靶向治疗 开发必须更强调时序性、细胞类型特异性和情境依赖性 [1]。因此,CD28研究的核心价值,不仅在于阐明T细胞共刺激的基本规律,也在于为精准免疫调控和安全转化提供理论基础。
2. CD28的分子结构、配体识别与信号转导机制
2.1 CD28的结构特征与配体识别
CD28是T细胞表面的关键共刺激分子,其结构可概括为三个功能区域:负责配体识别的胞外区、单次跨膜螺旋以及将胞外结合事件转化为胞内信号的短胞内尾段。CD28的经典配体是B7家族分子CD80和CD86,这一受体—配体相互作用构成了T细胞活化所必需的"第二信号",并在iNKT细胞发育等生理过程中具有不可替代的作用 [2,3]。在治疗研究中,模拟天然配体的可溶性CD80融合蛋白已显示出在肿瘤微环境中恢复或增强CD28共刺激的潜力,并可能兼顾免疫激活与安全性窗口 [2]。
近年来,关于CD28构象动力学的研究进一步拓展了人们对其调控方式的认识。相关研究提出,胞内膜叶层酸性磷脂与细胞内钙离子可作为相反的带电因素,共同调节CD28的构象状态及其跨膜信号传递能力 [4]。这一观点提示,CD28并非简单的"开/关"型受体,而更像一个受局部膜环境和离子条件精细调控的分子开关,有助于解释共刺激阈值及其时空特异性 [4]。不过,目前对于这一构象变化如何通过跨膜区和短胞内尾段传递到下游信号复合体,仍缺乏足够的高分辨率结构和动态实验证据 [4]。
此外,CD28配体结合位点的精细特异性也受到关注。分子动力学模拟和自由能计算提示,一些非典型配体如β-1,3寡聚糖,可能在接近B7结合位点的位置与CD28发生低亲和力相互作用 [5]。这提示CD28表面可能存在比传统蛋白—蛋白识别更复杂的相互作用界面。但这类结果目前仍主要停留在计算和推测层面,其体内生理意义仍需更多生化和功能实验加以验证 [5]。总体来看,现有证据表明,CD28的配体识别既具有明确的结构基础,也受到膜环境和离子条件的动态调节,这为理解其信号启动机制和药物开发可操作性提供了重要依据 [2-5]。
2.2 CD28介导的关键信号通路与分子机制
在抗原刺激后,TCR近端信号首先表现为CD3和TCRζ链的酪氨酸磷酸化,以及Lck和ZAP70的募集与激活。活细胞TIRF成像研究显示,CD28共刺激可显著加快Lck向TCR微簇的募集,并改变活性与非活性Lck的空间分布,进而促进ZAP70更快、更充分地结合并被激活,最终降低TCR激活阈值并增强CD3ζ等近端信号放大效应 [6]。这一结果说明,CD28并非仅在下游增强信号,而是在极早期就通过重塑信号微环境来改变T细胞激活效率 [6]。
在此基础上,CD28将信号进一步传递至多条经典 CD28信号通路 。计算与实验结合的CAR-T模型提示,CD28可通过增强CD3ζ磷酸化动力学来加速ERK激活,说明其对MAPK通路的影响,关键可能在于放大近端酪氨酸激酶事件,而非直接启动下游MAPK模块 [7]。磷酸化谱分析进一步表明,CD28共刺激可诱导一组具有特异性的酪氨酸激酶和受体酪氨酸激酶磷酸化模式,显示不同共刺激通路在信号节点选择上具有分子差异 [8]。同时,CD28还可协调PLCγ-1/IP3R相关钙信号,进而激活NFAT、AP-1和NF-κB等转录因子,促进IL-2及其他细胞因子的表达 [9]。
CD28信号也受到多种负向调控通路制约。TIM-3可与Lck、ITK及PI3K适配子p85相互作用,从而抑制CD3/CD28诱导的NF-κB和NFAT活性,并减少IL-2分泌[10]。B7-H7(HHLA2)在与TCR和CD28共同刺激时表现出抑制效应,其转录反应明显弱于经典B7-1共刺激,提示其可在生理性APC-T细胞互作中发挥"刹车"作用 [11]。更值得关注的是,PD-1招募的Shp2对CD28的去磷酸化偏好性甚至强于TCR组分,这说明免疫检查点可通过直接抑制CD28共刺激而削弱T细胞功能 [12]。这些发现改变了人们对共抑制信号的理解,也突出了CD28在效应T细胞功能维持中的核心地位。
除经典的激酶—转录轴外,CD28还通过转录后调控和代谢重编程影响T细胞命运。在CD8+ T细胞中,CD28可上调ARS2,促进剪接因子募集并改变激活相关的可变剪接事件,其中PKM1向PKM2的剪接转变被证明与葡萄糖代谢灵活性、IFN-γ产生和抗肿瘤功能密切相关,且这一过程独立于CD28驱动的PI3K通路 [13]。同时,CD28在某些情况下还能通过CAPRI介导Rap1失活而抑制细胞黏附,说明其信号输出并非单向增强,而是具有明显的情境依赖性和功能分化特点 [14]。因此,CD28应被理解为一个整合近端激酶、转录因子、可变剪接和代谢程序的复杂信号节点,而非单一路径放大器 [6-14]。
3. CD28在免疫调节与疾病发生发展中的作用
3.1 CD28与免疫耐受及自身免疫疾病
在免疫耐受建立过程中,B7-CD28共刺激既参与胸腺中的克隆删除,也支持Treg发育,但两者对CD28信号的依赖程度和对不同抗原提呈细胞的需求并不相同 [15]。小鼠研究显示,内生性组织限制性抗原特异性胸腺细胞的克隆删除和Treg诱导均依赖B7-CD28相互作用,但两者在信号强度、时间窗口和APC来源上的要求存在差异 [15]。更重要的是,当B7-CD28信号异常导致胸腺克隆删除受损时,成熟的自身反应性T细胞可在外周积累,并具备介导破坏性自身免疫的能力 [15]。这说明CD28不仅参与效应激活,也深度介入中心耐受的建立。
临床干预证据同样提示,CD28信号失衡与自身免疫密切相关。针对CTLA-4/B7轴的治疗可通过改变CD28获取共刺激的机会而影响T细胞反应,这在某些情境下具有治疗价值,但也可能扰动Treg稳态和耐受维持。由此可见,CD28通路并不适合简单地全局增强或全局抑制,而更需要根据疾病背景、T细胞亚群构成和病理阶段进行精细调控 [15-17]。
3.2 CD28在肿瘤免疫中的双重角色
CD28在 肿瘤免疫 中首先表现为抗肿瘤应答所需的关键共刺激分子。条件性敲除和慢性感染/肿瘤模型均显示,CD28/B7信号对于维持CD8+ T细胞功能和改善抗PD-1等治疗反应具有重要意义 [18]。这说明,即便在免疫检查点阻断背景下,效应T细胞仍需要CD28提供共刺激支持,才能维持较强的杀伤和增殖能力 [18]。
但CD28的作用并不完全是单向促效应。随着研究深入,人们发现CD28功能会受到肿瘤微环境、细胞类型和空间位置的复杂影响。例如,某些研究提示肿瘤相关环境可通过改变共刺激和共抑制信号平衡,重新塑造CD28输出,甚至在某些情况下限制治疗获益。此外,体内CRISPR筛选还提示,在特定肿瘤模型中,癌细胞自身也可能与CD28相关通路发生更复杂的非经典联系,这意味着CD28在肿瘤中的功能不应只从T细胞角度理解 [19-21]。因此,CD28在肿瘤免疫中的价值,既体现在促进抗肿瘤T细胞应答,也体现在它是连接共刺激、检查点和微环境抑制的重要交汇点。
3.3 CD28与衰老及其他疾病
随着年龄增长,外周免疫系统会发生明显重塑,其中CD28表达下降是最具代表性的T细胞衰老特征之一。对大样本人群的横断面分析表明,年龄增长伴随初始T细胞减少、终末分化或衰老相关T细胞比例上升,而CD28表达的下降则提示T细胞获得有效共刺激和增殖能力的基础被削弱 [22]。从功能上看,这种变化可能导致初始免疫应答能力下降、免疫监视减弱以及慢性低度炎症持续存在。
虽然这类研究多为横断面设计,尚难直接推断个体生命周期中的因果变化,但现有证据已提示,CD28丢失与免疫衰老、"炎症老化"及某些慢性疾病风险增加存在明显联系 [22,23]。因此,CD28不仅是T细胞共刺激分子,也是观察免疫衰老和免疫功能衰退的重要指标。
4. CD28靶向药物研究进展
目前靶向CD28的药物研发活跃,涵盖CAR-T、双/多特异性抗体等多种类型,主要应用于自身免疫病和各类癌症。部分药物如治疗狼疮性肾炎和淋巴瘤的产品已进入临床2/3期及2期,另有30余款处于临床1/2期或1期阶段,显示出广阔的治疗前景。部分在研管线列举如下表:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| Mivocabtagene Autoleucel(Kyverna) | CD19 x CD28 | 自体CAR-T | 狼疮性肾炎 | 类风湿关节炎 | 系统性硬皮病 | 僵人综合征 | 重症肌无力等 | Kyverna Therapeutics, Inc. | Hannover Medical School | 临床2/3期 |
| CD19CAR-CD28-CD3zeta-EGFRt-expressing Tn/mem-enriched T-lymphocytes(City of Hope National Medical Center) | CD19 x CD28 x EGFR | 自体CAR-T | 复发性套细胞淋巴瘤 | 难治性套细胞淋巴瘤 | 原发性中枢神经系统淋巴瘤等 | City of Hope National Medical Center | 临床2期 |
| Pegrizeprument | CD28 | Fab片段抗体 | 肾移植排斥反应 | 器官移植排斥 | 类风湿关节炎 | Veloxis Pharmaceuticals A/S | Biomedical Primate Research Centre | OSE Immunotherapeutics SA | Janssen Global Services LLC | 临床2期 |
| Acazicolcept | CD28 x ICOS | 双特异性抗体 | 狼疮性肾炎 | 系统性红斑狼疮 | Alpine Immune Sciences, Inc. | 临床2期 |
| Dalmitamig | CD28 x EGFR | 双特异性抗体 | 转移性非小细胞肺癌 | 非小细胞肺癌IIIB期 | 局部晚期直肠癌 等 | Regeneron Pharmaceuticals, Inc. | 临床2期 |
| REGN-5668 | CD28 x MUC16 | 双特异性抗体 | 铂类耐药性原发性腹膜癌 | 复发性卵巢癌 | 子宫内膜癌等 | Regeneron Pharmaceuticals, Inc. | 临床1/2期 |
| SIM-323 | CD28 x CTLA4 x IL-2Rβγ | Fc融合蛋白 | 晚期恶性实体瘤 | 膀胱癌 | 结直肠癌 | 食管鳞状细胞癌等 | GI Innovation, Inc. | 临床1/2期 |
| REGN-17372 | CD28 x GPRC5D | 双特异性抗体 | - | Regeneron Pharmaceuticals, Inc. | 临床1/2期 |
| ZGGS34 | CD28 x CD3 x MUC17 | 三特异性T细胞接合器 | 晚期恶性实体瘤 | 苏州泽璟生物制药股份有限公司 | 临床1/2期 |
| MDX-2003 | CD19 x CD20 x CD28 x CD3 | 四特异性抗体 | 滤泡性淋巴瘤 | 高级别B细胞淋巴瘤 | 淋巴浆细胞性淋巴瘤等 | ModeX Therapeutics, Inc. | 临床1/2期 |
(数据截止到2026年3月15日,来源于synapse)
5. CD28研究工具
CD28是T细胞共刺激网络中的核心分子,对T细胞活化、增殖、代谢重编程、效应维持和免疫耐受都具有不可替代的作用,已经从经典的T细胞共刺激分子,发展为兼具机制研究深度和临床转化潜力的重要靶点。华美生物提供CD28重组蛋白、抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD28 重组蛋白
Recombinant Human T-cell-specific surface glycoprotein CD28 (CD28), partial ; CSB-MP004913HU1
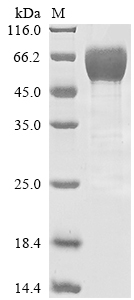
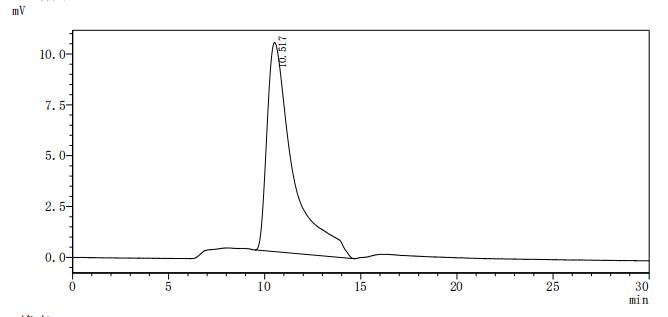
● CD28 抗体
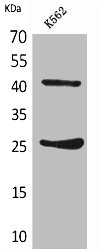
CD28 Antibody; CSB-PA005199
● CD28 ELISA 试剂盒
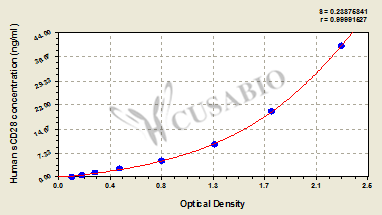
Human soluble cluster of differentiation 28,sCD28 ELISA Kit; CSB-E09296h
[1] Jonathan H Esensten, Ynes A Helou, Gaurav Chopra, Arthur Weiss, Jeffrey A Bluestone.(2016). CD28 Costimulation: From Mechanism to Therapy.
[2] Songna Wang, Pinliang Hu, Xuyao Zhang, Jiajun Fan, Jing Zou, Weidong Hong, Xuan Huang, Danjie Pan, Huaning Chen, Dianwen Ju, Yi Zhun Zhu, Li Ye.(2025). Recombinant CD80 fusion protein combined with discoidin domain receptor 1 inhibitor for cancer treatment.
[3] Masashi Watanabe, Sofia Celli, Farrah A Alkhaleel, Richard J Hodes.(2022). Antigen-presenting T cells provide critical B7 co-stimulation for thymic iNKT cell development via CD28-dependent trogocytosis.
[4] Wei Yang, Weiling Pan, Shuokai, Nicola Trendel, Shutan Jiang, Feng Xiao, Manman Xue, Wei Wu, Zeli Peng, Xiaoxi Li, Hongbin Ji, Xiaolong Liu, Hai Jiang, Haopeng Wang, Hongbin Shen, Omer Dushek, Hua Li, Chenqi Xu.(2017). Dynamic regulation of CD28 conformation and signaling by charged lipids and ions.
[5] Jeffrey Comer, Molly Bassette, Riley Burghart, Mayme Loyd, Susumu Ishiguro, Ettayapuram Ramaprasad Azhagiya Singam, Ariela Vergara-Jaque, Ayaka Nakashima, Kengo Suzuki, Brian V Geisbrecht, Masaaki Tamura.(2021). Beta-1,3 Oligoglucans Specifically Bind to Immune Receptor CD28 and May Enhance T Cell Activation.
[6] Kumarkrishna Raychaudhuri, Rohita Rangu, Alison Ma, Neriah Alvinez, Andy D Tran, Sandeep Pallikkuth, Katherine M McIntire, Joseph A Garvey, Jason Yi, Lawrence E Samelson.(2024). CD28 shapes T cell receptor signaling by regulating Lck dynamics and ZAP70 activation.
[7] Jennifer A. Rohrs, Elizabeth L. Siegler, Pin Wang, Stacey D. Finley.(2020). ERK Activation in CAR T Cells Is Amplified by CD28-Mediated Increase in CD3ζ Phosphorylation.
[8] Anuja Bhatta, Marcia A Chan, Stephen H Benedict.(2021). Transcription factor activation and protein phosphorylation patterns are distinct for CD28 and ICAM-1 co-stimulatory molecules.
[9] Xuelian Xiang, Nan Cao, Feiyue Chen, Long Qian, Yifei Wang, Yunmao Huang, Yunbo Tian, Danning Xu, Wanyan Li.(2020). Polysaccharide of Atractylodes macrocephala Koidz (PAMK) Alleviates Cyclophosphamide-induced Immunosuppression in Mice by Upregulating CD28/IP3R/PLCγ-1/AP-1/NFAT Signal Pathway.
[10] Brian Tomkowicz, Eileen S. Walsh, Adam Cotty, Raluca Verona, Nina Chi-Sabins, Fred M. Kaplan, Sandy Santulli-Marotto, Chen-Ni Chin, Jill M. Mooney, Russell B. Lingham, Michael Naso, Timothy J. McCabe.(2015). TIM-3 Suppresses Anti-CD3/CD28-Induced TCR Activation and IL-2 Expression through the NFAT Signaling Pathway.
[11] Sadiye Amcaoglu Rieder, Jingya Wang, Natalie White, Ariful Qadri, Catherine Menard, Geoffrey Stephens, Jodi L Karnell, Christopher E Rudd, Roland Kolbeck.(2021). B7-H7 (HHLA2) inhibits T-cell activation and proliferation in the presence of TCR and CD28 signaling.
[12] Enfu Hui, Jeanne Cheung, Jing Zhu, Xiaolei Su, Marcus J Taylor, Heidi A Wallweber, Dibyendu K Sasmal, Jun Huang, Jeong M Kim, Ira Mellman, Ronald D Vale.(2017). T cell costimulatory receptor CD28 is a primary target for PD-1-mediated inhibition.
[13] G Aaron Holling, Colin A Chavel, Anand P Sharda, Mackenzie M Lieberman, Caitlin M James, Shivana M Lightman, Jason H Tong, Guanxi Qiao, Tiffany R Emmons, Thejaswini Giridharan, Shengqi Hou, Andrew M Intlekofer, Richard M Higashi, Teresa W M Fan, Andrew N Lane, Kevin H Eng, Brahm H Segal, Elizabeth A Repasky, Kelvin P Lee, Scott H Olejniczak.(2024). CD8+ T cell metabolic flexibility elicited by CD28-ARS2 axis-driven alternative splicing of PKM supports antitumor immunity.
[14] Marianne Strazza, Inbar Azoulay-Alfaguter, Bryan Dun, Jairo Baquero-Buitrago, Adam Mor.(2015). CD28 inhibits T cell adhesion by recruiting CAPRI to the plasma membrane.
[15] Masashi Watanabe, Ying Lü, Michael Breen, Richard J. Hodes.(2020). B7-CD28 co-stimulation modulates central tolerance via thymic clonal deletion and Treg generation through distinct mechanisms.
[16] Yinghao Zhao, Wei Yang, Yuanyuan Huang, Ranji Cui, Xiangyan Li, Bingjin Li.(2018). Evolving Roles for Targeting CTLA-4 in Cancer Immunotherapy.
[17] Shunsuke Fukuyo, Shingo Nakayamada, Shigeru Iwata, Satoshi Kubo, Kazuyoshi Saito, Yoshiya Tanaka.(2017). Abatacept therapy reduces CD28+CXCR5+ follicular helper-like T cells in patients with rheumatoid arthritis.
[18] Alice O Kamphorst, Andreas Wieland, Tahseen Nasti, Shu Yang, Ruan Zhang, Daniel L Barber, Bogumila T Konieczny, Candace Z Daugherty, Lydia Koenig, Ke Yu, Gabriel L Sica, Arlene H Sharpe, Gordon J Freeman, Bruce R Blazar, Laurence A Turka, Taofeek K Owonikoko, Rathi N Pillai, Suresh S Ramalingam, Koichi Araki, Rafi Ahmed.(2017). Rescue of exhausted CD8 T cells by PD-1-targeted therapies is CD28-dependent.
[19] Wei Huff, Marpe Bam, Jack Shireman, Jae Hyun Kwon, Leo Song, Sharlé Newman, Aaron Cohen‐Gadol, Scott Shapiro, Tamara Jones, Kelsey Fulton, Sheng Liu, Hiromi Tanaka, Yunlong Liu, Jun Wan, Mahua Dey.(2021). Aging- and Tumor-Mediated Increase in CD8+CD28− T Cells Might Impose a Strong Barrier to Success of Immunotherapy in Glioblastoma.
[20] Zhen Yang, Xinpeng Liu, Jun Zhu, Yangyang Chai, Boyi Cong, Bo Li, Wanfeng Gao, Ye Hu, Mingyue Wen, Yanfang Liu, Li Fu, Xuetao Cao.(2025). Inhibiting intracellular CD28 in cancer cells enhances antitumor immunity and overcomes anti-PD-1 resistance via targeting PD-L1.
[21] Ryan C Augustin, Riyue Bao, Jason J Luke.(2023). Targeting Cbl-b in cancer immunotherapy.
[22] Xuexiao Jin, Qin Xu, Chengfei Pu, Kaixiang Zhu, Cheng Lu, Yu Jiang, Lei Xiao, Yongmei Han, Linrong Lu.(2021). Therapeutic efficacy of anti-CD19 CAR-T cells in a mouse model of systemic lupus erythematosus.
[23] Ling Qin, Jing Xie, Zhifeng Qiu, Wei Cao, Yang Jiao, Jean‐Pierre Routy, Taisheng Li.(2016). Aging of immune system: immune signature from peripheral blood lymphocyte subsets in 1068 healthy adults.



