武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
靶向“隐藏靶点”ROR1:广谱肿瘤治疗迎来突破?
439 人阅读发布时间:2025-07-25 10:09
1. ROR1背景介绍
受体酪氨酸激酶样孤儿受体1(Receptor tyrosine kinase-like orphan receptor 1, ROR1)是一种跨膜糖蛋白,属于ROR家族,其结构包含胞外免疫球蛋白样结构域、富含半胱氨酸结构域(Frizzled 结构域)、Kringle结构域,以及胞内酪氨酸激酶结构域和脯氨酸/丝氨酸-苏氨酸富集区 [1]。
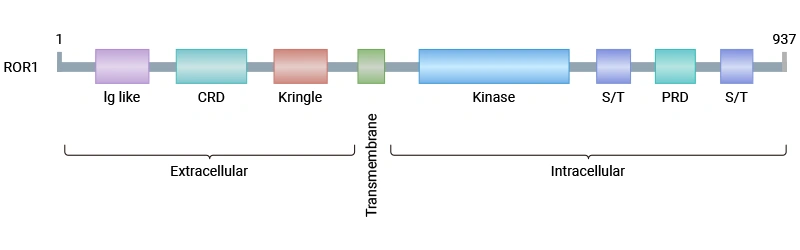
Figure 1. The structure of ROR1 protein with different domains
ROR1在胚胎发育中发挥重要作用,参与中枢神经、骨骼和心肺系统的发育 [2],但在正常成年组织中表达极低或缺失 [2,3]。这种 "癌胚抗原" 特性使其成为肿瘤靶向治疗的理想靶点:在多种血液肿瘤和实体瘤中,ROR1被重新激活并高表达,且与肿瘤增殖、侵袭、耐药及不良预后密切相关 [4-7]。
2. ROR1相关信号通路
ROR1的信号激活依赖配体结合,通过下游通路调控肿瘤生物学行为,主要包括以下途径:
2.1 Wnt5a-ROR1通路
Wnt5a是ROR1的经典配体,二者结合后激活非经典Wnt信号:
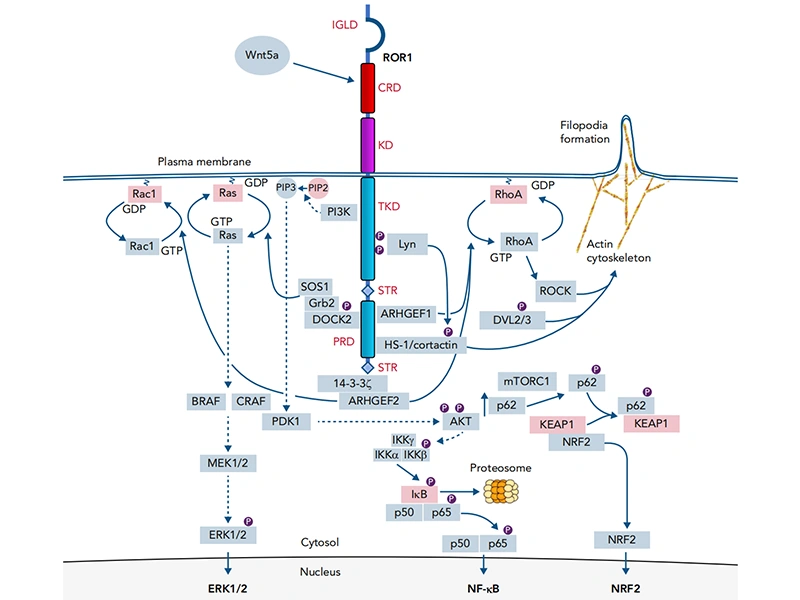
Figure 2. ROR1 signaling [1]
- 激活NF-κB通路:促进p62积累,抑制KEAP1对NRF2的降解,上调抗氧化基因,增强肿瘤细胞耐药性 [1];
- 激活PI3K/AKT/mTOR通路:通过AKT磷酸化促进细胞存活和增殖 [1];
- 激活ERK1/2和Rho/Rac GTPases:通过DOCK2、Grb2等分子激活Ras-MAPK通路,增强细胞迁移和侵袭 [1]。
2.2 IGFBP5-ROR1/HER2通路
在胶质母细胞瘤中,胰岛素样生长因子结合蛋白5(IGFBP5)作为ROR1的新型配体,与ROR1结合后促进其与HER2形成异二聚体,激活CREB转录因子,上调ETV5和FBXW9的表达,最终增强肿瘤干细胞的侵袭和致瘤性 [8]。
2.3 ROR1-STAT3通路
在卵巢癌中,ROR1通过激活AKT/ERK通路间接促进STAT3磷酸化,且ROR1与STAT3在肿瘤基质细胞(如癌相关成纤维细胞)中共表达,通过炎症反应和转录调控参与肿瘤异质性维持 [9]。
2.4 与其他通路的交叉调控
- 与BTK通路:套细胞淋巴瘤中,ROR1激活不依赖BCR/BTK通路,与BTK抑制剂联用可增强抗肿瘤效应 [10];
- 与BCL2通路:CLL中,ROR1通过上调BCL2L1(编码BCL-XL)降低Venetoclax敏感性,抗ROR1抗体可逆转该耐药 [6]。
3. ROR1相关疾病
ROR1的异常表达与多种恶性肿瘤相关,涵盖血液系统肿瘤和实体瘤:
3.1 血液系统肿瘤
3.1.1 慢性淋巴细胞白血病(CLL)
ROR1在CLL中呈现特异性高表达,90%以上患者的白血病细胞可检测到ROR1蛋白,且表达水平与疾病进展密切相关 [1,6]。ROR1通过结合配体Wnt5a激活多重信号通路:
- 抗凋亡通路:激活NF-κB并上调BCL2L1(编码BCL-XL),直接导致对BCL2抑制剂venetoclax的耐药 [6];
- 增殖与存活:通过PI3K/AKT/mTOR通路增强细胞存活信号,同时激活ERK1/2促进细胞增殖 [1];
- 微环境交互:信号诱导CLL细胞分泌IL-6等细胞因子,通过自分泌STAT3激活形成促癌循环 [1]。
临床研究显示,高ROR1表达的CLL患者治疗-free生存期(TFS)显著缩短,且对ibrutinib等BTK抑制剂的敏感性降低 [1]。
3.1.2 套细胞淋巴瘤(MCL)
MCL细胞普遍高表达ROR1,其信号通路与B细胞受体(BCR)-BTK通路存在交叉但独立的调控关系 [10]。包括:
- 耐药机制:通过激活Rac1和ERK1/2通路促进细胞增殖,该过程不依赖BCR信号,是BTK抑制剂耐药的重要原因 [10];
- 协同靶向效应:在TP53突变的MCL模型中,ROR1单抗(zilovertamab)与BTK抑制剂联用可显著增强细胞毒性,通过双重阻断NF-κB和MAPK通路诱导凋亡 [10]。
ROR1在MCL细胞中普遍表达,与BTK抑制剂耐药相关,双靶向ROR1和BTK可增强杀伤效果 [10];
3.1.3 非霍奇金淋巴瘤
DLBCL、FL等亚型中ROR1转录本高表达,是潜在治疗靶点 [4]。
- 弥漫性大B细胞淋巴瘤(DLBCL)和滤泡性淋巴瘤(FL):原位杂交(ISH)显示,DLBCL和FL患者的ROR1转录本阳性率分别达60%和55%,ROR1靶向T细胞衔接器(TCE)可通过激活T细胞特异性杀伤肿瘤细胞 [4];
- Richter综合征:由CLL转化的DLBCL中,ROR1高表达通过激活PI3K/AKT通路增强肿瘤侵袭性,抗体-药物偶联物(ADC)如VLS-101可特异性递送毒素至ROR1+细胞 [1]。
3.2 实体瘤
3.2.1 胶质母细胞瘤(GBM)
ROR1在GBM中的表达与肿瘤分级正相关,高级别GBM患者的ROR1 mRNA水平是低级别胶质瘤的3.2倍 [5,7]。关键机制包括:
- 侵袭与转移:IGFBP5作为ROR1的新型配体,通过结合ROR1促进其与HER2形成异二聚体,激活CREB转录因子,上调ETV5和FBXW9以增强肿瘤干细胞侵袭能力 [8];
- 预后关联:高ROR1表达的GBM患者中位生存期仅16个月,显著低于低表达者(70个月),且与肿瘤复发率升高相关 [7]。
3.2.2 肺癌、乳腺癌、肝癌
ROR1在这些肿瘤中高表达,抗ROR1人源化抗体(h1B8、h6D4)可抑制肿瘤生长 [8];
- 肺癌:肺腺癌中ROR1通过激活PI3K/AKT通路促进细胞增殖,抗ROR1人源化抗体h1B8和h6D4可通过阻断该通路抑制肿瘤生长 [11];
- 乳腺癌:三阴性乳腺癌(TNBC)中ROR1与EGFR共表达,通过激活ERK1/2增强转移能力,h6D4抗体可显著减少肺转移灶形成 [11];
- 肝癌:肝细胞癌(HCC)中ROR1通过Wnt5a依赖的方式激活β-catenin通路,h1B8抗体可下调cyclin D1表达抑制细胞周期进展 [11]。
3.2.3 卵巢癌
高级别浆液性卵巢癌(HGSOC)中,ROR1在新辅助化疗(NACT)后表达显著上调,与肿瘤异质性增强相关 [9]。ROR1在癌相关成纤维细胞(CAFs)中高表达,通过AKT/ERK激活STAT3,促进IL-6和TGF-β分泌,形成促转移微环境;ROR1+CAFs通过分泌Wnt5b促进上皮-间质转化(EMT),降低铂类药物敏感性 [9]。
3.2.4 妇科癌症
宫颈癌、子宫内膜癌等妇科肿瘤中,ROR1高表达率达45%-60%。机制研究显示,ROR1通过激活Wnt5a/PI3K通路上调cyclin E1,加速细胞周期进程;ROR1与整合素β1共定位,增强肿瘤细胞与extracellular基质的黏附,促进局部浸润 [4]。
3.3 其他恶性肿瘤
3.3.1 胰腺癌
胰腺导管腺癌(PDAC)中,ROR1在肿瘤干细胞中特异性高表达,通过激活Notch通路维持干细胞特性 [2]。小分子抑制剂KAN0439834可靶向ROR1酪氨酸激酶结构域,抑制其下游AKT磷酸化,在PDX模型中使肿瘤体积缩小58%[2]。
3.3.2 黑色素瘤
ROR1通过非经典Wnt通路激活RhoA/ROCK信号,增强细胞迁移能力 [1]。临床样本显示,ROR1高表达的黑色素瘤患者远处转移率是低表达者的2.3倍,且与BRAF抑制剂耐药相关 [1]。
4. ROR1靶点药物最近研究进展
目前,有多条以ROR1为靶点的药物管线在研,主要药物类型为ADC、自体CAR-T、单抗等;适应症覆盖血液瘤和实体瘤(肺癌、乳腺癌、淋巴瘤等),多款药物已进入后期临床验证阶段,凸显ROR1作为广谱肿瘤靶点具有极大的潜力。部分在研管线列举如下:
| 药物 | 作用机制 | 在研适应症(疾病名) | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|
| Zilovertamab | ROR1拮抗剂 | 套细胞淋巴瘤 | 慢性淋巴细胞白血病 | 边缘区B细胞淋巴瘤 | 小淋巴细胞淋巴瘤 | 去势抵抗性前列腺癌 | 局部晚期不能切除的乳腺癌 | University of California San Diego | Oncternal Therapeutics, Inc. | University of California | 临床3期 |
| Zilovertamab vedotin | ROR1拮抗剂 | 微管蛋白抑制剂 | 弥漫性大B细胞淋巴瘤 | 复发性弥漫性大B细胞淋巴瘤 | 侵袭性 B 细胞非霍奇金淋巴瘤 | B细胞恶性肿瘤等 | Merck Sharp & Dohme Corp. | Merck Sharp & Dohme LLC | 默沙东研发(中国)有限公司 | Merck & Co., Inc. | 临床3期 |
| B-013 | ROR1拮抗剂 | 三阴性乳腺癌 | 输卵管癌 | 铂耐药性卵巢癌 | 铂类耐药性原发性腹膜癌 | 铂耐药性输卵管癌 | 肿瘤等 | 上海上药交联医药科技有限公司 | 上海医药集团股份有限公司 | 临床2/3期 |
| HDM-2005 | ROR1调节剂 | 微管蛋白抑制剂 | 弥漫性大B细胞淋巴瘤 | 血液肿瘤 | 难治性淋巴瘤 | 晚期恶性实体瘤 | 晚期癌症 | 杭州中美华东制药有限公司 | 临床1/2期 |
| GNC-035四特异性抗体(百利药业) | 4-1BB激动剂 | CD3抑制剂 | PDL1抑制剂 | ROR1拮抗剂 | 难治性非霍奇金淋巴瘤 | 慢性淋巴细胞白血病 | 急性淋巴细胞白血病 | 急性髓性白血病 | 弥漫性大B细胞淋巴瘤等 | 四川百利药业有限责任公司 | Systimmune, Inc. | 临床1/2期 |
| LCB-71 | ROR1拮抗剂 | 急性淋巴细胞白血病 | 套细胞淋巴瘤 | 非小细胞肺癌 | 三阴性乳腺癌 | 晚期淋巴瘤 | 晚期恶性实体瘤等 | 无锡药明合联生物技术有限公司 | 基石药业 | 基石药业(苏州)有限公司 | LigaChem Biosciences, Inc. | ABL Bio, Inc. | 临床1期 |
| IM-1021 | ROR1拮抗剂 | T_O_P_1_抑制剂 | 晚期癌症 | 里氏综合症 | 小淋巴细胞淋巴瘤 | 晚期恶性实体瘤 | Immunome, Inc. | 临床1期 |
| ROR1-TILs(Guangdong Zhaotai InVivo Biomedicine) | HPK1抑制剂 | PD-1抑制剂 | ROR1拮抗剂 | 免疫细胞毒性 | 淋巴细胞替代物 | 晚期恶性实体瘤 | 脑癌 | 乳腺癌 | 结直肠癌 | 肝癌 | 肺癌 | 广东昭泰体内生物医药科技有限公司 | 临床1期 |
| JCAR-024 | ROR1调节剂 | 血液肿瘤 | 中美上海施贵宝制药有限公司 | 临床1期 |
| TQB2101 | ROR1调节剂 | 血液肿瘤 | 晚期癌症 | 乳腺癌 | 结直肠癌 | 肺癌 | 正大天晴药业集团股份有限公司 | 正大天晴药业集团南京顺欣制药有限公司 | 临床1期 |
| PRGN 3007 | ROR1拮抗剂 | Gene transference | T淋巴细胞替代物 | 急性淋巴细胞白血病 | 慢性淋巴细胞白血病 | 弥漫性大B细胞淋巴瘤 | 套细胞淋巴瘤 | 三阴性乳腺癌 | 血液肿瘤 | 实体瘤 | Precigen, Inc. | Precigen ActoBio, Inc. | 临床1期 |
| BR-111 | ROR1拮抗剂 | 晚期癌症 | 晚期恶性实体瘤 | B细胞淋巴瘤 | 血液肿瘤 | 实体瘤 | 浙江博锐生物制药有限公司 | Bioray, Inc. | 临床1期 |
| ROR1R-CAR(The University of Texas MD Anderson Cancer Center) | ROR1调节剂 | Gene transference | T淋巴细胞替代物 | 白血病 | The University of Texas MD Anderson Cancer Center | CLL Global Research Foundation | 临床1期 |
| EMB-07 | CD3刺激剂 | ROR1拮抗剂 | 子宫癌 | 肺腺癌 | 膀胱癌 | 慢性淋巴细胞白血病 | 结直肠癌 | 子宫内膜癌等 | 岸迈生物科技(苏州)有限公司 | 上海岸迈生物科技有限公司 | 临床1期 |
| ROR1-CAR-TILs(Guangdong Zhaotai InVivo Biomedicine) | HPK1抑制剂 | PD-1抑制剂 | ROR1拮抗剂 | 免疫细胞毒性 | 淋巴细胞替代物 | 晚期恶性实体瘤 | 脑癌 | 乳腺癌 | 结直肠癌 | 肝癌 | 肺癌 | 广东昭泰体内生物医药科技有限公司 | 临床1期 |
| SYS-6005 | ROR1拮抗剂 | 晚期癌症 | 晚期恶性实体瘤 | 慢性淋巴细胞白血病 | 血液肿瘤 | 实体瘤 | 石药集团巨石生物制药有限公司 | Radiance Biopharma, Inc. | 临床1期 |
| NVG-111 | CD3刺激剂 | ROR1调节剂 | 慢性淋巴细胞白血病 | 弥漫性大B细胞淋巴瘤 | 滤泡性淋巴瘤 | 套细胞淋巴瘤 | 黑色素瘤等 | Novalgen Ltd. | 临床1期 |
| PBA-0405 | ROR1拮抗剂 | 脑癌 | 软组织肉瘤 | 头颈部鳞状细胞癌 | 三阴性乳腺癌 | Presage Biosciences, Inc. | Pure Biologics SA | 早期临床1期 |
5. 华美生物ROR1相关产品推荐
● ROR1重组蛋白
Recombinant Human Inactive tyrosine-protein kinase transmembrane receptor ROR1 (ROR1), partial (Active); CSB-MP020067HU1d7
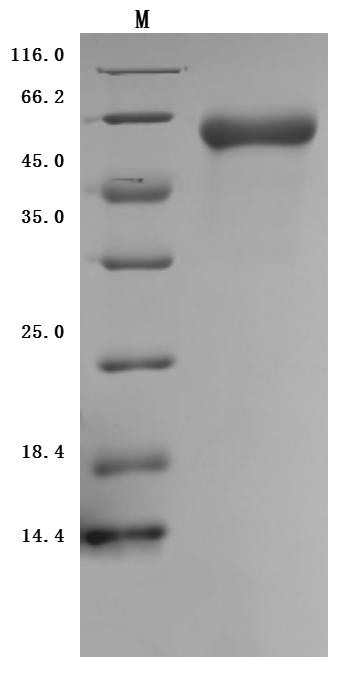
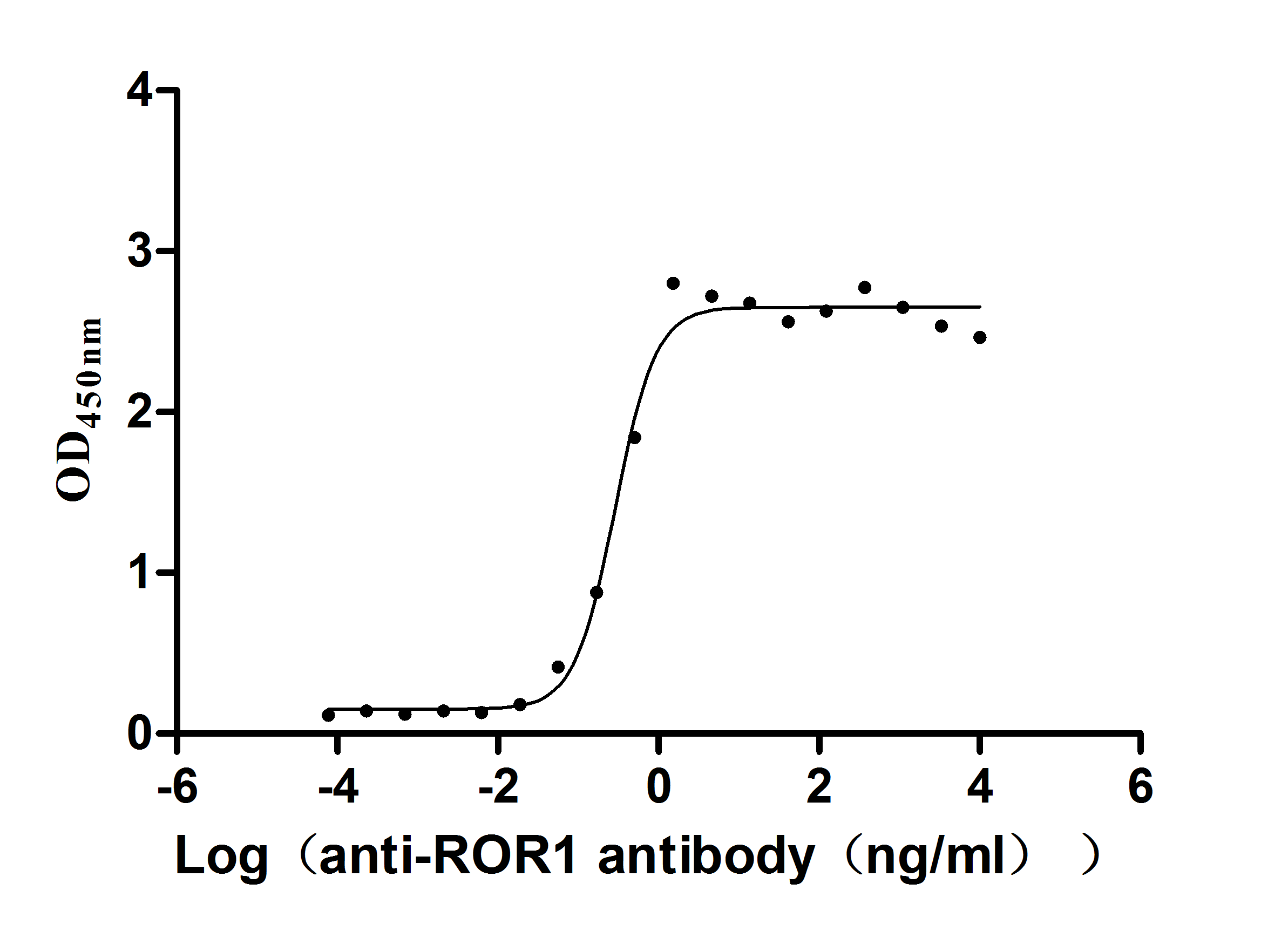
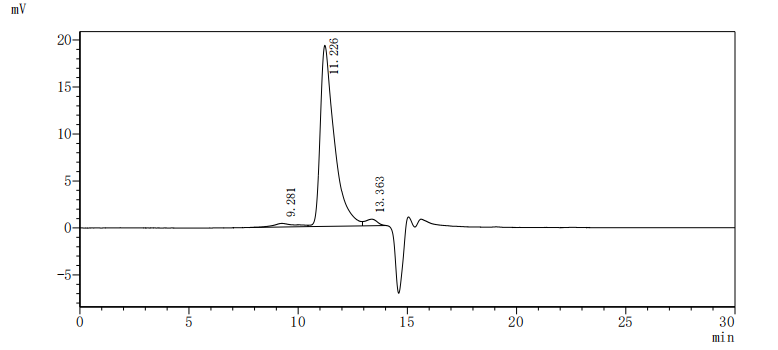
Recombinant Mouse Inactive tyrosine-protein kinase transmembrane receptor ROR1 (Ror1), partial (Active); CSB-MP4008MO
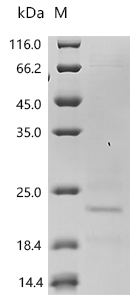
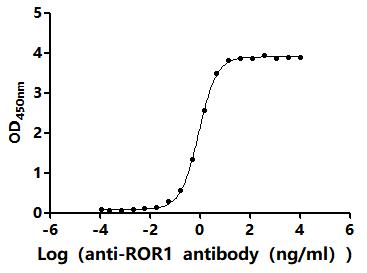
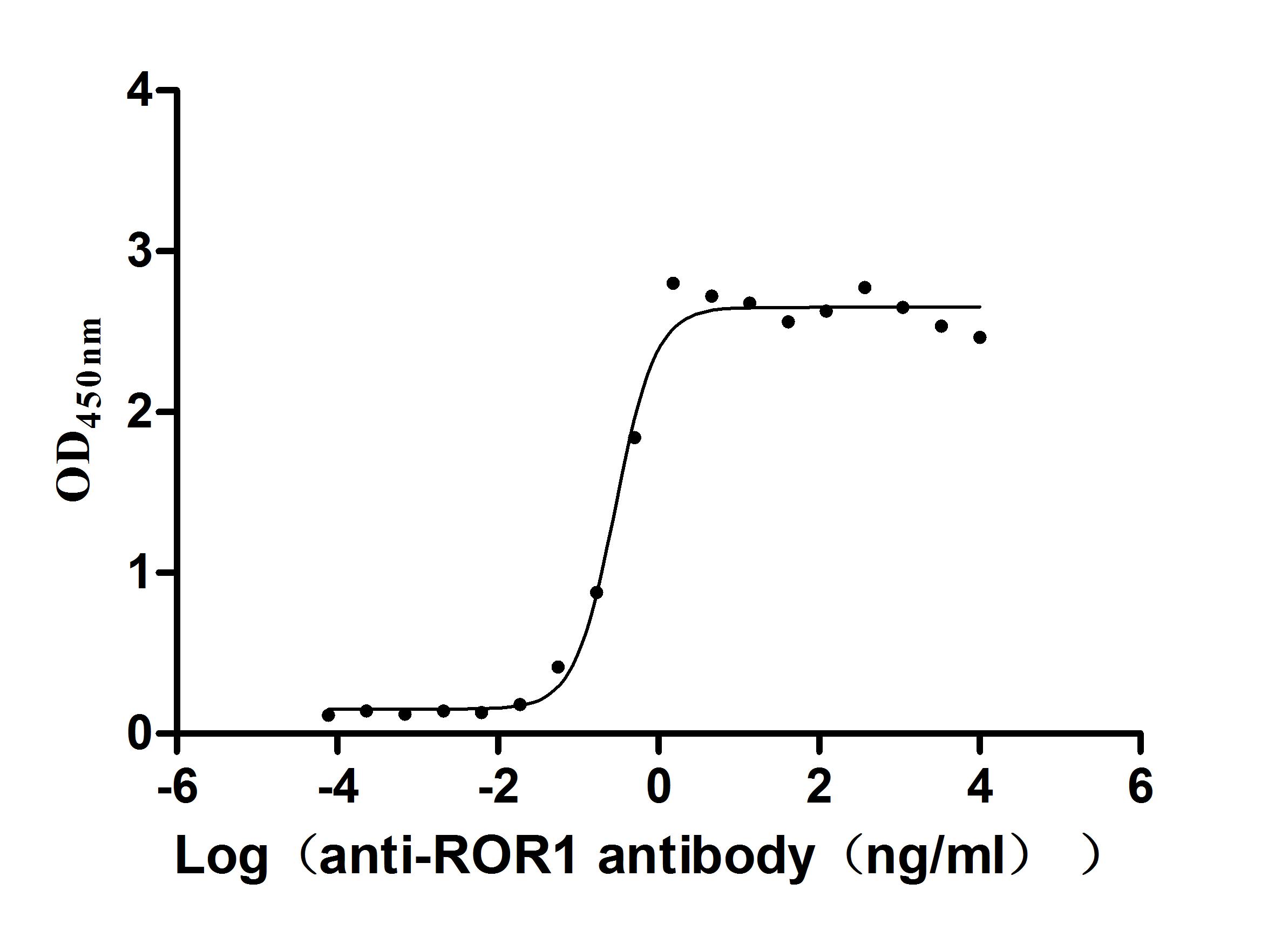
● ROR1抗体
ROR1 Recombinant Monoclonal Antibody; CSB-RA020067A1HU
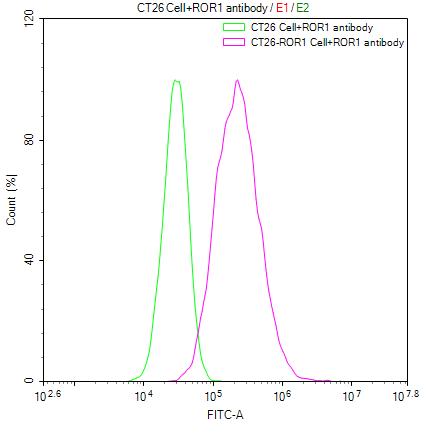
● ROR1 稳转细胞株
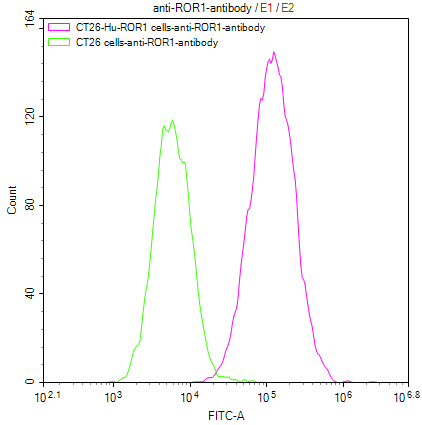
CT26/Human ROR1 Stable Cell Line; CSB-SC020067HU
参考文献:
[1] Kipps T J. ROR1: an orphan becomes apparent[J]. Blood, 2022, 140(14): 1583-1591.
[2] Mellstedt H, Hojjat-Farsangi M, Daneshmanesh A H, et al. First generation of a small chemical molecule ROR1 RTK tyrosine kinase inhibitor[J]. Annals of Oncology, 2016, 27(Supplement 6): vi526-vi544.
[3] Anonymous. Antibody-drug conjugates for cancer score with ROR1[J]. Nature Biotechnology, 2021, 39(1): 3-12.
[4] Snell D, Kirk N, Bassler N, et al. An assessment of ROR1 expression across tumor tissue and the investigation of a ROR1-targeted T cell engager as a therapeutic strategy to target ROR1 positive tumors[J]. J Immunother Cancer, 2023, 11(Suppl 1): A1-A1731.
[5] Madani D, John M, Satgunaseelan L, et al. ROR1 mRNA expression in glioma - a novel prognostic biomarker[J]. Neuro-Oncology, 2022, 24(Supplement 7): vii6.
[6] Ghia E M, Rassenti L Z, Choi M Y, et al. High expression level of ROR1 and ROR1-signaling associates with venetoclax resistance in chronic lymphocytic leukemia[J]. Leukemia, 2022, 36(6): 1609-1618.
[7] Madani D, Satgunaseelan L, El-Hayek J, et al. ROR1 mRNA expression in glioma - a novel prognostic biomarker[J]. Neuro-Oncology, 2024, 26(Supplement 7): vii4-vii5.
[8] Lin W, Niu R, Park S M, et al. IGFBP5 is an ROR1 ligand promoting glioblastoma invasion via ROR1/HER2-CREB signaling axis[J]. Nature Communications, 2023, 14(1): 1578.
[9] Piki E, Dini A, Raivola J, et al. ROR1-STAT3 signaling contributes to ovarian cancer intra-tumor heterogeneity[J]. Cell Death Discovery, 2023, 9(1): 222.
[10] Nie L, Jiang V C Y, Liu Y, et al. Dual Targeting of ROR1 and BTK Augments the Anti-Lymphoma Activity in Mantle[J]. Blood, 2023, 142(Supplement 1): 4366-4367.
[11] Wei R, Liao X, Li J, et al. Novel humanized monoclonal antibodies against ROR1 for cancer therapy[J]. Molecular Cancer, 2024, 23(1): 165.



