武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
解码Siglec家族:关键成员、作用机制与实验研究策略
47 人阅读发布时间:2026-04-30 09:14
在免疫学研究的宏大版图中,糖生物学(Glycobiology)曾一度被视为“暗物质”——复杂且难以捉摸。然而,随着肿瘤免疫治疗进入瓶颈期,研究者们开始意识到,细胞表面那层被称为“糖萼(Glycocalyx)”的结构,并非仅仅是物理屏障,而是蕴含着极其精密的免疫调控逻辑。其中,Siglec(唾液酸结合免疫球蛋白样凝集素)家族凭借其对唾液酸(Sialic acid)信号的精准解码能力,正迅速成为继 PD-1/PD-L1 之后,免疫检查点研究领域的又一个核心焦点。
对于试图在这一领域寻找突破口的研究者而言,Siglec 家族既带来了希望,也充满了挑战。面对 15 个成员、复杂的配体环境以及高度动态的表达模式,如何快速判断研究优先级?如何根据特定的生物学场景选择最合适的靶点?这不仅需要对该家族有深入的结构生物学认知,更需要一套基于转化医学逻辑的“研究决策模型”。
Siglec 家族的崛起并非偶然,而是伴随着人类对肿瘤免疫逃逸机制理解的深化而发生的。在健康的组织中,细胞表面的唾液酸化修饰是“自我”状态的标签,免疫细胞通过其表面的抑制性 Siglec 受体识别这些信号,维持免疫耐受,防止自身免疫反应的发生。然而,在肿瘤微环境(TME)中,癌细胞通过代谢重编程诱导了“超唾液酸化(Hypersialylation)”,这相当于为自己披上了一层厚厚的“糖盾牌”,通过强行激活免疫细胞表面的抑制性 Siglec 信号,终止了免疫系统的攻击 [1]。
这种基于糖链识别的免疫抑制机制,与传统的蛋白-蛋白相互作用(如 PD-L1 识别 PD-1)具有本质的区别。它不仅涉及蛋白的表达水平,更涉及糖基化酶的动力学、糖链的构型以及空间位阻等多个维度。当前的研究已清晰地指向一个核心主题:Siglec 家族是髓系免疫调控(Myeloid immunoregulation)的核心枢纽,也是突破肿瘤免疫耐受的关键切口。
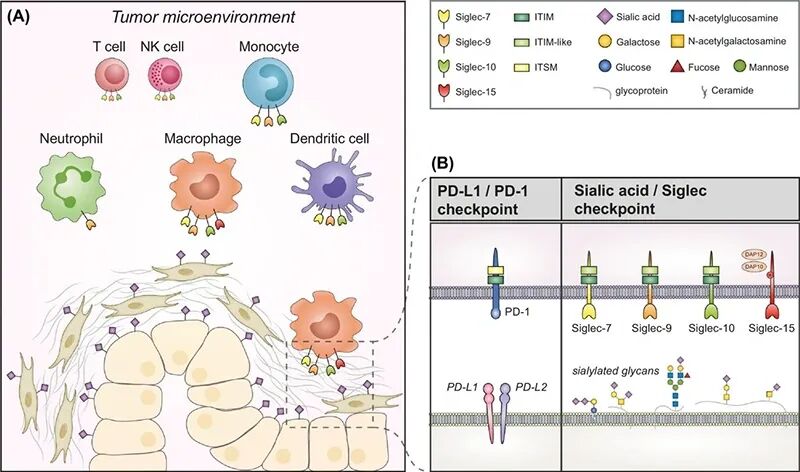
图 肿瘤微环境中的唾液酸-Siglec免疫检查点 [2]
((A) TME中Siglec-7/9/10/15及其唾液酸配体的表达示意图。 (B) PD-1/PD-L1检查点与唾液酸-Siglec检查点的机制对比。)
要深入研究 Siglec,首先必须理解其独特的分子架构。Siglec 属于 I 型跨膜蛋白,是免疫球蛋白超家族(IgSF)的成员。其胞外区由不同数量的 Ig 样结构域组成,最末端(N 端)是一个特征性的 V-set 结构域,这是所有 Siglec 成员识别配体的物理核心。
在 V-set 结构域内部,存在一个高度保守的精氨酸(Arginine)残基。这个残基在空间结构上形成了一个带正电荷的“口袋”,能够与唾液酸分子的羧基形成关键的盐桥。正是这种分子尺度的精密耦合,决定了 Siglec 对含唾液酸聚糖(Sialoglycans)的特异性结合 [3]。紧随 V-set 结构域之后的是不同数量的 C2-set 结构域,它们像“支架”一样将识别端推向细胞外空间,结构域的数量直接影响了受体在细胞表面的“触及范围”和柔韧性。
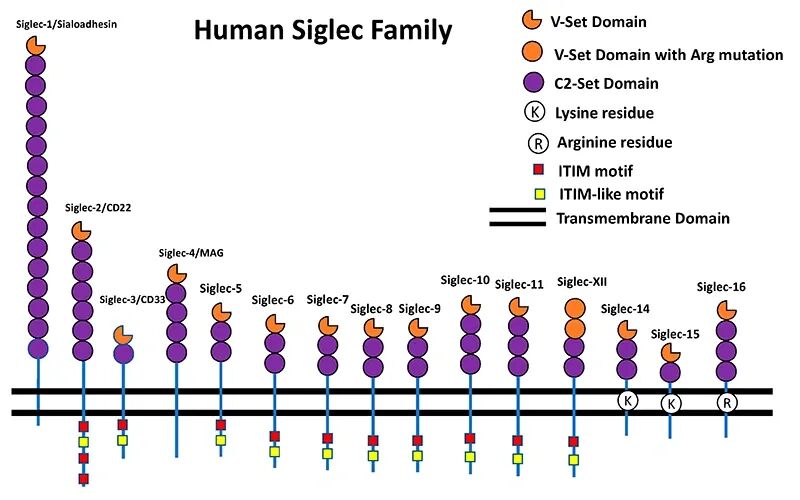
图 人类Siglec家族受体结构示意图 [4]
人类 Siglec 家族一共包括15个成员,从进化和结构特征来看,主要分为两大亚群 [5]:
进化保守型(Conserved Siglecs)
成员包括:Siglec-1(CD169)、Siglec-2(CD22)、Siglec-4(MAG)、Siglec-15
这类成员在物种间高度同源,承担基础性生理功能。例如,Siglec-1 凭借多达 16 个 C2-set 结构域,可在巨噬细胞表面实现长距离抗原捕获;Siglec-15 则因结构与 PD-L1 相似,且在肿瘤免疫中具备独特的双向调节潜力而备受关注。
CD33 相关型(CD33-related Siglecs)
成员包括:Siglec-3(CD33)、Siglec-5、Siglec-6、Siglec-7、Siglec-8、Siglec-9、Siglec-10、Siglec-11、Siglec-XⅡ、Siglec-14、Siglec-16
这类成员进化速率较快,因此也叫作快速进化型。主要分布于髓系细胞(中性粒细胞、单核细胞、巨噬细胞)。其胞内段通常含有免疫受体酪氨酸抑制基序(ITIM)或 ITIM 样基序,配体结合后通过招募磷酸酶 SHP-1/2 传递抑制信号,从而发挥“免疫刹车”作用。
值得注意的是,部分成员如 Siglec-14 和 Siglec-15,其跨膜区含有带正电荷的氨基酸,能与含有免疫受体酪氨酸激活基序(ITAM)的接头蛋白(如 DAP12)相互作用。这一结构特征在经典免疫学框架中通常与激活信号传导相关联。然而,高通量功能筛选研究显示,Siglec-15 在依赖 DAP12 表达的同时,却表现出对 T 细胞活性的持续抑制作用 [6]。这种抑制性与激活信号的交织与语境依赖性,使得 Siglec 家族在免疫调节中展现出超越传统二元分类的复杂性。
肿瘤免疫逃逸机制的复杂性在于其多层次的抑制网络,研究决策需从宏观维度出发,筛选具有战略互补性的Siglec靶点。当前证据表明,唾液酸-Siglec轴通过不同分子在特定免疫细胞亚群上的特异性表达,构建了分工明确的免疫抑制体系。基于此,研究可以聚焦于以下三个核心方向:
突破T/NK细胞功能耗竭的“隐形枷锁”
针对效应细胞功能受阻的逃逸策略,Siglec-9与Siglec-7构成了关键研究靶点。确凿的实验证据显示,肿瘤细胞表面高度唾液酸化的粘蛋白(如MUC1)作为配体,能够特异性结合NK细胞上的Siglec-7以及T细胞和髓系细胞上的Siglec-9。这种结合触发其胞内ITIM结构域介导的抑制性信号级联反应,直接导致NK细胞的杀伤活力受损及T细胞的细胞毒性功能受阻 [7]。因此,该方向的核心逻辑在于验证阻断这一交互能否解除效应细胞的抑制状态,恢复免疫系统对肿瘤的“免疫巡逻”功能。
逆转巨噬细胞的“别吃我”信号
针对先天免疫逃逸机制,Siglec-10作为核心调控分子展现出重要价值。大量研究证实,肿瘤细胞表面高表达的CD24作为“抗吞噬”信号,通过与巨噬细胞上的Siglec-10结合,招募并激活胞内SHP-1/2磷酸酶,从而传递强效的抑制信号,阻断巨噬细胞的吞噬作用 [8]。这一机制在乳腺癌和卵巢癌等实体瘤中尤为显著。因此,将Siglec-10纳入研究靶点,旨在探索通过阻断CD24-Siglec-10轴来重编程肿瘤相关巨噬细胞(TAMs),恢复其吞噬能力的可行性。
独立于 PD-L1 的全新赛道
针对免疫检查点的代偿与耐药机制,Siglec-15开辟了独立于经典PD-1轴的全新赛道。关键的空间转录组学数据揭示,Siglec-15在多种肿瘤组织(如非小细胞肺癌、膀胱癌)中呈现特异性高表达,且其空间分布与PD-L1表现出显著的互斥性。这意味着在PD-L1阴性的“免疫冷肿瘤”中,Siglec-15可能通过其独特的DAP12接头蛋白依赖但输出抑制性信号的特征,独立介导免疫逃逸。因此,将其作为独立方向研究,有助于覆盖PD-L1阴性患者群体,并解析非PD-1依赖的免疫抑制重塑机制。
在明确了Siglec家族在肿瘤免疫微环境中的差异化定位与战略分工后,研究的逻辑必须从宏观的靶点筛选深入到具体的细胞内信号机制层面。髓系细胞(包括肿瘤相关巨噬细胞TAMs和髓系来源的抑制细胞MDSCs)作为Siglec家族最主要的表达载体和功能执行者,其内部的信号转导博弈直接决定了免疫抑制的最终效能。因此,Step 2的核心在于解析髓系细胞内部,Siglec受体如何通过特定的信号通路传导抑制性信号,从而重塑细胞功能状态。
机制焦点:髓系细胞内Siglec介导的信号转导与功能重塑
尽管在Step 1中确立了Siglec-9、-10、-15等靶点的宏观价值,但这些受体在髓系细胞表面识别唾液酸化配体后,其胞内段如何通过特定的接头蛋白(如DAP12、SHP-1/2)激活下游信号级联反应,进而精确调控细胞的极化状态、吞噬功能或抑制性细胞因子的分泌,是决定治疗成败的关键所在。
例如,Siglec-15虽依赖DAP12接头蛋白,却表现出抑制性功能,这种独特的信号转导特征如何在髓系细胞内部实现免疫抑制?再如,Siglec-10与CD24结合后,SHP-1/2的激活如何具体阻断吞噬突触的形成?这些问题指向了一个更深层次的科学问题:在复杂的髓系细胞信号网络中,Siglec轴如何通过分子层面的博弈,最终决定免疫微环境的走向。因此,Step 2的研究决策应聚焦于此,旨在揭示髓系细胞内部的信号转导机制,为开发精准的干预策略提供直接的理论依据。
如果您的研究并不局限于肿瘤,而是希望在特定的组织场景或病理过程中寻找具有潜力的差异化靶点,那么以下成员提供了极具吸引力的研究切口:
神经免疫与阿尔茨海默病:CD33 的核心地位
在大脑这个特殊的免疫环境中,小胶质细胞(Microglia)的吞噬能力决定了 Aβ 淀粉样蛋白的清除效率。CD33 在小胶质细胞上的高表达已被证实会抑制这种吞噬作用,从而增加阿尔茨海默病(AD)的风险 [9]。与之相对应的 TREM2 则是激活信号。CD33 与 TREM2 之间的拮抗平衡,构成了当前神经免疫研究中最具转化潜力的研究方向之一。
嗜酸性粒细胞与过敏性炎症:Siglec-8 的精准打击
Siglec-8 的表达具有极高的组织特异性——它仅表达在嗜酸性粒细胞、肥大细胞和嗜碱性粒细胞上。在过敏性哮喘、慢性荨麻疹等疾病中,激活 Siglec-8 能直接诱导嗜酸性粒细胞凋亡并抑制肥大细胞脱颗粒 [10]。近期的临床研究进一步证实,靶向 Siglec-8 的抗体在治疗嗜酸性胃炎和十二指肠炎中展现出显著疗效,能有效耗竭胃肠道病灶部位的嗜酸性粒细胞 [11]。这使其成为炎症研究中极少数具有“组织精准性”和临床转化潜力的靶点。
B 细胞稳态:CD22 (Siglec-2) 的经典与新知
CD22 是 B 细胞信号传导的负调节因子,它通过识别顺式(cis)分布的唾液酸配体来调节 B 细胞受体(BCR)的激活阈值。在自身免疫性疾病或 B 细胞恶性肿瘤中,CD22 不仅仅是检测靶标,更是研究受体“掩蔽效应”与配体竞争的最佳模型[12-13]。
在 Siglec 研究中,最容易导致研究结论偏差的地方在于忽略了其独特的配体生物学特性。这是将 Siglec 研究从“表象描述”提升到“机制解析”的关键。
顺式掩蔽效应(Cis-masking)
大多数 Siglec 在静息状态下,会被细胞膜表面的唾液酸配体所结合(掩蔽)。研究证实,这种内源性配体以极高的局部浓度占据受体,导致外源性探针无法结合 [14]。这意味着,即便流式数据显示受体高表达,它们也可能处于功能沉默状态。在设计实验时,若不使用唾液酸酶(Sialidase)去除这种掩蔽,您所观察到的受体结合能力可能仅仅是冰山一角。
配体特异性的精细差异
Siglec 对唾液酸的识别极其挑剔,不仅区分 α2,3-、α2,6- 连接方式,还高度依赖于深层的聚糖骨架甚至载体蛋白的序列背景。最近的研究证实,硫酸化修饰(如 CHST1 介导的修饰)和特定的 O-聚糖模式是决定 Siglec-3/7/8 等成员结合的关键开关 [15]。CD22 与 Siglec-8 的配体偏好截然不同,仅依赖总唾液酸定量或泛特异性探针,极易导致结论偏差;必须深入至聚糖结构的单一位点及蛋白质背景分析。
物种差异与直系同源物的局限性
这是进行体内实验时最令人头疼的问题。CD33相关Siglecs属于免疫系统中演化速度极快的基因簇,这种快速演化往往源于宿主与病原体之间持续的选择压力,导致不同物种的Siglecs在基因序列和功能上产生了巨大的分歧 [16]。特别值得注意的是,人类在唾液酸生物学上存在特异性事件——丢失了唾液酸Neu5Gc,这直接重塑了人类Siglec的配体识别谱。这意味着小鼠模型中的Siglec-F或Siglec-E,往往无法真实模拟人类Siglec-8或Siglec-9在人体内的实际生物学功能。研究者须进一步评估小鼠模型所得结论向临床转化的可靠性。
当您确定了研究的 Siglec 成员和应用场景后,接下来的挑战是选择能够支撑高质量数据的实验工具。研究工具的选择应直接回馈您的实验问题:
如果您的问题是“受体能否识别特定的聚糖配体”:您需要具有生物活性的重组蛋白(如 Fc 融合蛋白或构象稳定的 His 标签蛋白)。这种工具是 SPR(表面等离子共振)或配体结合实验的基石,能帮助您捕捉到真实的结合信号,而非非特异性吸附。
如果您的问题是“阻断该轴能否逆转免疫抑制”:此时,高特异性的功能性抗体是核心。您需要关注抗体是否能精准靶向 V-set 结构域中的关键结合位点(如精氨酸口袋),并验证其在体外功能实验(如 T 细胞共培养、巨噬细胞吞噬实验)中的中和或激活能力。
如果您的问题是“该受体在样本中的定量分析”:那么高灵敏度的 ELISA 试剂盒则是优选。经过严格种属特异性验证的试剂盒,能够精准检测血清、细胞上清或组织裂解液中的 Siglec 水平,为您提供可靠的定量数据,避免交叉反应的干扰。
为了助您精准应对上述科研挑战,华美生物精心准备了一套覆盖重组蛋白、抗体、ELISA试剂盒的全维度Siglec研究工具箱,旨在为您提供从机制探索到功能验证的一站式支持。
● 重组蛋白
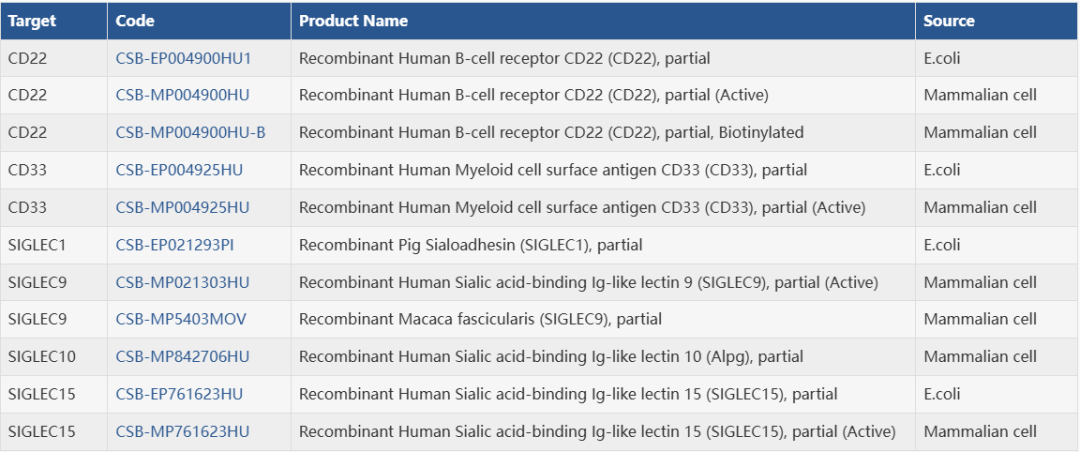
● 抗体
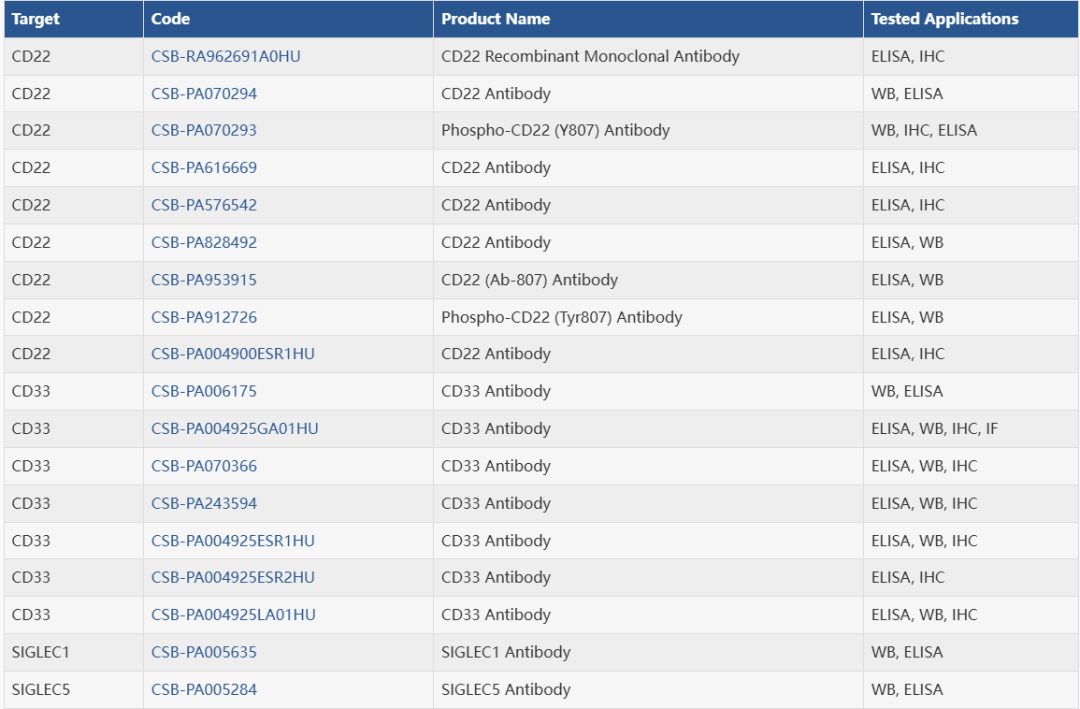
● ELISA试剂盒

[1] Feng H,Feng J,Han X, et al. The Potential of Siglecs and Sialic Acids as Biomarkers and Therapeutic Targets in Tumor Immunotherapy. Cancers (Basel). 2024;16 (2):.
[2] Boelaars K,van Kooyk Y. Targeting myeloid cells for cancer immunotherapy: Siglec-7/9/10/15 and their ligands. Trends Cancer. 2024;10 (3):230-241.
[3] Jame-Chenarboo Z,Gray TE,Macauley MS. Advances in understanding and exploiting Siglec-glycan interactions. Curr Opin Chem Biol. 2024;80:102454.
[4] Siddiqui SS,Matar R,Merheb M, et al. Siglecs in Brain Function and Neurological Disorders. Cells. 2019;8 (10):.
[5] Lin SY,Schmidt EN,Takahashi-Yamashiro K, et al. Roles for Siglec-glycan interactions in regulating immune cells. Semin Immunol. 2025;77:101925.
[6] Wang J,Sun J,Liu LN, et al. Siglec-15 as an immune suppressor and potential target for normalization cancer immunotherapy. Nat Med. 2019;25 (4):656-666.
[7] Rodriguez E,Boelaars K,Brown K, et al. Sialic acids in pancreatic cancer cells drive tumour-associated macrophage differentiation via the Siglec receptors Siglec-7 and Siglec-9. Nat Commun. 2021;12 (1):1270.
[8] Barkal AA,Brewer RE,Markovic M, et al. CD24 signalling through macrophage Siglec-10 is a target for cancer immunotherapy. Nature. 2019;572 (7769):392-396.
[9] Akinluyi ET,Akinluyi ET,Takahashi-Yamashiro K, et al. Interplay between CD33 and TREM2 in Alzheimer's Disease: Potential Mechanistic Insights into Microglial Function in Amyloid Pathology. ACS Chem Neurosci. 2026;17 (1):62-76.
[10] Kiwamoto T,Kawasaki N,Paulson JC, et al. Siglec-8 as a drugable target to treat eosinophil and mast cell-associated conditions. Pharmacol Ther. 2012;135 (3):327-36.
[11] Peterson KA,Chehade M,Genta RM, et al. Anti-Siglec-8 Antibody for Eosinophilic Gastritis and Duodenitis. N Engl J Med. 2020;383 (17):1624-1634.
[12] Frank MJ,Baird JH,Kramer AM, et al. CD22-directed CAR T-cell therapy for large B-cell lymphomas progressing after CD19-directed CAR T-cell therapy: a dose-finding phase 1 study. Lancet. 2024;404 (10450):353-363.
[13] Rhein S,Serin N,Timiliotis S, et al. A CD22-specific T-cell receptor enables effective adoptive T-cell therapy for B-cell malignancies. Blood. 2026;147 (10):1058-1069.
[14] Razi N,Varki A. Masking and unmasking of the sialic acid-binding lectin activity of CD22 (Siglec-2) on B lymphocytes. Proc Natl Acad Sci U S A. 1998;95 (13):7469-74.
[15] Büll C,Sun L,Van Coillie J, et al. Probing the binding specificities of human Siglecs by cell-based glycan arrays. Proc Natl Acad Sci U S A. 2021;118 (17):.
[16] Angata T,Varki A. Discovery, classification, evolution and diversity of Siglecs. Mol Aspects Med. 2023;90:101117.



