武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
不只是 PD-1:CD96 正成为免疫治疗的下一个“必争之地”
49 人阅读发布时间:2026-04-13 14:04
CD96 是近年来备受关注的新兴免疫检查点分子,在维持免疫稳态和疾病治疗中显示出越来越重要的价值。本文围绕 CD96 的分子背景、作用机制、信号通路、相关疾病及药物研究进展进行系统梳理,以期为相关机制研究及靶向治疗策略开发提供参考。
1. CD96 是什么:新兴免疫检查点的研究背景与临床价值
2. CD96 的分子结构、表达特征与细胞分布
3. CD96 信号通路与作用机制:配体结合如何调控免疫反应
4. CD96 的双重功能:为什么既能抑制免疫又能促进免疫
5. CD96 与疾病的关系:癌症、自身免疫病、妊娠与病毒感染
6. CD96 靶向药物研发进展
7. CD96 研究工具
1. CD96 是什么:新兴免疫检查点的研究背景与临床价值
免疫检查点在维持免疫稳态以及治疗多种癌症和自身免疫疾病中具有关键作用。针对 PD-1 和 CTLA-4 等经典免疫检查点的治疗,已经在临床上取得显著成功 [1]。在这一背景下,更多新型免疫调节分子开始受到关注,其中 TIGIT-CD112R-CD96 轴成为近年来的重要研究方向 [1]。CD96 又称 T 细胞激活和黏附分子(TACTILE),是该轴的重要成员之一,可与 CD155(PVR)结合,并参与免疫反应调控 [1]。
与经典免疫检查点不同,CD96 的功能并非单一抑制,而是具有明显的复杂性。在不同细胞类型和不同微环境中,CD96 既可能提供共刺激信号,也可能介导共抑制效应,从而调节 T 细胞和 NK 细胞的活化、耗竭和效应功能 [1]。已有研究表明,CD96 在抗原经历性 T 细胞、肿瘤浸润淋巴细胞以及部分 NK 细胞群体中表达升高,并与肿瘤免疫状态密切相关 [2]。
泛癌种分析进一步显示,CD96 的表达与预后之间的关系具有明显的肿瘤类型依赖性 [3]。例如,在低级别胶质瘤中,CD96 高表达与较差预后相关;而在皮肤黑色素瘤中,CD96 高表达却与较好生存结局相关 [3]。这种差异提示,CD96 的临床意义不能脱离具体癌种和免疫微环境来理解。与此同时,CD96 的表达还与 CD8+ T 细胞、树突状细胞、巨噬细胞、NK 细胞和调节性 T 细胞等多种免疫浸润成分密切相关 [3]。因此,CD96 已成为值得重点关注的新型免疫检查点分子,其分子特征、功能机制、疾病相关性及药物开发进展,都具有较高的研究和转化价值。
2. CD96 的分子结构、表达特征与细胞分布
2.1 CD96 蛋白结构与分子特征
CD96 又称 Tactile,是一种跨膜糖蛋白,属于免疫球蛋白超家族成员。其分子结构提示其在细胞识别、黏附和信号转导中具有重要作用。已有研究尝试解析 CD96 作为免疫受体的结构基础 [4],但从目前研究情况来看,其与配体结合的精细结构机制仍有待进一步明确。
2.2 CD96 主要表达在哪些免疫细胞
CD96 具有明显的细胞类型特异性,其表达常受细胞活化状态及局部微环境调控。在 T 细胞中,CD96 是人类淋巴细胞谱系中的重要表达分子之一 [2]。研究显示,T 细胞活化过程中 CD96 表达会发生动态变化,高表达 CD96 的 T 细胞通常具有较为特殊的效应功能 [2]。在肿瘤环境中,CD96 在抗原经历性 T 细胞和肿瘤浸润淋巴细胞中升高,并与 T 细胞标志物表达密切相关 [2]。
在 NK 细胞中,CD96 同样具有重要意义。肝细胞癌患者肿瘤组织内 CD96+ NK 细胞的比例、绝对数量及平均荧光强度均明显升高,并伴随 CD96、TIGIT 和 CD226 之间与共同配体 CD155 的受体平衡被打破 [5]。这些结果提示,CD96 在肿瘤中的 NK 细胞调控中可能发挥关键作用。
2.3 CD96 在不同生理和病理环境中的表达差异
CD96 的表达不仅存在于肿瘤相关免疫细胞中,在特殊生理环境中也具有明显特征。例如,在早期妊娠母胎界面,CD96 高表达于蜕膜自然杀伤细胞,而 TIGIT 主要表达于 T 细胞,CD155 和 CD112 主要分布于间期基质细胞和滋养层细胞 [6]。CD96+ dNK 细胞通常表现为低细胞毒性、高黏附性表型,并参与母胎界面的免疫抑制效应 [6]。这说明,CD96 的表达特征与其功能状态密切相关,也是理解其生物学作用的重要基础。
3. CD96 信号通路与作用机制:配体结合如何调控免疫反应
3.1 CD96 与配体 CD155 的结合机制
CD96 的核心功能主要通过与配体 CD155(PVR)的结合介导。研究已明确证实,CD96 可直接与 CD155 相互作用,这一结合是其启动下游信号转导、调节免疫细胞功能的关键基础 [7]。从结构角度看,CD96 是典型的 I 型跨膜糖蛋白,其胞外区含有多个 Ig 样结构域,其中 N 端 IgV 结构域被认为是与 CD155 结合的关键区域 [8]。CD155 同样属于 Ig 超家族,其胞外区由三个 Ig 样结构域组成,CD96 主要通过自身 IgV 结构域与 CD155 的 N 端 IgV 结构域相互识别 [8]。
3.2 CD96、TIGIT、CD226 免疫调控网络
CD96、TIGIT 和共刺激受体 CD226(DNAM-1)共同构成一个复杂的免疫调控网络,它们共享 CD155 和 CD112 等配体,在免疫激活与抑制之间形成动态平衡 [1],[9]。其中,TIGIT 可与 CD155 和 CD112 结合,CD96 主要与 CD155 结合,而 CD112R(PVRIG)主要与 CD112 结合 [1]。这些抑制性受体与共刺激受体 CD226 竞争相同配体,尤其是 CD155 和 CD112 [1],[10]。因此,受体之间的竞争和协同,共同决定了 T 细胞和 NK 细胞的最终功能状态。
3.3 CD96 下游信号通路:MEK-ERK 通路如何传导信号
CD96 与配体结合后可引发胞内信号转导,这是其发挥生物学作用的关键。研究表明,在 CD8+ T 细胞中,CD96 可发挥共刺激功能。当在人或小鼠 CD8+ T 细胞表面交联 CD96 时,可诱导细胞活化、效应细胞因子产生以及增殖 [11]。这一激活作用主要通过 MEK-ERK 通路传导 [11]。通过该通路,CD96 能促进 NUR77 和 T-bet 等转录因子的表达,并增强 CD8+ T 细胞的细胞毒性效应,进而影响效应 T 细胞分化 [11]。
相关体内研究进一步表明,无论是抗体阻断 CD96 活性还是基因敲除 CD96,均会损害 CD8+ T 细胞的活化和效应功能 [11]。这说明,在特定细胞类型中,CD96 并非单纯抑制性受体,而可能是 T 细胞有效应答所需的正向调节因子。
4. CD96 的双重功能:为什么既能抑制免疫又能促进免疫
4.1 CD96 的免疫抑制作用机制
CD96 作为重要免疫检查点分子,在部分背景下表现出明显的免疫抑制作用,尤其是在肿瘤微环境中与免疫细胞耗竭和免疫逃逸密切相关。
在 NK 细胞中,这一现象较为典型。肝细胞癌患者肿瘤组织中 CD96+ NK 细胞显著增多,并呈现功能耗竭状态,表现为 IFN-γ 和 TNF-α 产生受损,同时 IL-10 和 TGF-β1 等免疫抑制相关因子表达升高 [5]。这些结果说明,肿瘤微环境中的高 CD96 表达可能促使 NK 细胞失去有效杀伤功能,进而促进肿瘤进展。
不过,CD96 在 NK 细胞中的抑制作用并非在所有体系中都同样显著。针对扩增 NK 细胞的 CRISPR-Cas9 敲除研究发现,虽然能够有效降低 CD96 蛋白表达,但在体外对白血病细胞的抗肿瘤活性并未显著增强 [12]。这一结果提示,单独干预 CD96 可能不足以显著恢复已扩增和激活 NK 细胞的抗肿瘤能力,说明其功能仍受其他受体网络和背景因素共同影响。
在 T 细胞中,CD96 也可表现出抑制作用。虽然其在人类 T 细胞中的功能一度存在争议,但 CRISPR/Cas9 研究表明,敲除 CD96 可增强人 T 细胞对白血病细胞的杀伤能力 [13]。进一步构建包含 HER2 结合胞外区、CD96 和 CD3ζ 胞内区的 CAR-T 细胞,也揭示了 CD96 胞内结构域在抑制 T 细胞抗肿瘤效应中的作用 [13]。这些结果说明,CD96 在某些背景下可通过胞内信号削弱 T 细胞细胞毒性,促进肿瘤免疫逃逸。
4.2 CD96 的免疫共刺激作用机制
与上述抑制作用不同,CD96 在 CD8+ T 细胞中也可发挥明确的共刺激功能 [11]。作为 PVR-nectin 家族成员,CD96 与 TIGIT 和 CD226 共同参与免疫调控。早期关于其在 CD8+ T 细胞中究竟是抑制还是刺激作用并不明确,但后续研究已证实,CD96 在 CD8+ T 细胞上具有增强活化和效应反应的能力 [11]。CD96 交联可促进 CD8+ T 细胞增殖、细胞因子分泌及细胞毒性分化,并通过 MEK-ERK 通路增强 NUR77 和 T-bet 相关反应 [11]。因此,在 CD8+ T 细胞语境中,CD96 更接近正向调节受体,而非传统意义上的单向抑制分子。
4.3 CD96 双重功能的关键决定因素
CD96 的最大特点之一,就是其功能并非固定,而是强烈依赖于细胞类型和微环境背景 [1]。在 CD8+ T 细胞中,它可表现为共刺激受体,促进活化和效应功能;而在肿瘤微环境中的 NK 细胞中,它又常与耗竭和抑制表型相关 [5],[11]。此外,CD96 与 TIGIT、CD226 共同竞争 CD155 和 CD112 配体,这种复杂的受体-配体网络也进一步放大了其功能差异 [1]。因此,在评估 CD96 作为治疗靶点时,必须充分考虑其所处细胞环境、疾病状态及局部免疫背景。
5. CD96 与疾病的关系:癌症、自身免疫病、妊娠与病毒感染
5.1 CD96 在癌症中的作用与临床意义
5.1.1 CD96 表达与肿瘤预后的关系
CD96 作为新型免疫检查点分子,在不同肿瘤中的表达模式和预后意义具有显著异质性。乳腺癌研究显示,肿瘤细胞高表达 CD96 与更高复发风险相关 [9]。在三阴性乳腺癌新辅助化疗研究中,CD96 及其相关轴线分子的表达也与治疗反应存在关联 [11]。在胃癌中,肿瘤内高水平 CD96+ 细胞浸润是预后不良的独立预测因素,并与氟尿嘧啶类辅助化疗获益较差相关 [14]。在肝细胞癌中,CD96+ NK 细胞增加并伴随功能耗竭,同时 CD96 或 CD155 的高表达与较短 DFS 和 OS 显著相关 [5]。
与此同时,泛癌分析显示 CD96 的临床意义并非单向一致 [3]。在低级别胶质瘤中,CD96 高表达提示不良预后;而在黑色素瘤中,其高表达却与更佳生存结局相关 [3]。这说明 CD96 的预后价值具有鲜明的肿瘤背景依赖性。
5.1.2 CD96 如何影响肿瘤免疫微环境和治疗反应
CD96 在肿瘤免疫微环境中具有重要的负向调节作用,其表达水平与 T 细胞和 NK 细胞的功能状态密切相关。在胃癌中,高 CD96+ 细胞浸润与 CD8+ T 细胞耗竭相关,并形成免疫抑制性肿瘤微环境 [14]。在宫颈癌中,CD96 在肿瘤浸润淋巴细胞中同样与耗竭表型有关 [15]。CD96 主要通过结合 CD155 抑制 NK 细胞和 T 细胞的细胞毒性功能,并与 DNAM-1、TIGIT 共同构成复杂的调控网络 [16]。
值得关注的是,CD96 还与免疫治疗反应和耐药密切相关。在宫颈癌中,PD-1 阻断后 CD8+ TILs 上 CD96 进一步上调,提示 CD96 可能参与补偿性免疫抑制 [15]。研究发现,阻断 CD96 可增强 PD-1 阻断在小鼠模型和宫颈癌样本中的抗肿瘤效果,并改善 CD8+ TIL 功能 [15]。这些结果为 CD96 与 PD-1 联合靶向提供了重要依据。
5.2 CD96 在自身免疫和炎症性疾病中的作用
CD96 的研究已逐渐拓展至自身免疫和炎症性疾病领域。在银屑病样皮炎模型中,CD96 缺陷小鼠较野生型小鼠表现出更轻的炎症症状,并伴随真皮 γδ T 细胞 IL-17A 产生减少 [17]。进一步实验表明,CD96 对 γδ T 细胞的功能调控在银屑病样炎症中具有直接作用 [17]。这一发现说明,CD96 不仅参与肿瘤免疫,也可能介导炎症性疾病中的关键免疫失衡过程。
5.3 CD96 在妊娠免疫调控中的作用
在妊娠早期母胎界面,dNK 细胞是核心免疫细胞群,其数量或功能异常与复发性流产相关。研究表明,CD96 在母胎界面高度表达,dNK 细胞是其主要表达者;与此同时,CD155 和 CD112 分布于间质细胞和滋养层细胞 [6]。CD96+ dNK 细胞呈现低细胞毒性和高黏附性特征,有助于维持母胎界面的免疫抑制状态 [6]。因此,CD96 可能在维持早期妊娠免疫稳态方面发挥重要作用。
5.4 CD96 在病毒感染与抗病毒免疫中的作用
CD96 在病毒感染中的作用同样具有复杂性。HIV-1 感染研究显示,在原代 CD4+ T 细胞中,CD96 表达明显下调,且这一变化受病毒蛋白调控。进一步分析发现,高表达 CD96 的 CD4+ T 细胞通常具有促炎性的 TH1/TH17 表型,并表现出更强的 IFN-γ 和 IL-17 分泌能力。此外,CD96 的配体结合可增强病毒肽刺激后的 IFN-γ 释放,并促进 TH1/TH17 相关因子分泌。这些结果提示,HIV-1 可能通过调控 CD96 表达来削弱宿主抗病毒免疫应答。与此同时,CD96 的配体 CD155 也在抗病毒免疫中发挥重要作用,其表达受基因毒性应激、RAS 激活以及 TLR 相关通路调控。
6. CD96 靶向药物研发进展
目前,靶向CD96的药物研发主要集中于单克隆抗体和双特异性抗体,在研适应症以非小细胞肺癌、晚期恶性实体瘤及多种晚期癌症为主,最高研发阶段已推进至临床2期,部分在研管线列举如下表:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| Nelistotug | CD96 | 单克隆抗体 | 非小细胞肺癌 | 晚期恶性实体瘤 | 肿瘤 | GSK Plc | 23andMe, Inc. | 临床2期 |
| BMS-986442 | CD96 x TIGIT | 双特异性抗体 | 晚期癌症 | 局部晚期恶性实体瘤 | 胃癌 | 结肠癌 | 胃食管交界处腺癌 | 头颈部鳞状细胞癌 | Agenus, Inc. | Bristol Myers Squibb Co. | 临床1期 |
| anti-CD96 antibody (Jiangsu hengrui) | CD96 | 单克隆抗体 | 肿瘤 | 江苏恒瑞医药股份有限公司 | 药物发现 |
(数据截止到2026年3月25日,来源于synapse)
7. CD96 研究工具
CD96 是一个兼具潜力与复杂性的免疫检查点分子,已成为新一代免疫调节研究的重要节点。随着其生物学机制不断被厘清,以及抗体、小分子和基因编辑等多类策略持续推进,CD96 有望在肿瘤免疫治疗及其他免疫相关疾病干预中展现更明确的应用价值。华美生物提供CD96重组蛋白、抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD96 重组蛋白
Recombinant Human T-cell surface protein tactile (CD96), partial (Active); CSB-MP004971HU1(F2)
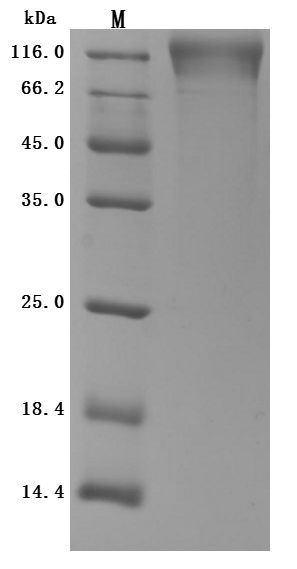
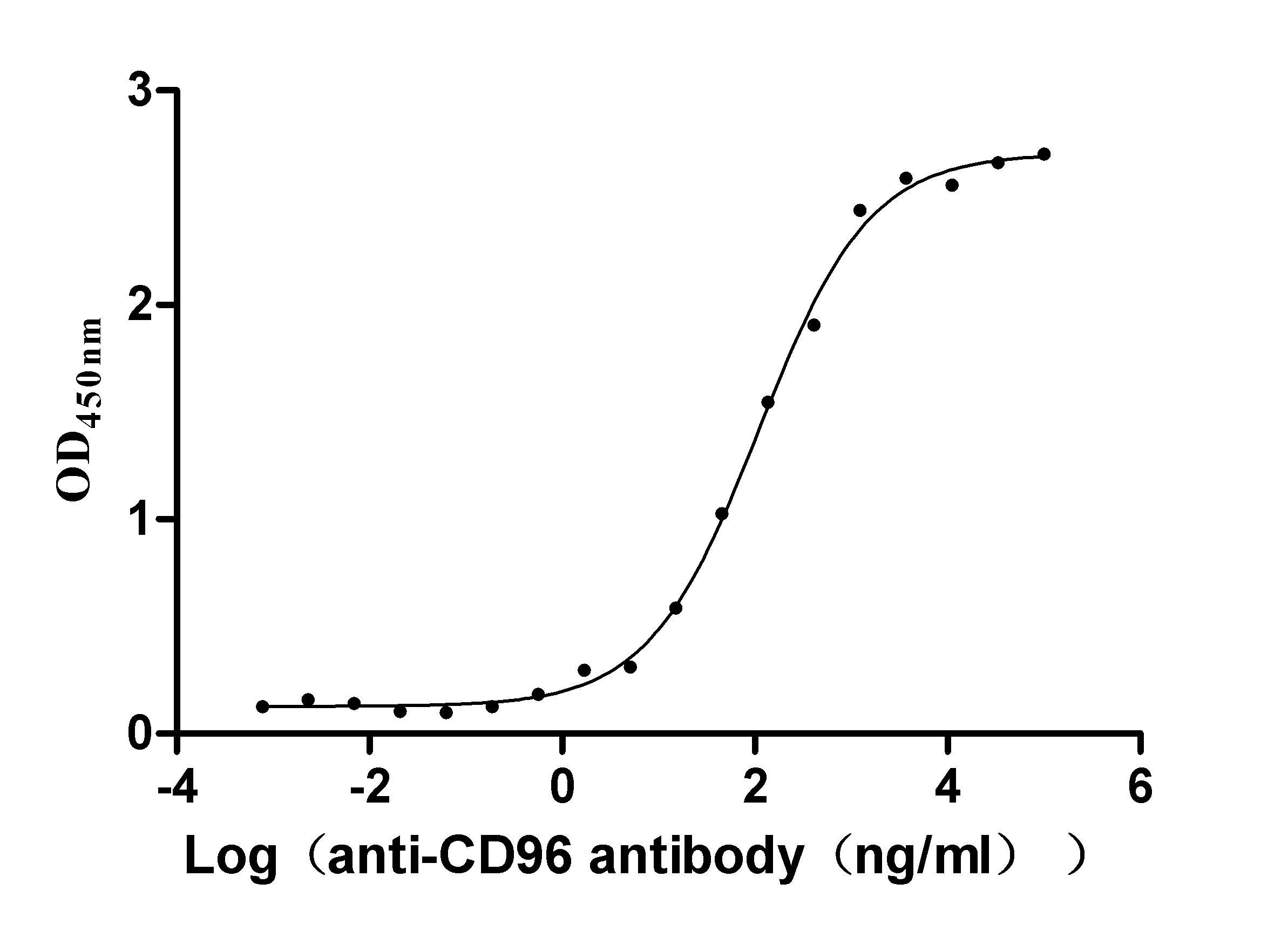
● CD96 抗体
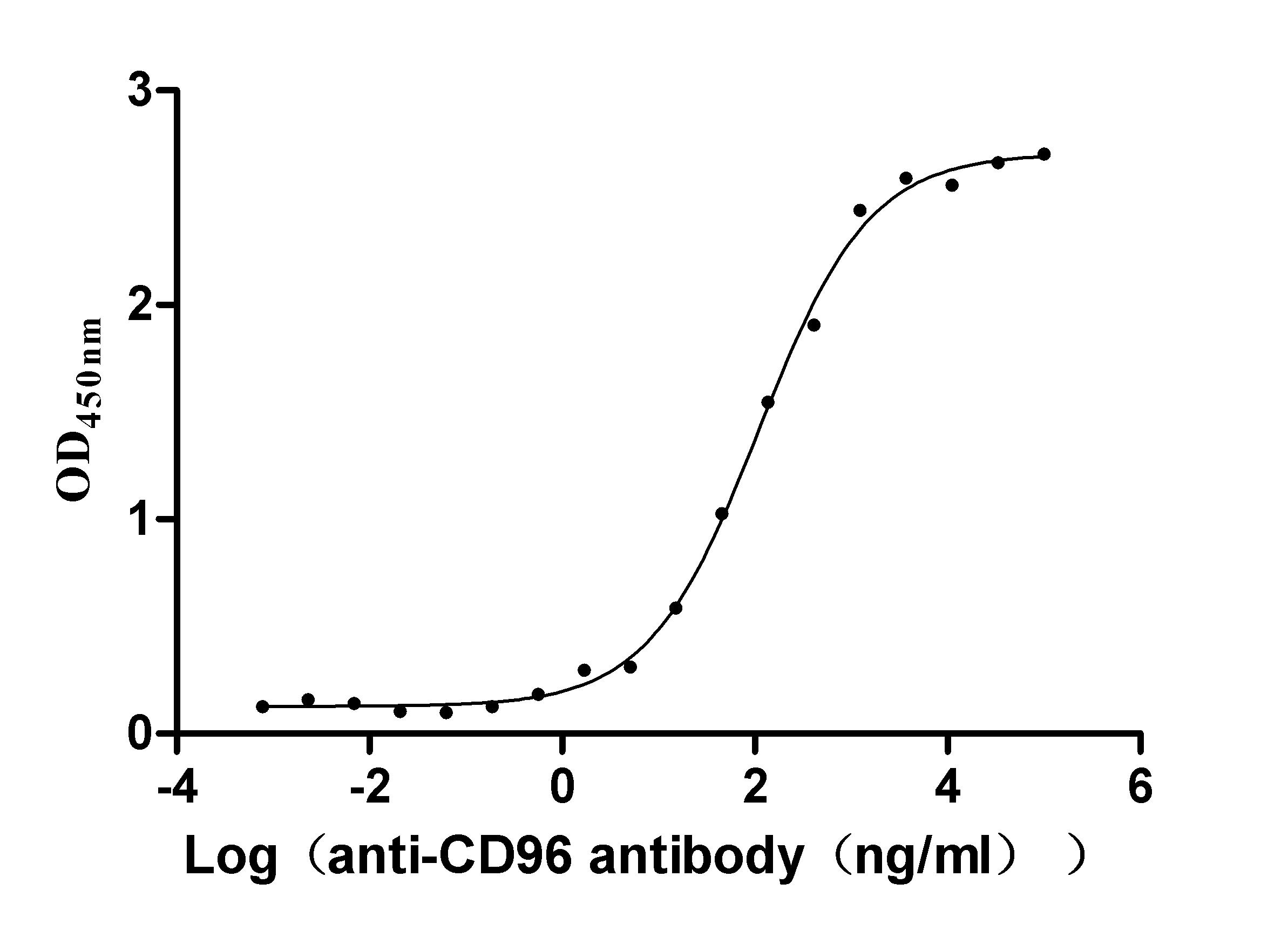
CD96 Recombinant Monoclonal Antibody; CSB-RA004971A0HU
● CD96 ELISA 试剂盒
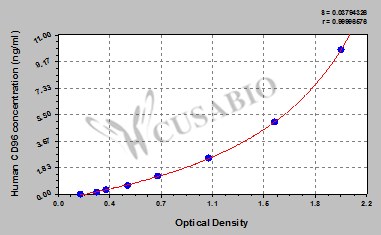
Human T-cell surface protein tactile(CD96) ELISA kit; CSB-EL004971HU
[1] .(2023). Abstract 6651: MoA-based potency bioassays for immunotherapy programs targeting the TIGIT/CD112R/CD96 axis.
[2] A. Lepletier, V. Lutzky, D. Mittal, Kimberley A Stannard, Thomas S. Watkins, C. Ratnatunga, Corey Smith, H. McGuire, R. Kemp, P. Mukhopadhyay, N. Waddell, M. Smyth, W. Dougall, John J Miles.(2018). The immune checkpoint CD96 defines a distinct lymphocyte phenotype and is highly expressed on tumor‐infiltrating T cells.
[3] W. Ye, C. Luo, Fangkun Liu, Zhixiong Liu, Fenghua Chen.(2021). CD96 Correlates With Immune Infiltration and Impacts Patient Prognosis: A Pan-Cancer Analysis.
[4] Felix A. Deuss, G. M. Watson, Zhihui Fu, J. Rossjohn, R. Berry.(2019). Structural Basis for CD96 Immune Receptor Recognition of Nectin-like Protein-5, CD155.
[5] Haoyu Sun, Qiang Huang, Meijuan Huang, H. Wen, R. Lin, M. Zheng, K. Qu, Kun Li, Haiming Wei, Weihua Xiao, R. Sun, Z. Tian, Cheng-song Sun.(2019). Human CD96 Correlates to Natural Killer Cell Exhaustion and Predicts the Prognosis of Human Hepatocellular Carcinoma.
[6] Yingjie Wang, Yun Wang.(2023). Palmitic Acid Upregulates CD96 Expression to Mediate Maternal--Foetal Interface Immune Tolerance by Inhibiting Cytotoxic Activity and Promoting Adhesion Function in Human Decidual Natural Killer Cells.
[7] Hui Zhang, Qianwen Liu, Yiyan Lei, Jianwen Zhou, Wenting Jiang, Yongmei Cui, Qiong He, Junfeng Zhu, Zheng-zhi Zhu, Yu Sun, Zunfu Ke.(2020). Direct interaction between CD155 and CD96 promotes immunosuppression in lung adenocarcinoma.
[8] D. Meyer, S. Seth, J. Albrecht, M. Maier, L. Pasquier, I. Ravens, L. Dreyer, R. Burger, M. Gramatzki, R. Schwinzer, E. Kremmer, R. Foerster, G. Bernhardt.(2009). CD96 Interaction with CD155 via Its First Ig-like Domain Is Modulated by Alternative Splicing or Mutations in Distal Ig-like Domains.
[9] Xin Ou, Junyu Yin, F. Shi, Yanjie Zhao, Quan Zhou, Keyu Yuan, S. Lyu, Jiangping Wu, Yanping Li, Q. Song.(2025). CD155-TIGIT/CD96/CD226 immune checkpoint axis interacting with tumor-infiltrating lymphocytes to exhibit diverse prognostic effects on breast cancer: a cohort study.
[10] H. Stamm, J. Wellbrock, W. Fiedler.(2018). Interaction of PVR/PVRL2 with TIGIT/DNAM-1 as a novel immune checkpoint axis and therapeutic target in cancer.
[11] Keyu Yuan, Xin Ou, S. Lyu, Feng Shi, Quan Zhou, Yanjie Zhao, Jiangping Wu, Yu Cao, Yanping Li, Qingkun Song.(2025). The predictive effect of the CD155-TIGIT immune checkpoint axis complex on neoadjuvant chemotherapy efficacy in triple-negative breast cancer: A preliminary study.
[12] E. Chiang, Patrícia E. de Almeida, D. Nagata, Kristin Bowles, Xiangnan Du, A. Elgin, Karl L. Banta, Y. Kwon, Brent S. McKenzie, S. Mittman, R. Cubas, Keith Anderson, S. Warming, J. Grogan.(2020). CD96 Functions as a co‐stimulatory receptor to enhance CD8+ T cell activation and effector responses.
[13] Tahereh Mohammadian Gol, Miso Kim, Ralph Sinn, Guillermo Ureña-Bailén, Sarah Stegmeyer, P. G. Gratz, Fatemeh Zahedipour, Alicia Roig-Merino, Justin S Antony, Markus Mezger.(2023). CRISPR-Cas9-Based Gene Knockout of Immune Checkpoints in Expanded NK Cells.
[14] Chelsia Qiuxia Wang, F. C. Choy, A. Sanny, Takashi Murakami, A. Tan, K. Lam.(2023). An Inhibitory Role for Human CD96 Endodomain in T Cell Anti-Tumor Responses.
[15] Chang Xu, H. Fang, Yun Gu, K. Yu, Jieti Wang, Chao Lin, Heng Zhang, He Li, Hongyong He, Hao Liu, Ruochen Li.(2022). Impact of intratumoural CD96 expression on clinical outcome and therapeutic benefit in gastric cancer.
[16] Yumeng Wang, Congwen Wang, J. Qiu, Xinyu Qu, Jing Peng, Chong Lu, Meng Zhang, Mingxing Zhang, Xingling Qi, Guiling Li, K. Hua.(2022). Targeting CD96 overcomes PD-1 blockade resistance by enhancing CD8+ TIL function in cervical cancer.
[17] R. Maas, J. H. Hoogstad-van Evert, J. V. D. Van der Meer, V. Mekers, Somayeh Rezaeifard, A. Korman, P. D. de Jonge, J. Cany, R. Woestenenk, N. Schaap, L. Massuger, J. Jansen, W. Hobo, H. Dolstra.(2020). TIGIT blockade enhances functionality of peritoneal NK cells with altered expression of DNAM-1/TIGIT/CD96 checkpoint molecules in ovarian cancer.



