武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
不止PD-1/CTLA-4!这个新兴免疫检查点CD160正在改变肿瘤免疫治疗格局
61 人阅读发布时间:2026-04-07 10:26
1. 什么是CD160?
CD160是一种与免疫调节密切相关的膜分子,主要分布于NK细胞、部分T细胞及肠上皮内淋巴细胞等免疫细胞中。近年来,随着肿瘤免疫、慢性感染和免疫检查点研究的持续推进,CD160逐渐成为值得关注的新兴研究靶点。其核心特点在于,CD160并不是一个功能单一的分子,而是在不同细胞类型、不同组织环境和不同配体条件下,表现出激活或抑制等不同生物学功能。
当前,免疫检查点研究早已不再局限于PD-1/PD-L1或CTLA-4等经典分子。越来越多研究表明,免疫细胞的功能失调通常并非由单一分子决定,而是多种抑制性受体共同参与的结果。针对这一问题,研究者建立了用于分析人外周血和肿瘤浸润淋巴细胞的16色流式面板OMIP-037,将PD-1、TIM-3、CD160、LAG-3和TIGIT等多个抑制性受体纳入同一检测体系,可在单细胞层面识别多达32种抑制受体组合,并进一步区分CD4+、CD8+、NK、iNKT和γδ T细胞等亚群,为系统研究CD160在不同免疫细胞中的表达特征提供了重要工具 [1]。
这一研究框架说明了两个关键问题。首先,免疫耗竭本质上是多分子参与的复杂过程,单一标志物难以完整反映功能状态。其次,CD160并不是一个单纯冗余的共抑制分子。现有证据显示,它既可能在NK细胞中促进代谢活化和细胞因子分泌,也可能在某些T细胞环境中与抑制性表型相关,并通过与HVEM结合参与负向调节。因此,CD160很可能代表一条具有独立生物学意义的免疫调控通路 [1]。
来自多种实体瘤的泛癌分析也进一步支持了CD160作为新兴免疫检查点的重要性。TCGA整合研究显示,在肺癌、乳腺癌和结直肠癌等多种肿瘤中,CD160与LAG-3、TIGIT等检查点分子在CD8+ T细胞中普遍呈高表达,不同肿瘤之间差异并不十分显著,提示其可能参与广泛存在的肿瘤免疫抑制机制。同时,不同检查点配体在肿瘤微环境中的来源细胞并不相同,例如某些配体更偏向由巨噬细胞表达,而另一些则更多来自上皮细胞。这意味着,CD160相关信号不仅取决于分子本身,还与细胞空间分布和局部微环境密切相关 [2]。
不过,目前关于CD160的研究仍存在明显不足。现有文献中,许多结果集中于表达谱描述和相关性分析,而其在不同细胞中的下游信号机制、异构体差异、膜环境影响以及与其他检查点分子的功能分工仍未完全阐明。因此,CD160虽然已成为肿瘤免疫和免疫调控研究中的热点分子之一,但其机制研究和临床转化仍处于持续推进阶段 [1,2]。
2. CD160的分子结构与基础特征
2.1 CD160的发现历史
CD160最初作为一种GPI锚定的免疫球蛋白样受体被发现,并通过BY55单抗在外周血细胞毒性较强的CD56dim NK细胞和TCRγδ淋巴细胞中被鉴定出来。研究还发现,尽管外周血中表达CD160的CD4+或CD8+ T细胞数量有限,但在肠道和皮肤等组织中,该分子的表达更加明显,提示它可能与组织免疫监视和局部效应功能相关 [3]。
2.2 CD160的主要异构体类型
后续研究表明,CD160至少存在两种主要形式:一种是经典的GPI锚定型CD160-GPI,另一种是跨膜型CD160-TM。两种异构体都可以在初代CD4+和CD8+ T细胞中检测到,但其功能并不相同。实验显示,CD160-GPI在HVEM-Fc或抗-CD160抗体刺激下,可增强Jurkat细胞活化,提示其具有一定的正向共刺激潜能;而CD160-TM在相同条件下响应较弱,对HVEM的结合信号也较低 [4]。
这一现象说明,CD160的功能不仅由胞外识别决定,还可能受到膜锚定方式、膜区定位和受体聚集能力的影响。换句话说,不同异构体并非只是结构差异,而可能决定CD160在不同细胞环境中发挥完全不同的生物学作用 [4]。
2.3 CD160与HVEM的结合机制
围绕CD160与HVEM的结合方式,结构生物学研究提供了更深入的解释。基于昆虫细胞共表达和原位纯化的实验结果,天然非连接型CD160-HVEM复合物在溶液中可形成3:3三聚体,相关晶体学分析支持这一结论 [5]。这一结果与早期一些将CD160视为单体的结论并不完全一致,提示不同实验体系、表达系统、糖基化修饰状态以及重组策略,都会影响对其寡聚形式的判断 [5]。
从功能角度看,可以合理推测,GPI锚定形式更有利于CD160在膜上横向移动并聚集于脂筏区域,从而增强与HVEM形成稳定复合物的能力;而跨膜型CD160-TM则可能因空间取向或局部膜环境不同而表现出较弱的信号活性。不过,这种推断目前仍缺乏在天然细胞膜环境中的直接高分辨率证据,仍需进一步验证 [4,5]。
3. CD160的表达模式与配体识别
3.1 CD160的细胞表达分布
CD160最早被视为NK细胞相关分子,主要表达于CD56dim NK细胞、TCRγδ淋巴细胞及少部分具有细胞毒特征的CD8+ T细胞中,同时在肠上皮内淋巴细胞(IEL)中也有较高表达。随着研究深入,科学家发现CD160的表达并不局限于这些经典细胞群。例如,在皮肤组织中,一部分效应记忆型CD4+ T细胞同样表达CD160,并伴随CLA、CCR4等皮肤归巢分子及穿孔素等细胞毒相关分子,提示CD160也可能是组织驻留型或终末分化效应细胞的标志之一 [6]。
在肿瘤微环境中,HVEM和CD160往往与BTLA等分子共同构成一个相互关联的调控网络。研究表明,BTLA轴相关基因在肿瘤组织中常呈共表达趋势,说明HVEM-CD160/BTLA通路可能参与肿瘤免疫抑制和肿瘤微环境重塑 [7]。此外,在肿瘤抗原特异性CD8+ T细胞中,CD160常与PD-1、TIM-3、LAG-3等分子共表达,这一现象通常与功能障碍或耗竭状态相关,但不同肿瘤和不同组织部位之间仍存在差异 [8]。
3.2 CD160对HVEM的结构识别机制
在结构层面,人源CD160胞外区具有独特的免疫球蛋白样折叠,可与HVEM形成1:1化学计量的复合物。其结合界面在总体上与BTLA-HVEM复合体有一定相似性,但又保留自身特点 [9]。更广义地看,HVEM本身是一个多配体平台,除可与CD160和BTLA结合外,还可识别TNF家族配体LIGHT,而且这些结合位点并不完全重叠。在某些情况下,HVEM甚至可以同时参与形成更高阶的复合物,从而整合多条免疫信号 [10]。
早期基于HDX-MS和分子建模的研究虽然分辨率有限,但对于关键接触区域和构象变化趋势的描述,与后续晶体学研究结果基本一致 [11]。因此,现有证据总体支持这样一个观点:CD160与HVEM之间的结合是有明确结构基础的,而且该结合并不只是简单的二元相互作用,而是嵌入在更复杂的HVEM配体网络之中 [9,10,11]。
不过,也需要看到,大多数结构研究仍基于重组胞外片段完成,尚未充分纳入糖基化、膜面排列、脂筏定位及细胞间空间构型等因素。因此,CD160-HVEM互作在真实生理环境中究竟如何被动态调控,仍是后续研究的重要问题 [9,10,11]。
4. CD160的信号通路与免疫调控机制
4.1 CD160/HVEM/BTLA轴的信号传导机制
HVEM并不是一个固定输出激活或抑制信号的分子,它更像是一个"信号中枢",其功能取决于所结合的配体以及结合发生的空间环境。研究显示,在人类系统中,HVEM与CD160结合后可选择性地共刺激NK细胞。肿瘤细胞表面的HVEM能够增强CD56dim NK细胞的活化,促进I型 IFN 和IL-2诱导的IFN-γ、TNF-α分泌,同时触发ERK1/2和AKT的快速磷酸化,并增强细胞毒作用 [12]。这说明CD160-HVEM互作可联动MAPK和PI3K-AKT等经典效应通路,在NK细胞中发挥促活化作用 [12]。
但当HVEM结合的对象变为BTLA时,结果则可能转向抑制。研究发现,BTLA可抑制细胞毒活性,说明HVEM的信号输出依赖于配体身份,并非天然偏向激活 [12]。更进一步,BTLA与HVEM还能在同一细胞膜上形成顺式复合物,这种构型会阻断外源性HVEM的共刺激,同时保留BTLA的抑制功能,因此整体上更倾向于抑制性信号 [13]。这也解释了为什么HVEM在部分原代T细胞中并不表现出强烈的共刺激效应。
在某些病毒感染模型中,HVEM和BTLA之间还可形成更复杂的双向调节关系。例如,在疫苗痘病毒模型中,HVEM和BTLA缺失都会损害效应CD8+ T细胞的存活和记忆形成,提示BTLA在特定情况下也可作为HVEM的反向配体,在trans模式下向T细胞提供促存活信号 [14]。
另一方面,CD160本身的表达还受到上游诱导程序调控。在HIV-1暴露树突细胞激活T细胞的模型中,p38 MAPK/STAT3通路可促进包括CD160在内的抑制性受体上调,而阻断该通路则可降低这些分子的表达并恢复T细胞增殖 [15]。这意味着,CD160相关信号不仅是受体-配体结合的结果,也受细胞内转录调控网络的影响 [15]。
4.2 CD160对不同免疫细胞的功能调控
CD160在NK细胞中的作用相对清晰。基因敲除小鼠研究显示,CD160缺失并不影响NK细胞发育或基础杀伤能力,但会削弱机体对NK敏感性肿瘤的控制能力,并显著降低NK细胞IFN-γ分泌。骨髓嵌合和回输实验进一步证明,CD160阳性NK细胞在早期肿瘤免疫监视中具有关键作用 [16]。由此可见,CD160在NK细胞中的主要价值,可能更偏向促进细胞因子输出和早期抗肿瘤效应,而不是单纯影响脱颗粒能力 [16]。
这一作用与代谢状态密切相关。在HIV感染者中,NK细胞表面CD160表达下降,并与疾病进展呈负相关。CD160阳性NK细胞通常具有更高的GLUT1表达和葡萄糖摄取能力,其活化伴随PI3K/AKT/mTOR/S6K代谢轴增强,而血浆TGF-β1升高则与CD160下调有关 [17]。类似结果也见于肝细胞癌:肿瘤内NK细胞CD160水平下降,与更差预后和更高复发风险相关,高水平TGF-β1可抑制CD160+ NK细胞IFN-γ产生,而阻断TGF-β1则可部分恢复该功能 [18]。这些研究说明,CD160不仅是一个免疫细胞表面标志物,也与NK细胞代谢适应性和效应状态密切相关 [17,18]。
与NK细胞相比,CD160在T细胞中的作用更加复杂。在TCR工程化T细胞研究中,持续存活的移植物T细胞可上调包括CD160在内的多种共抑制分子,并伴随功能下降 [19]。在慢性淋巴细胞白血病(CLL)患者中,CD160是CD8+ T细胞显著上调的共抑制受体之一,其高表达与耗竭样表型相关,并受到细胞外囊泡和炎症因子的调控 [20]。此外,也有研究提示CD160在某些T细胞环境中具有负向调节作用 [21]。由于CD160本身是GPI锚定分子,并不具备典型胞内信号结构域,因此它在T细胞中究竟通过何种膜微区、共受体或反向信号机制发挥抑制作用,仍需要进一步明确 [19,20,21]。
除了肿瘤和感染场景外,CD160在组织修复中也有生理作用。研究显示,在化疗诱导的肠损伤模型中,肠上皮内淋巴细胞可通过CD160与上皮细胞表面HVEM相互作用,激活上皮细胞NF-κB信号,促进过渡放大细胞增殖和黏膜修复。若该通路缺失,则会导致肠道再生受损和更高死亡风险,而回输CD160阳性IEL则能改善这一表型 [22]。这说明CD160并不只是"抑制性检查点",在特定组织环境中还参与免疫-组织互作和损伤修复 [22]。
5. CD160与疾病:肿瘤、感染、自身免疫和炎症
5.1 CD160在肿瘤中的双重作用
在肿瘤研究中,CD160具有明显的双重属性:一方面,它可能标记有效的抗肿瘤免疫细胞;另一方面,它又可能参与免疫逃逸或功能障碍。
在错配修复缺陷/微卫星高度不稳定(dMMR/MSI-H)结直肠癌新辅助免疫治疗研究中,一类肿瘤内PD-1lo CD8+ T细胞同时高表达CD160、TRGC2和KLRB1,且低表达典型增殖/耗竭基因,这一亚群与病理完全缓解显著相关,提示CD160可能标记一类对PD-1阻断敏感的功能性效应细胞 [23]。在肺腺癌中,血浆细胞外囊泡转录组研究也发现,基线EV-CD160水平与免疫化疗应答、无进展生存期和总生存期均呈正相关,且其动态变化可用于疗效监测 [24]。
但另一方面,CD160也可能被肿瘤细胞本身利用。在三阴性乳腺癌中,研究发现肿瘤细胞可表达跨膜型CD160-TM,研究者据此开发出特异性抗体22B12,可在体外诱导抗体依赖的细胞介导的细胞毒性作用(ADCC)和抗体依赖的细胞介导的吞噬作用(ADCP),并在小鼠模型中显示抗肿瘤活性 [25]。这说明CD160并不只是免疫细胞标志物,在某些肿瘤中还可能成为直接的治疗靶点 [25]。
此外,不同肿瘤中的CD160结果并不一致。食管鳞癌中,肿瘤细胞高表达XCL1和CD160可能与免疫逃逸相关 [26];流行病学蛋白组研究提示血浆CD160与乳腺癌风险有关 [27];在血液肿瘤中,CLL来源外泌体可诱导受体细胞上调PD-1和CD160,而在急性髓系白血病中,CD8+ T细胞虽然上调CD160和PD-1,却未必表现为典型终末衰竭,可能更接近激活相关或"伪耗竭"状态 [28,29]。
因此,可以将CD160理解为一个**兼具肿瘤免疫标志物和潜在治疗靶点属性的新兴分子**。但其真正的应用价值仍取决于细胞来源区分、异构体鉴定和具体肿瘤类型分析 [23,24,25]。
5.2 CD160在慢性感染中的作用
在感染性疾病研究中,CD160最常与T细胞耗竭联系在一起。HIV研究显示,单独表达CD160或PD-1的HIV特异性CD8+ T细胞仍保留一定功能,而CD160与PD-1共表达的细胞则表现出更明显的增殖受限和细胞因子下降,并伴随NFκB相关节点下调及多种抑制性分子上调。阻断CD160-HVEM互作可在体外恢复这些细胞的增殖和细胞因子分泌,说明该轴在维持或强化耗竭状态中具有实际作用 [30]。
进一步研究发现,HIV慢性感染中的T-betdimEomeshi表型与PD-1、CD160和2B4高表达密切相关,这类细胞通常处于过渡性记忆/耗竭状态,并可在抗逆转录病毒治疗(ART)长期抑制后持续存在 [31]。与此同时,高亲和力HIV特异性T细胞也更易富集于PD-1/2B4/CD160共表达群体中,在病毒反弹时呈现更强的功能障碍和克隆更新 [32]。这些结果说明,CD160相关耗竭并不是短暂现象,而可能嵌入稳定的转录和分化程序之中 [30,31,32]。
不过,CD160高表达并不总等同于抑制。例如在败血症中,2B4hiPD-1lowCD160hi表型与更强细胞因子产生和更差预后有关,提示其也可能代表一种高度激活但失衡的免疫状态 [33]。在急性戊型肝炎病毒(HEV)感染和疟疾等疾病中,CD160同样表现出与病原类型和免疫病理过程相关的复杂作用 [34,35]。因此,在感染场景下,CD160更适合作为一个**情境依赖的免疫状态指示分子**,而不是简单归类为"抑制性标志物" [30,33,34,35]。
5.3 CD160在自身免疫、炎症和代谢性疾病中的作用
除肿瘤和感染外,CD160也出现在多种自身免疫和炎症性疾病研究中。原发性舍格伦综合征患者外周血中,BTLA、HVEM和CD160的表达及共表达频率均下降,提示BTLA-HVEM-CD160网络在免疫稳态维持中可能受损 [36]。在系统性红斑狼疮中,CD8+ T细胞CD160水平下降,并与疾病活动度相关 [37]。这一现象与慢性感染中CD160作为耗竭相关分子的上调趋势形成对照,再次说明CD160的意义必须放在具体疾病背景中解释 [38,39]。
在遗传学层面,针对自身免疫性甲状腺疾病的研究发现,CD160相关位点rs744877与Graves病风险相关,但与桥本甲状腺炎无明显关联,提示CD160通路可能参与部分自身免疫病的易感性形成 [40]。
在炎症性肠病模型中,单细胞研究发现一类IL-23R依赖的Th1样致病细胞表达CD160,干扰该分子可抑制移植性结肠炎,说明在某些促炎T细胞亚群中,CD160可能参与致病性程序维持 [41]。在非酒精性脂肪肝(NAFLD)研究中,CD160又被纳入NAFLD相关的色氨酸代谢-免疫互作网络,其诊断判别能力较高,并与M2巨噬细胞浸润相关 [42]。不过,这类证据目前多为关联性结果,尚不足以证明CD160是直接驱动因子 [42]。
总体来说,CD160在这些疾病中的共同特点是:它既可能反映免疫稳态破坏,也可能直接参与炎症或致病过程。因此,CD160是否适合作为治疗靶点或生物标志物,还需要更多细胞类型特异性和纵向随访研究来支持 [36,37,40,41,42]。
6. CD160/HVEM轴的药物研究进展
随着CD160研究不断深入,围绕CD160/HVEM轴的药物开发也逐渐展开。目前主要有两类思路:一类是阻断HVEM相关抑制信号以增强抗肿瘤免疫,另一类是利用CD160通路的免疫调节功能来抑制异常免疫反应。部分在研管线列举如下:
| 药物 | 靶点 | 药物类型 | 在研适应症 | 在研机构 | 最高研发阶段 |
|---|---|---|---|---|---|
| ELB011 | CD160 | 抗体 | 眼部疾病 | ElsaLys Biotech SAS | 临床前 |
| CD160-TM(Alderaan) | CD160 | 单克隆抗体 | 三阴性乳腺癌 | Alderaan Biotechnology SAS | 临床前 |
| ELB-012 | CD160 | 双特异性抗体 | 青光眼 | 视网膜疾患 | ElsaLys Biotech SAS | 药物发现 |
| ELB-021 | CD160 | 单克隆抗体 | 实体瘤 | ElsaLys Biotech SAS | 药物发现 |
| WO2023170207 | CD160 | 抗体 | 免疫系统疾病 | 骨髓增生异常综合征 | 肿瘤 | University of Reims Champagne-Ardenne | Centre National de la Recherche Scientifique等 | 药物发现 |
(数据截止到2026年3月26日,来源于synapse)
7. CD160研究工具推荐
CD160连接了免疫检查点、生物能量代谢、细胞分化状态和组织微环境等多个方向,既可能作为肿瘤免疫和慢性感染中的状态标志物,也可能成为肿瘤、自身免疫、移植和局部炎症相关疾病中的干预靶点。目前,CD160已从早期的表面标志物研究,逐步进入机制整合和药物探索阶段。华美生物提供CD160抗体及ELISA试剂盒产品,助力您进行相关机制研究及靶向药物开发。
● CD160 抗体
CD160 Antibody; CSB-PA004881EA01HU
● CD160 ELISA 试剂盒
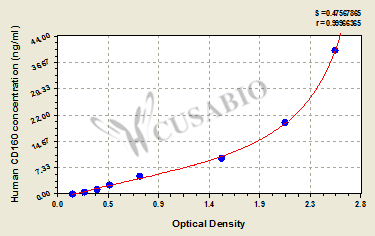
Human CD160 antigen(CD160) ELISA kit; CSB-EL004881HU
[1] Anna C. Belkina, Jennifer Snyder‐Cappione. (2016). OMIP‐037: 16‐color panel to measure inhibitory receptor signatures from multiple human immune cell subsets.
[2] Jiahuan Jiang, Yazhang Xu, Di Chen, Jiaxin Li, Xiaoling Zhu, Jun Pan, Leyi Zhang, Pu Cheng, Jian Huang. (2024). Pan-cancer analysis of immune checkpoint receptors and ligands in various cells in the tumor immune microenvironment.
[3] Nouhoum Sako, Valérie Schiavon, T. Bounfour, Valérie Dessirier, Nicolás Ortonne, Daniel Olive, C. Ram‐Wolff, Laurence Michel, Hélène Sicard, Anne Marie‐Cardine, M. Bagot, Armand Bensussan, Christian Schmitt. (2014). Membrane expression of NK receptors CD160 and CD158k contributes to delineate a unique CD4+ T‐lymphocyte subset in normal and mycosis fungoides skin.
[4] Mohamed El-Far, Charles Pellerin, Louise Pilote, Jean-Francois Fortin, Ivan A D Lessard, Yoav Peretz, Elizabeth Wardrop, Patrick Salois, Richard C Bethell, Michael G Cordingley, George Kukolj. (2014). CD160 isoforms and regulation of CD4 and CD8 T-cell responses.
[5] Simona Lenhartová, Marek Nemčovič, Radka Šebová, Mário Benko, Dirk M. Zajonc, Ivana Nemčovičová. (2021). Molecular Characterization of the Native (Non-Linked) CD160--HVEM Protein Complex Revealed by Initial Crystallographic Analysis.
[6] Anna E. S. Brooks. (2014). Skin‐resident CD4+ T cells express NK receptors: Lessons from skin pathologies.
[7] Daisuke Nishizaki, Sharon Choi, Chinmayi Pandya, Suzanna Lee, Sarabjot Pabla, Paul DePietro, Taylor J Jensen, Razelle Kurzrock, Shumei Kato. (2025). Pan-Cancer Landscape of B- and T-Lymphocyte Attenuator: Implications for Potential Immunotherapy Combinations.
[8] Lukas Baitsch, Amandine Legat, Leticia Barba, Silvia A. Fuertes Marraco, Jean‐Paul Rivals, Petra Baumgaertner, Céline Christiansen-Jucht, Hanifa Bouzourène, Donata Rimoldi, Hanspeter Pircher, Nathalie Rufer, Maurice Matter, Olivier Michielin, Daniel E. Speiser. (2012). Extended Co-Expression of Inhibitory Receptors by Human CD8 T-Cells Depending on Differentiation, Antigen-Specificity and Anatomical Localization.
[9] Weifeng Liu, Sarah C Garrett, Elena V Fedorov, Udupi A Ramagopal, Scott J Garforth, Jeffrey B Bonanno, Steven C Almo. (2019). Structural Basis of CD160:HVEM Recognition.
[10] Weifeng Liu, Ting-Fang Chou, Sarah C. Garrett-Thomson, Goo‐Young Seo, E.V. Fedorov, U.A. Ramagopal, J.B. Bonanno, Qingyang Wang, Kenneth Kim, S. Garforth, Kiyokazu Kakugawa, Hilde Cheroutre, Mitchell Kronenberg, Steven C. Almo. (2021). HVEM structures and mutants reveal distinct functions of binding to LIGHT and BTLA/CD160.
[11] Katarzyna Kuncewicz, Marta Spodzieja, Adam K. Sieradzan, Agnieszka Karczyńska, Katarzyna Dąbrowska, Michał Dadlez, Daniel E. Speiser, Laurent Derré, Sylwia Rodziewicz‐Motowidło. (2019). A structural model of the immune checkpoint CD160-HVEM complex derived from HDX-mass spectrometry and molecular modeling.
[12] John R. Šedý, Ryan Bjordahl, Vasileios Bekiaris, Matthew G. Macauley, Brian C. Ware, Paula S. Norris, Nell S. Lurain, Chris A. Benedict, Carl F. Ware. (2013). CD160 Activation by Herpesvirus Entry Mediator Augments Inflammatory Cytokine Production and Cytolytic Function by NK Cells.
[13] Claire Battin, Judith Leitner, Petra Waidhofer‐Söllner, Katharina Grabmeier‐Pfistershammer, Daniel Olive, Peter Steinberger. (2022). BTLA inhibition has a dominant role in the cis-complex of BTLA and HVEM.
[14] Rachel Flynn, Tarun E. Hutchinson, Kenneth M. Murphy, Carl F. Ware, Michael Croft, Shahram Salek‐Ardakani. (2013). CD8 T Cell Memory to a Viral Pathogen Requires Trans Cosignaling between HVEM and BTLA.
[15] Karlhans Fru, Esaki M. Shankar, Sundaram Muthu, Sasan Zandi, Mikael Sigvardsson, Jorma Hinkula, Davorka Messmer, Marie Larsson. (2012). p38 Mitogen-Activated Protein Kinase/Signal Transducer and Activator of Transcription-3 Pathway Signaling Regulates Expression of Inhibitory Molecules in T Cells Activated by HIV-1-Exposed Dendritic Cells.
[16] Tony C Tu, Nicholas K Brown, Tae-Jin Kim, Joanna Wroblewska, Xuanming Yang, Xiaohuan Guo, Seoyun Hyunji Lee, Vinay Kumar, Kyung-Mi Lee, Yang-Xin Fu. (2015). CD160 is essential for NK-mediated IFN-γ production.
[17] Zheng Rong Sun, Yidi Li, Zining Zhang, Yajing Fu, Xiaoxu Han, Qinghai Hu, Haibo Ding, Hong Shang, Yongjun Jiang. (2022). CD160 Promotes NK Cell Functions by Upregulating Glucose Metabolism and Negatively Correlates With HIV Disease Progression.
[18] Haoyu Sun, Jing Xu, Qiang Huang, Mei Huang, Kun Li, Kun Qu, Hao Wen, Renyong Lin, Meijuan Zheng, Haiming Wei, Weihua Xiao, Rui Sun, Zhigang Tian, Cheng Sun. (2018). Reduced CD160 Expression Contributes to Impaired NK-cell Function and Poor Clinical Outcomes in Patients with HCC.
[19] Daniel Abate-Daga, Ken-ichi Hanada, Jeremy L Davis, James C Yang, Steven A Rosenberg, Richard A Morgan. (2013). Expression profiling of TCR-engineered T cells demonstrates overexpression of multiple inhibitory receptors in persisting lymphocytes.
[20] Najmeh Bozorgmehr, Isobel Okoye, Olaide Oyegbami, Lai Xu, Amélie Fontaine, Nanette Cox-Kennett, Loree Larratt, Mark Hnatiuk, Andrei Fagarasanu, Joseph Brandwein, Anthea Peters, Shokrollah Elahi. (2021). Expanded antigen-experienced CD160+CD8+effector T cells exhibit impaired effector functions in chronic lymphocytic leukemia.
[21] Tae-Jin Kim, Gayoung Park, Jeongmin Kim, Seon Ah Lim, Jiyoung Kim, Kyungtaek Im, Min Hwa Shin, Yang-Xin Fu, Maria-Luisa Del Rio, Jose-Ignacio Rodriguez-Barbosa, Cassian Yee, Kyung-Suk Suh, Seong-Jin Kim, Sang-Jun Ha, Kyung-Mi Lee. (2019). CD160 serves as a negative regulator of NKT cells in acute hepatic injury.
[22] Jiaoyan Huang, Xin Zhang, Hongkai Xu, Liuhui Fu, Yuke Liu, Jie Zhao, Jida Huang, Zuodong Song, Mingzhao Zhu, Yang--Xin Fu, Ye‐Guang Chen, Xiaohuan Guo. (2024). Intraepithelial lymphocytes promote intestinal regeneration through CD160/HVEM signaling.
[23] Jianxia Li, Huabin Hu, Ge Qin, Fan Bai, Xianrui Wu, Haoxian Ke, Jianwei Zhang, Yuqian Xie, Zehua Wu, Yang Fu, Hongbo Zheng, Longlong Gong, Zhi Xie, Yanhong Deng. (2024). Biomarkers of Pathologic Complete Response to Neoadjuvant Immunotherapy in Mismatch Repair-Deficient Colorectal Cancer.
[24] Jiatao Liao, Hongyan Lai, Chang Liu, Xin Zhang, Qiuxiang Ou, Qiaojuan Li, Yan Li, Zhen Wang, Cuicui Liu, Xianghua Wu, Huijie Wang, Hui Yu, Si Sun, Xinmin Zhao, Zhihuang Hu, Yao Zhang, Ying Lin, Bo Yu, Shenglin Huang, Jialei Wang. (2023). Plasma extracellular vesicle transcriptomics identifies CD160 for predicting immunochemotherapy efficacy in lung cancer.
[25] Claire Scheffges, Jérôme Devy, Jérôme Giustiniani, Stessy Francois, Lucille Cartier, Yacine Merrouche, Arnaud Foussat, Stéphane Potteaux, Armand Bensussan, Anne Marie-Cardine. (2024). Identification of CD160-TM as a tumor target on triple negative breast cancers: possible therapeutic applications.
[26] Guozhong Jiang, Zhizhong Wang, Zhenguo Cheng, Weiwei Wang, Shuangshuang Lu, Zifang Zhang, Chinedu A. Anene, Faraz Khan, Yue Chen, Emma Bailey, Huisha Xu, Yunshu Dong, Peinan Chen, Zhongxian Zhang, Dongling Gao, Zhimin Wang, Jinxin Miao, Xia Xue, Pengju Wang, Lirong Zhang, Rathi Gangeswaran, Peng Liu, Louisa S. Chard, Junkuo Li, Yongjun Guo, Jianzeng Dong, Nicholas R. Lemoine, Wencai Li, Jun Wang, Yaohe Wang. (2024). The integrated molecular and histological analysis defines subtypes of esophageal squamous cell carcinoma.
[27] Anders Mälarstig, Felix Graßmann, Leo Dahl, Marios Dimitriou, Dianna McLeod, Marike Gabrielson, Karl Smith‐Byrne, Cecilia Engel Thomas, Tzu-Hsuan Huang, Simon K. G. Forsberg, Per Eriksson, Mikael Ulfstedt, Mattias Johansson, Helgi B. Schiöth, Per Hall, Jochen M. Schwenk, Kamila Czene, Åsa K. Hedman. (2023). Evaluation of circulating plasma proteins in breast cancer using Mendelian randomisation.
[28] Ivo Veletic, David M Harris, Uri Rozovski, Maria Teresa S Bertilaccio, George A Calin, Koichi Takahashi, Ping Li, Zhiming Liu, Taghi Manshouri, Rares-Constantin Drula, Ken Furudate, Muharrem Muftuoglu, Anwar Hossain, William G Wierda, Michael J Keating, Zeev Estrov. (2025). CLL cell-derived exosomes alter the immune and hematopoietic systems.
[29] Felix S. Lichtenegger, Frauke M. Schnorfeil, Katharina Emmerig, Julia Neitz, Barbara Beck, Rika Draenert, Wolfgang Hiddemann, Marion Subklewe. (2013). Pseudo-Exhaustion Of CD8+ T Cells in AML.
[30] Yoav Peretz, Zhong He, Yu Shi, Bader Yassine‐Diab, Jean-Philippe Goulet, Rebeka Bordi, Ali Filali‐Mouhim, Jean-Baptiste Loubert, Mohamed El‐Far, Franck P. Dupuy, Mohamed Rachid Boulassel, Cécile Tremblay, Jean‐Pierre Routy, Nicole F. Bernard, Robert Balderas, Elias K. Haddad, Rafick‐Pierre Sékaly. (2012). CD160 and PD-1 Co-Expression on HIV-Specific CD8 T Cells Defines a Subset with Advanced Dysfunction.
[31] Marcus Buggert, Johanna Tauriainen, Takuya Yamamoto, Juliet Frederiksen, Martin A. Ivarsson, Jakob Michaëlsson, Ole Lund, Bo Hejdeman, Marianne Jansson, Anders Sönnerborg, Richard A. Koup, Michael R. Betts, Annika C. Karlsson. (2014). T-bet and Eomes Are Differentially Linked to the Exhausted Phenotype of CD8+ T Cells in HIV Infection.
[32] Selena Viganò, Felicitas Bellutti Enders, Isabelle Miconnet, Cristina Cellerai, Anne-Laure Savoye, Virginie Rozot, Matthieu Perreau, Mohamed Faouzi, Khalid Ohmiti, Matthias Cavassini, Pierre-Alexandre Bart, Giuseppe Pantaleo, Alexandre Harari. (2013). Rapid perturbation in viremia levels drives increases in functional avidity of HIV-specific CD8 T cells.
[33] Damien Guinault, Marie-Laure Nicolau-Travers, Stein Silva, Olivier Cointault, Barnabé Daniau, Arnaud Del Bello, Michaël Pérès, David Rousset, Julie Rieunier, Laurence Lavayssière, Marie‐Béatrice Nogier, Edith Hourcastagnou, Arnaud Mari, Nassim Kamar, François Vergez, Stanislas Faguer. (2021). Expression of Exhaustion Markers on CD8+ T-Cell Patterns Predict Outcomes in Septic Patients Admitted to the ICU.
[34] Hugo Barragué, Jessica Fontaine, Florence Abravanel, Emilie Mauré, Jean‐Marie Péron, Laurent Alric, Martine Dubois, Jacques Izopet, Éric Champagne. (2021). Mobilization of γδ T Cells and IL-10 Production at the Acute Phase of Hepatitis E Virus Infection in Cytomegalovirus Carriers.
[35] Franziska Muscate, Nadine Stetter, Christoph Schramm, Julian Schulze zur Wiesch, Lidia Bosurgi, Thomas Jacobs. (2018). HVEM and CD160: Regulators of Immunopathology During Malaria Blood-Stage.
[36] Annabelle Small, Suzanne Cole, Jing Jing Wang, Sunil Nagpal, Ling‐Yang Hao, Mihir D. Wechalekar. (2022). Attenuation of the BTLA/HVEM Regulatory Network in the Circulation in Primary Sjögren's Syndrome.
[37] Chin-Man Wang, Yeong-Jian Jan Wu, Jian-Wen Zheng, Li Yu Huang, Keng Poo Tan, Ji-Yih Chen. (2024). T cell expressions of aberrant gene signatures and Co-inhibitory receptors (Co-IRs) as predictors of renal damage and lupus disease activity.
[38] Marjolein Wentink, Yvonne M. Mueller, Virgil A. S. H. Dalm, Gertjan J. Driessen, P. Martin van Hagen, Joris M. van Montfrans, Mirjam van der Burg, Peter D. Katsikis. (2018). Exhaustion of the CD8+ T Cell Compartment in Patients with Mutations in Phosphoinositide 3-Kinase Delta.
[39] Kohei Hosokawa, Pawel Muranski, Xingmin Feng, Danielle M. Townsley, Baoying Liu, Jared E. Knickelbein, Keyvan Keyvanfar, Bogdan Dumitriu, Sawa Ito, Sachiko Kajigaya, James G. Taylor, Mariana J. Kaplan, Robert B. Nussenblatt, A. John Barrett, John J. O'Shea, Neal S. Young. (2016). Memory Stem T Cells in Autoimmune Disease: High Frequency of Circulating CD8+ Memory Stem Cells in Acquired Aplastic Anemia.
[40] Weiwei He, Jing Zhao, Xuerong Liu, Sheli Li, Kaida Mu, Jing Zhang, Jin‐an Zhang. (2020). Associations Between CD160 Polymorphisms and Autoimmune Thyroid Disease: A Case-Control Study.
[41] Mathias Pawlak, David DeTomaso, Alexandra Schnell, Gerd Meyer Zu Horste, Youjin Lee, Jackson Nyman, Danielle Dionne, Brianna M L Regan, Vasundhara Singh, Toni Delorey, Markus A Schramm, Chao Wang, Antonia Wallrapp, Patrick R Burkett, Samantha J Riesenfeld, Ana C Anderson, Aviv Regev, Ramnik J Xavier, Nir Yosef, Vijay K Kuchroo. (2022). Induction of a colitogenic phenotype in Th1-like cells depends on interleukin-23 receptor signaling.
[42] Cuihua Jiang, Jianqi Liang, Kaibo Hu, Yanqing Ye, Jiajia Yang, Xiaozhi Zhang, Guilin Ye, Jing Zhang, Deju Zhang, Bin Zhong, Peng Yu, Liefeng Wang, Bin Zeng. (2025). Identification of tryptophan metabolism-related biomarkers for nonalcoholic fatty liver disease through network analysis.



