武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
【第78期】前沿靶点速递:每周医学研究精选
205 人阅读发布时间:2026-03-20 11:48
靶点:OSMR、SST、SCN11A
应用:神经性疼痛的潜在治疗靶点
来源:Molecular architecture of human dermal sleeping nociceptors.Cell,2026 Feb 04
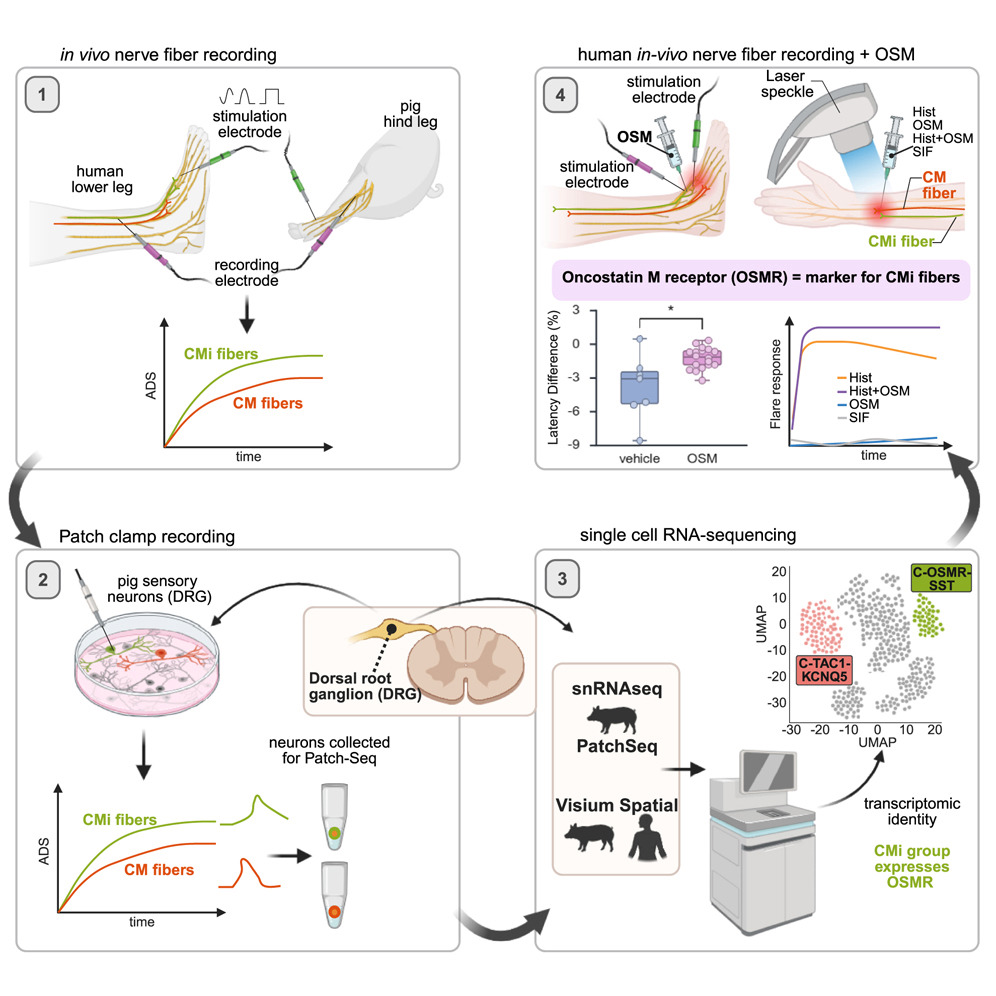
图源:10.1016/j.cell.2025.12.048[1]
德国亚琛工业大学和多伦多大学团队在Cell发表一篇研究,利用Patch-seq技术结合猪与人类跨物种分析,首次鉴定出人类皮肤"休眠痛觉感受器"(CMis)的特异性分子标记物OSMR和SST。研究团队通过构建猪背根神经节神经元分子分类图谱,发现C-OSMR-SST亚群高表达SCN11A(Nav1.9)并表现出典型CMis功能特征;计算模型证实Nav1.9超慢失活动力学是导致活动依赖性传导速度减慢的核心机制。人体实验显示,OSMR配体OSM能特异性调节CMis纤维传导动力学而不影响普通机械敏感纤维,且不会直接引发痛觉,为神经性疼痛精准疗法开发提供了全新靶点。
靶点:RAP1A
应用:肝纤维化的潜在治疗靶点
来源:Endothelial RAP1A attenuates sinusoidal capillarisation and liver fibrosis by inhibiting RAF1-mediated Notch activation.Gut,2026 Feb 11
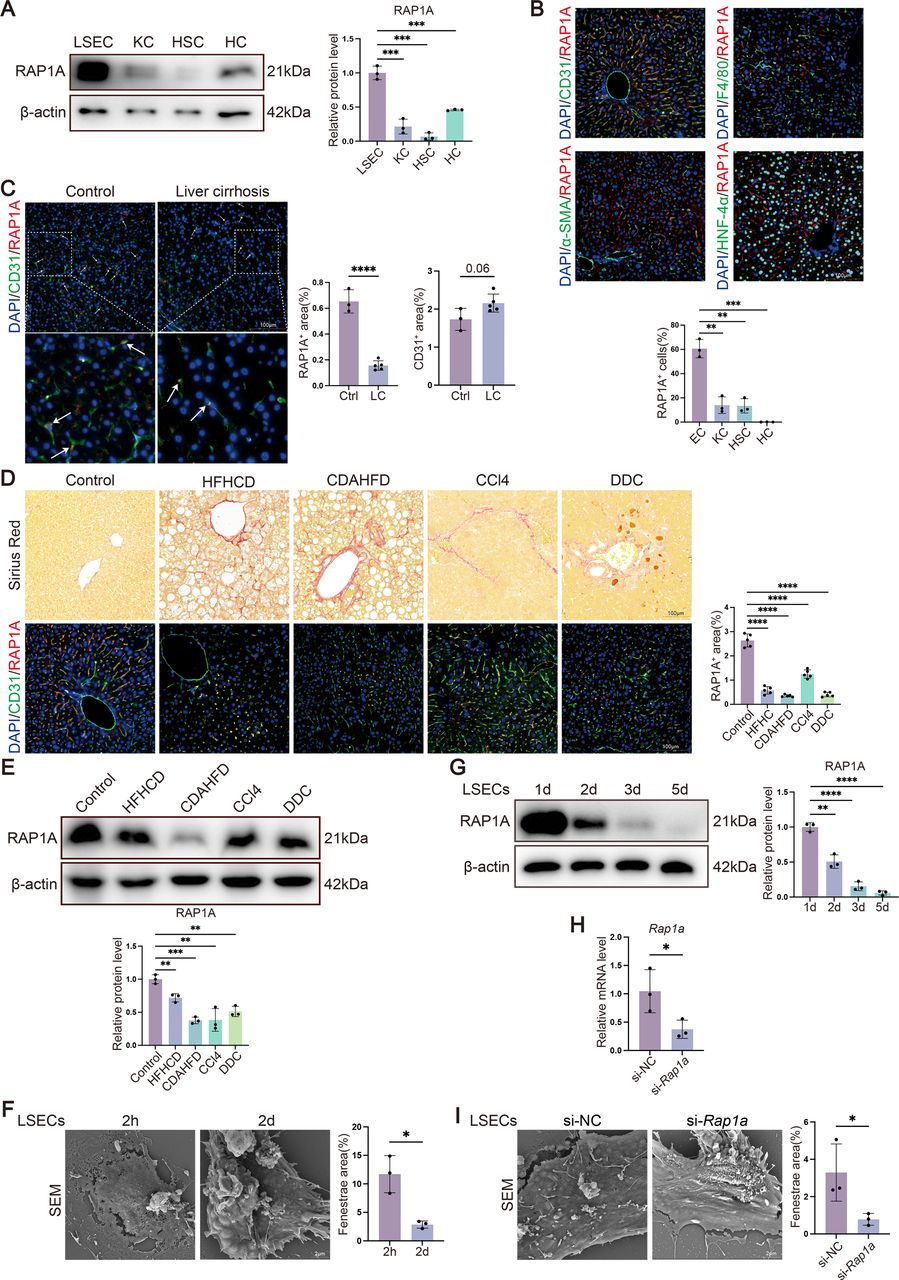
图源:10.1136/gutjnl-2025-337143[2]
上海交通大学蔡晓波/陆伦根团队在Gut发表了一篇研究,揭示了RAP1A调控肝窦毛细血管化与肝纤维化的新机制。研究发现,肝窦内皮细胞(LSEC)中RAP1A表达下调是肝纤维化早期关键事件,内皮特异性敲除Rap1a可导致LSEC自发性毛细血管化及肝纤维化。机制上,RAP1A通过稳定RAF1蛋白抑制Notch信号过度激活;RAP1A缺失促进RAF1降解,导致Notch信号异常激活,驱动LSEC去分化。更重要的是,使用RAP1激活剂可显著缓解小鼠肝纤维化,恢复LSEC窗孔结构,减轻纤维沉积。该研究将RAP1A定位为Notch异常激活的"上游闸门",为肝纤维化提供了早期干预的新靶点。
靶点:LOXL2
应用:转移瘤免疫治疗耐药的潜在治疗靶点
来源:CLIM-TIME identifies metastatic microenvironment modulators for T cell therapy response.Cell,2026 Mar 05
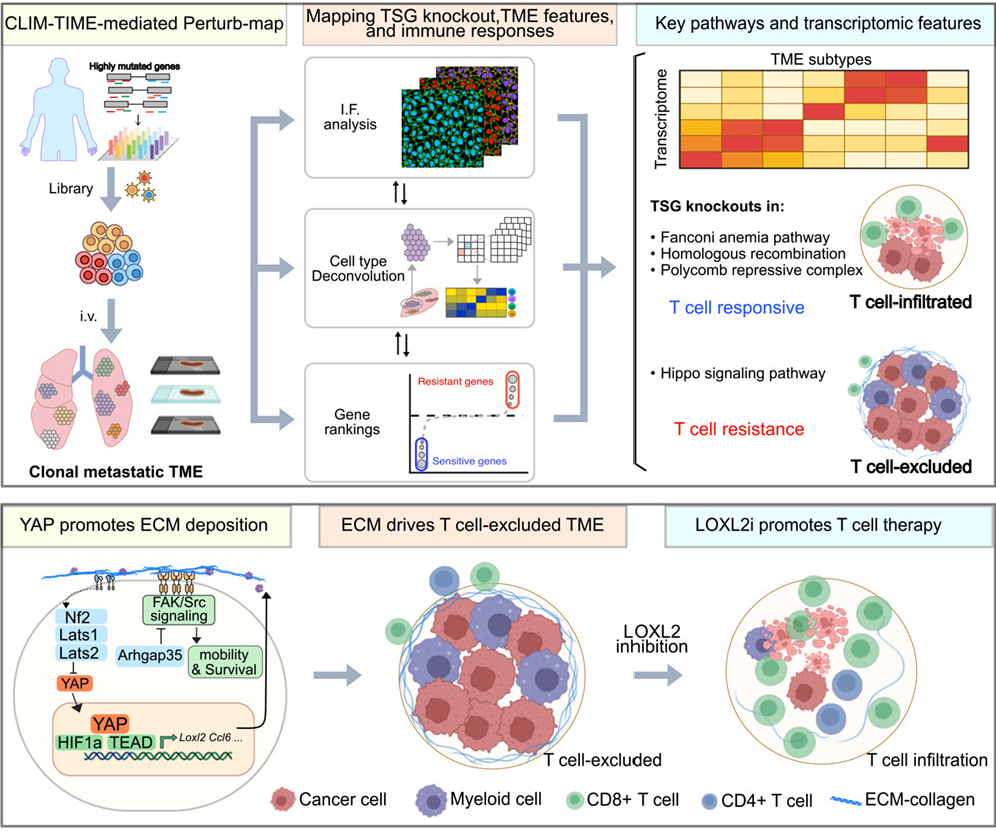
图源:10.1016/j.cell.2025.12.042[3]
一篇发表于Cell的研究建立了新型微环境空间筛选平台CLIM-TIME,系统解析肿瘤遗传改变与转移灶微环境及免疫治疗应答的因果关系。研究对391种抑癌基因缺失的肺转移灶分析发现,T细胞治疗耐受的转移瘤主要呈"髓系富集且T细胞排斥型"特征。机制上,Nf2等基因缺失可上调胶原交联酶LOXL2表达,重塑微环境并诱导髓系细胞呈M2样免疫抑制特征,共同促进T细胞排斥。靶向抑制LOXL2可减少胶原沉积、促进T细胞浸润,显著提升TCR-T和CAR-T治疗效果,为克服转移瘤免疫治疗耐药提供了关键靶点。
靶点:GPX1
应用:通过诱导铁死亡治疗癌症的潜在治疗靶点
来源:A GPX1–OSBPL8 Axis Mediates Noncanonical In Vivo Ferroptosis and Cancer Growth Suppression.Cell,2026 Feb 19
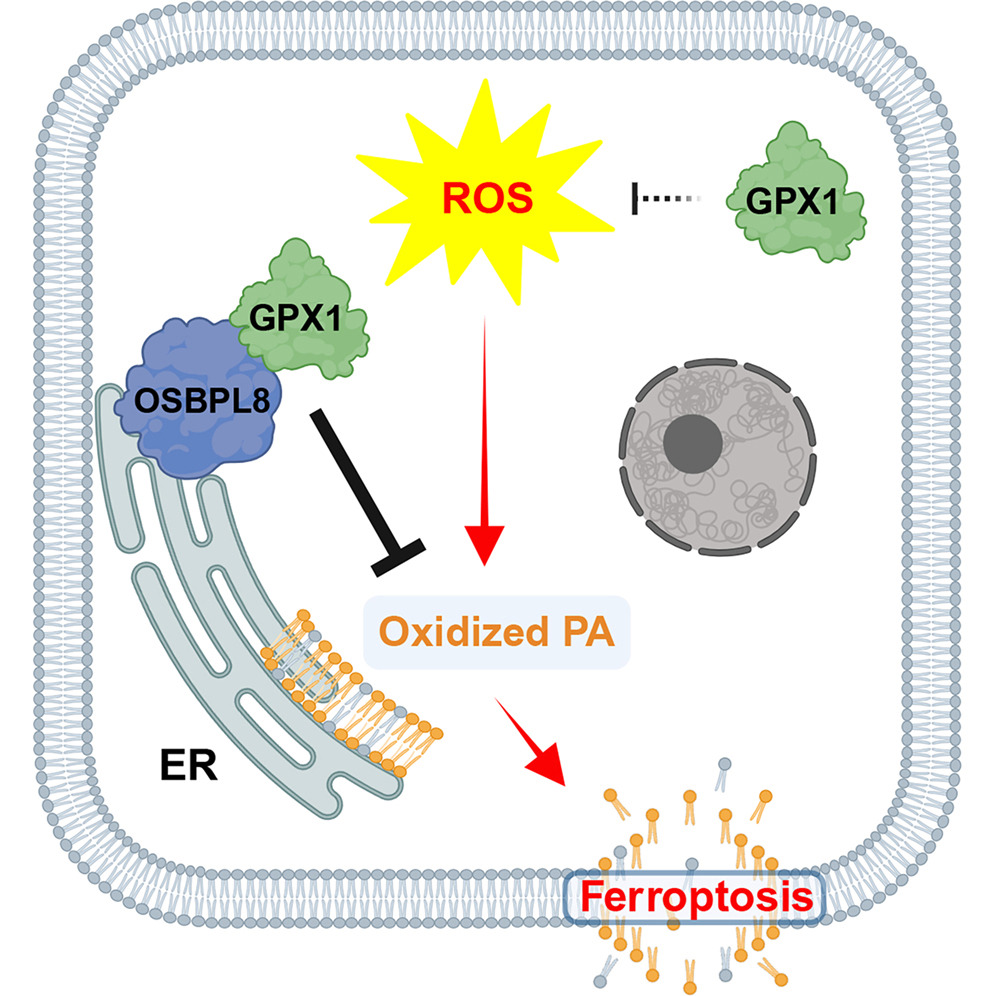
图源:10.1016/j.cell.2026.01.009[4]
近期在Cell发表的一篇研究揭示了GPX1-OSBPL8轴在肿瘤细胞自发性铁死亡中的关键调控作用。研究团队通过全基因组筛选发现,GPX1是抑制ROS诱导的非经典铁死亡的特异性因子,其缺失可显著抑制多种肿瘤生长。机制上,内质网蛋白OSBPL8作为"适配器",将GPX1招募至内质网并递送特异性底物过氧化磷脂酸(PA),从而清除脂质过氧化物、阻断铁死亡。该通路对正常细胞非必需,但肿瘤细胞因高ROS环境对其产生依赖性,使GPX1成为诱导铁死亡治疗癌症的潜在靶点。
靶点:PHGDH
应用:阿尔茨海默病的潜在治疗靶点
来源:RNA-binding activity of PHGDH drives amyloid-betaproduction in a human brain organoid model of sporadic Alzheimer's disease.Proc Natl Acad Sci U S A,2026 Feb 24
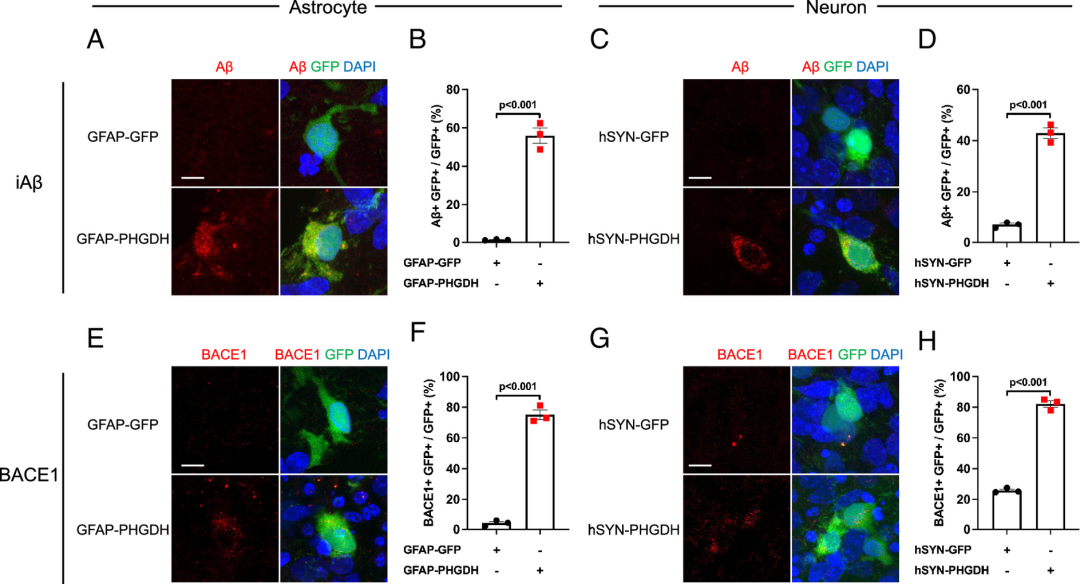
图源:10.1073/pnas.2532234123[5]
近期在PNAS发表的一篇研究揭示了阿尔茨海默病(AD)早期毒性蛋白产生的关键机制。加州大学圣地亚哥分校钟声教授团队发现,磷酸甘油酸脱氢酶(PHGDH)通过特异性结合EIF2AK1激酶的mRNA,促进EIF2α磷酸化,进而驱动BACE1合成和Aβ生成,形成"PHGDH-EIF2AK1-EIF2α-BACE1-Aβ"病理通路。利用人脑类器官和小鼠模型证实,PHGDH过表达可诱导神经元和星形胶质细胞内Aβ积累,且该效应依赖于其RNA结合能力而非酶活性。该发现为散发性AD的早期诊断提供了潜在生物标志物,并提示靶向PHGDH的RNA结合功能可能成为从源头阻断Aβ生成的新治疗策略。
靶点:GPNMB
应用:代谢功能障碍相关脂肪性肝炎的潜在治疗靶点
来源:RYK is a GPNMB receptor that drives MASH.Nature,2026 Feb 18

图源:10.1038/s41586-026-10160-z[6]
近期在Nature发表的一篇研究揭示了GPNMB-RYK新型配体-受体信号通路在代谢功能障碍相关脂肪性肝炎(MASH)中的关键作用。武汉大学宋保亮团队发现,肝细胞脂代谢调控分子GPNMB经蛋白酶切割生成分泌型胞外域(G-ECD),并首次鉴定单次跨膜蛋白RYK为其受体,该通路通过增强肝脏脂质摄取和合成驱动MASH发生发展。研究证实,靶向该信号轴的疫苗、中和抗体、AAV-shRNA及GalNAC-siRNA等多种策略均可有效预防或治疗MASH,为开发同时改善脂肪变性、炎症和纤维化的创新疗法提供了具有转化价值的全新靶点。
靶点:TMEM175
应用:肿瘤免疫治疗
来源:Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway.Nat Commun,2026 Feb 14

图源:10.1038/s41467-026-69546-2[7]
近期在Nature Communications发表的一篇研究揭示了溶酶体TMEM175蛋白作为肿瘤免疫治疗新靶点的潜力。四川大学华西医院魏霞蔚团队发现,TMEM175在肿瘤相关巨噬细胞(TAMs)中高表达,其条件性敲除可显著抑制黑色素瘤和肺癌生长,并增强M1样巨噬细胞极化及CD4+/CD8+T细胞、NK细胞的募集活化。机制上,TMEM175缺失导致溶酶体pH不稳定,促进钙离子释放和NLRP3炎性小体激活,释放IL-1β和IL-18,同时增强抗原交叉呈递;且敲除TMEM175能提升PD-1抗体治疗效果。该研究为开发靶向巨噬细胞TMEM175的肿瘤免疫治疗新策略提供了理论依据。
靶点:SEC61A1
应用:衰老相关认知衰退的潜在治疗靶点
来源:Mitochondrial double-stranded RNA drives aging-associated cognitive decline.Cell Res,2026 Feb 16

图源:10.1038/s41422-026-01224-w[8]
近期在Cell Research发表的一篇研究揭示了SEC61A1-mt-dsRNA-天然免疫轴驱动衰老相关认知衰退的新机制。厦门大学王耿团队发现,内质网蛋白SEC61A1在衰老大脑中特异性上调,通过与线粒体蛋白RMDN3互作增强内质网-线粒体接触,促进线粒体转录和mt-dsRNA累积,激活MDA5/RIG-I-MAVS天然免疫通路,诱发神经炎症和认知损伤。研究证实,神经元特异性过表达SEC61A1可模拟衰老及阿尔茨海默病病理表型,而靶向敲低SEC61A1或其下游MAVS可显著改善衰老小鼠认知功能。该机制在秀丽隐杆线虫中保守,为神经退行性疾病的防治提供了全新靶点。
靶点:SLAMF6
应用:癌症免疫治疗
来源:SLAMF6 as a drug-targetable suppressor of T cell immunity against cancer.Nature,2026 Feb 11

图源:10.1038/s41586-026-10106-5[9]
近期在Nature发表的一篇研究揭示了SLAMF6通过顺式互作抑制T细胞免疫的新机制。研究团队发现,T细胞表面的SLAMF6受体通过10纳米尺度的顺式二聚化形成"自我枷锁",持续招募磷酸酶SHP-1抑制TCR信号传导。基于该机制,研究人员筛选出能高效阻断顺式互作的人源化抗体mAb 21/23,在多种肿瘤模型中显著增强T细胞功能、逆转耗竭状态,并与PD-1抗体产生协同抗肿瘤效应。该研究颠覆了免疫检查点依赖细胞间反式互作的传统认知,为开发不依赖肿瘤PD-L1表达的新型免疫治疗策略提供了重要靶点。
靶点:ARID1A
应用:结直肠癌联合免疫治疗
来源:ARID1A Mediates SWI/SNF-Independent Maintenance of Heterochromatin Architecture to Restrain Viral Mimicry and Immunogenicity in Colon Cancer.Cancer Res,2026 Feb 09

图源:10.1158/0008-5472.CAN-25-3231[10]
近期在Cancer Research发表的一篇研究揭示了ARID1A通过非经典途径维持异染色质并调控肿瘤免疫微环境的新机制。上海交通大学沈键锋团队联合多家单位发现,ARID1A可不依赖SWI/SNF复合体,通过与TRIM28互作维持异染色质结构稳定;其缺失导致SETDB1解离和H3K9me3减少,解除对内源性逆转录元件的抑制,触发病毒拟态反应和I型干扰素应答,增强肿瘤免疫原性。研究还证实,阻断ARID1A-TRIM28互作的合成短肽可将"冷"肿瘤转为"热"肿瘤,且ARID1A缺失能增强PD-1抗体疗效,为结直肠癌联合免疫治疗提供了新策略。
推荐产品
|
靶点 |
重组蛋白 |
货号 |
|
ARID1A |
Recombinant Human AT-rich interactive domain-containing protein 1A (ARID1A), partial |
CSB-EP002058HU1 |
|
GPNMB |
Recombinant human Transmembrane glycoprotein NMB |
CSB-MP0620444h |
|
GPX1 |
Recombinant Human Glutathione peroxidase 1 (GPX1) (U49S) |
CSB-EP009866HU |
|
LOXL2 |
Recombinant Mouse Lysyl oxidase homolog 2 (Loxl2) |
CSB-EP013041MO |
|
OSMR |
Recombinant Human Oncostatin-M-specific receptor subunit beta (OSMR), partial |
CSB-EP857869HU |
|
PHGDH |
Recombinant Human D-3-phosphoglycerate dehydrogenase (PHGDH), partial |
CSB-EP017920HU1 |
|
RAP1A |
Recombinant Human Ras-related protein Rap-1A (RAP1A) |
CSB-MP019321HU |
|
SCN11A |
Recombinant Human Sodium channel protein type 11 subunit alpha (SCN11A), partial |
CSB-MP883417HU |
|
SEC61A1 |
Recombinant Human Protein transport protein Sec61 subunit alpha isoform 1 (SEC61A1) |
CSB-CF020956HU(A4) |
|
SLAMF6 |
Recombinant Human SLAM family member 6 (SLAMF6), partial |
CSB-EP021368HU |
|
SST |
Recombinant Human Somatostatin (SST), partial |
CSB-EP022723HU |
|
TMEM175 |
Recombinant Human Transmembrane protein 175 (TMEM175), partial |
CSB-MP023756HU |
参考文献:
[1]Molecular architecture of human dermal sleeping nociceptors.Cell,2026 Feb 04
[2]Endothelial RAP1A attenuates sinusoidal capillarisation and liver fibrosis by inhibiting RAF1-mediated Notch activation.Gut,2026 Feb 11
[3]CLIM-TIME identifies metastatic microenvironment modulators for T cell therapy response.Cell,2026 Mar 05
[4]A GPX1-OSBPL8 Axis Mediates Noncanonical In Vivo Ferroptosis and Cancer Growth Suppression.Cell,2026 Feb 19
[5]RNA-binding activity of PHGDH drives amyloid-betaproduction in a human brain organoid model of sporadic Alzheimer's disease.Proc Natl Acad Sci U S A,2026 Feb 24
[6]RYK is a GPNMB receptor that drives MASH.Nature,2026 Feb 18
[7]Deficiency of lysosomal TMEM175 in myeloid macrophages exerts anti-tumor immunity via inflammasome and cross-presentation pathway.Nat Commun,2026 Feb 14
[8]Mitochondrial double-stranded RNA drives aging-associated cognitive decline.Cell Res,2026 Feb 16
[9]SLAMF6 as a drug-targetable suppressor of T cell immunity against cancer.Nature,2026 Feb 11
[10]ARID1A Mediates SWI/SNF-Independent Maintenance of Heterochromatin Architecture to Restrain Viral Mimicry and Immunogenicity in Colon Cancer.Cancer Res,2026 Feb 09
*免责声明:华美生物内容团队仅是分享和解读公开研究论文及其发现,本文仅作信息交流,文中观点不代表华美生物立场,请理解。



