武汉华美生物工程有限公司CUSABIO®品牌商
15 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
肿瘤免疫治疗新兴靶点 ROR1,究竟有多大潜力?
7924 人阅读发布时间:2021-01-06 08:54
10 月 29 日,基石药业宣布与 LegoChem Biosciences 公司达成一项授权协议,获得在韩国以外地区开发和商业化 LCB71 的独。家授权。LCB71 是一款靶向 ROR1 的抗体偶联药物(ADC),合作金额总计可超过 3.6 亿美元。无独有偶,一周后,11 月 5 日,默沙东(MSD)公司和 VelosBio 公司联合宣布,双方已达成协议,默沙东将斥资 27.5 亿美元收购 VelosBio 公司。VelosBio 公司是一家致力于开发靶向受体酪氨酸激酶样孤儿受体 1(ROR1)的 “first-in-class” 抗癌疗法的生物医药公司。其主打在研产品 VLS-101 是一款靶向 ROR1 的抗体偶联药物(ADC),目前正分别在一项 1 期临床试验和一项 2 期临床试验中用于治疗血液癌症和实体瘤。那 ROR1 究竟是什么?该靶点为何会如此受默沙东和基石药业的青睐?让我们带着这两个问题阅读完这篇文章,这篇文章包含以下几个部分:
1、ROR1 是什么?
2、ROR1 的结构与功能
3、Wnt5a/ROR1 与肿瘤
4、靶向 ROR1 的临床意义
1、什么是 ROR1?
ROR1 是受体酪氨酸激酶样孤儿受体(ROR)家族成员之一,属于 I 型受体酪氨酸激酶 (receptor tyrosine kinase, RTK) 家族。与核受体中的 ROR 家族不同,ROR 是一类膜受体。它们与家族中的原肌球蛋白激酶受体家族 (tropomyosin-related kinase, Trk)、骨骼肌特异性酪氧酸激酶样受体家族 (muscle specific knase, MuSK) 和神经营养因子酯氨酸激酶受体家族 (neurotrophic tyrosine kinase receptor, NT-RTK) 关系密切,由于 ROR 蛋白最初发现时配体未知,所以被定义为孤儿受体 [1]。
ROR 家族的另一个成员是 ROR2,ROR1 与 ROR2 氨基酸序列的同源性达 58%。其中 ROR1 又含有 2 种亚型:完整的细胞膜受体型 ROR1 以及截短型变异体。截断型变异体主要分为无胞外结构的膜结合型 ROR1I 与只含胞外结构的可溶型 ROR1 [2]。可溶型 ROR1 的表达在正常人与肿瘤患者中并无差异,血清中的表达量很低或者检测不到,且与疾病的进展和严重程度无关,而完整结构的膜结合型 ROR1 在多种肿瘤组织特异性高水平表达 [3]。后文中所提到的 ROR1 都是指完整结构的膜结合型 ROR1。
2、ROR1的结构与功能
ROR1 是一种跨膜受体酪氨酸激酶蛋白。ROR1 编码基因共 2814bp,位于染色体 1p31.3。ROR1 膜蛋白由 937 个氨基酸组成,分子量约 105 kDa。ROR1 结构在生物种间高度保守,如人与鼠的 ROR1 氨基酸序列同源性可达 97%。如图 1 所示,人源 ROR1 由一个胞外的免疫球蛋白样结构域 (Ig)、两个富含半胱氨酸的结构域 (FZD)、近膜 kringle 结构域、单次跨膜结构以及一个胞内酪氨酸激酶结构域(TKD)、两个丝 / 苏氨酸富集结构域 (S/TRD) 和一个脯氨酸富集结构域(PRD)组成 [4]。
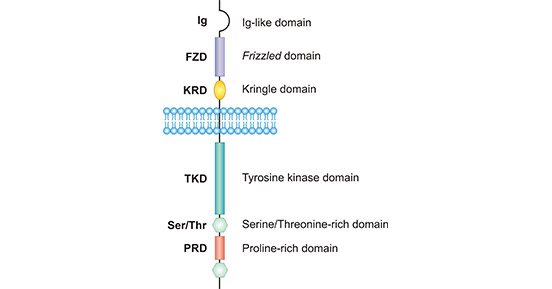
图1. The structure of ROR1
*图片参考文献发表在Protein Cell上[4]。
免疫球蛋白样结构域和半胱氨酸富集结构域与 ROR1 结合配体的功能相关。其中 FZD 结构域由 10 个保守的半胱氨酸残基和 5 个相应的二硫键组成。FZD 结构还见于平滑肌家族受体(如 Smo)、卷曲家族受体(如 sFRP)、金属羧肽酶 Z(CPZ)、collagen α1 XVIII 和低密度脂蛋白受体相关蛋白 (LRP)。这些蛋白大都可以结合 Wnt 蛋白并参与 Wnt 通路的信号转导。目前大量研究己经证实 ROR1 也是通过 FZD 结合 Wnt5a 并激活非经典 Wnt 信号通路 [5] [6]。 Kringle 结构域在 ROR 家族中比较保守,由 80 个氨基酸组成 [7]。其结构特点是含有三个由二硫键形成的环状结构,这三个环状结构也参与了 ROR 受体识别 Wnt 蛋白的过程。
ROR 的酪氨酸激酶结构域在生物体高度保守,和 Trk、MuSK 的酪氨酸激酶结构域极其相似。但 ROR1 蛋白在这段高度保守的区域内存在某些氨基酸序列的改变,提示其胞内激酶活性有可能发生改变。丝 / 苏氨酸、脯氨酸富集结构域是由丝 / 苏氨酸富集结构域、脯氨酸富集结构域、丝 / 苏氨酸富集结构域三个结构域串联而成。该区域存在潜在的磷酸化位点、与下游信号传导有关。
3、Wnt5a/ROR1与肿瘤
目前关于 ROR1 信号传导的主流说法是,ROR1 可通过介导非经典 Wnt 信号通路(non-canonical Wnt pathways)的信号传递,在多种生理过程中发挥重要作用,其中包括调节细胞分裂、增殖、迁移、和细胞趋化,尤其是 Wnt5a。Wnt5a 是典型的非经典 Wnt 信号通路的激活因子,参与 NF-κB 亚基 p65 的磷酸化,激活肿瘤细胞中 NF-κB 通路,促进细胞迁移和侵袭,EMT、癌转移等。接下来,我们具体了解下 ROR1 是如何通过 Wnt5a 信号通路激活肿瘤细胞的。
Wnt5a/ROR1 在多种癌症中的高度表达。作为 Wnt5a 的受体,ROR1 参与激活肿瘤细胞 NF-κB 通路。NF-κB 通路是炎症反应和免疫调控的掌舵者,在多种肿瘤类型中组成性激活。如图 2 所示,Wnt5a 激活受体 ROR1 或 FZD5,导致 Dvl2/3 激活和 Akt 磷酸化。Akt 继而促进 IKKα 磷酸化激活 IKK 复合体,IKK 复合体负责 IκBα 降解和 NF-κB 亚基 p65 的磷酸化。磷酸化的 p65 转移到细胞核促进包括 Wnt5a 在内的靶基因转录表达。Wnt5a 的分泌又促进新一轮的自主反馈循环。自主反馈循环 ROR1/Akt/p65 通路的激活会进一步促进促炎因子(如 IL-6)和趋化因子(如 CCL2)的分泌。
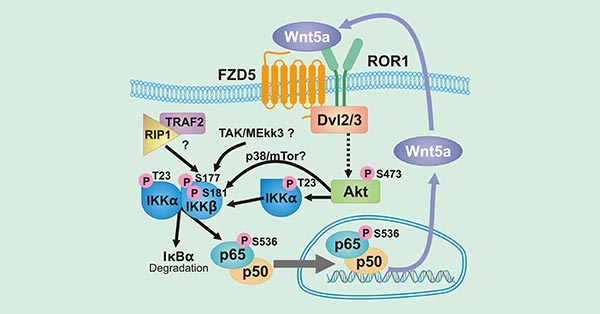
此外,有多项研究已将 ROR1 的表达与 YAP / TAZ 转录的激活相关联,从而增强肿瘤发生和化学耐药性 [8] [9]。如图 3 所示,Wnt5a 与 ROR1 / FZD 复合物的结合,然后通过结合 Gα12/13 进一步激活 RhoA,从而抑制 Lats1/2 活性,进而导致 YAP / TAZ 去磷酸化和核易位。易位到细胞核里的 YAP/TAZ 与 TEAD 结合后可以诱导涉及细胞增殖、干细胞自我更新和肿瘤发生基因的转录。增加的 YAP/TAZ 转录反过来又可以上调 ROR1 表达。
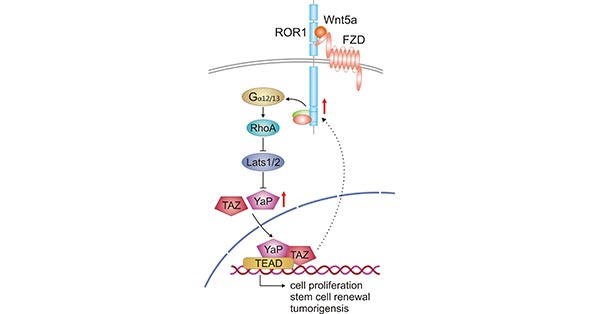
图3. Crosstalk between Wnt5a-ROR1 signaling and YAP/TAZ pathway
*图片参考文献发表在Cells上[10]。
4、靶向 ROR1 的临床意义
ROR1 被认为是个非常有潜力的靶点,因为它作为酪氨酸激酶受体,具有可药性;其次,它在细胞表面表达;更重要的是,它在肿瘤细胞中高度表达,而在成人健康组织中表达量很低。目前有多家公司在开发靶向 ROR1 的抗癌疗法,其中包括单克隆抗体、抗体偶联药物(ADC)、双特异性抗体、以及 CAR-T 疗法等多种治疗模式(见下表)。免疫检查点疗法(ICT)已经改变了许多肿瘤的治疗模式,然而有些肿瘤类型对 ICT 的响应率低,这大部分要归因于 TME 中高度的免疫抑制和肿瘤缺少 T 细胞浸润。在这种情况下,采用 ICT 联合靶向 ROR1/Wnt5a 的疗法有可能能解决响应率低的问题。
| 药物名称 | 药物类型 | 研发公司 | 适应症 | 研发状态 | 最后更新日期 |
|---|---|---|---|---|---|
| ROR1 CAR-T | 嵌合抗原受体T细胞疗法(CAR-T),基因疗法 | Oncternal Therapeutics | 血液癌症和实体瘤 | 临床前 | 2020-09-30 |
| HG-030 | 化学药 | 成都先导药物开发股份有限公司 | 肿瘤 | 临床一期 | 2020-09-27 |
| NBE-002 | 抗体偶联药物(ADC) | Nbe-Therapeutics Ag | 三阴性乳腺肿瘤 | 临床二期 | 2020-08-28 |
| Cirmtuzumab | 人源化单克隆抗体 | Oncternal Therapeutics,加利福尼亚大学 | 慢性淋巴细胞白血病 | 临床二期 | 2020-08-28 |
| 套细胞淋巴瘤 | 临床二期 | ||||
| 乳腺癌 | 临床一期 | ||||
| ROR1R-CAR | 嵌合抗原受体T细胞疗法(CAR-T),基因疗法 | CLL的全球研究基金会联盟,The University Of Texas M.D. Anderson Cancer Center | 白血病 | 临床一期 | 2020-08-28 |
| APVO-425 | 双特异性抗体 | Emergent Biosolutions | 三阴性乳腺肿瘤 | 临床前 | 2020-08-28 |
| JCAR-024 | 嵌合抗原受体T细胞疗法(CAR-T),基因疗法 | 弗莱德哈钦森癌症研究中心 | / | 无进展 | 2020-08-28 |
| VLS-101 | 抗体偶联药物 | Velosbio | 血液癌症 | 临床一期 | / |
| 实体瘤 | 临床二期 | ||||
| LCB71 | 抗体偶联药物 | LegoChem Biosciences/基石药业 | / | 临川前 | / |
| KAN0439834 | 小分子抑制剂 | Kancera | / | 临川前 | / |
*表格数据来源于公开资料
参考文献:
[1] Forrester WC. The Ror receptor tyrosine Kinase family [J]. CMLS Cell Mol Life Sci. 2002, 59:83-06.
[2] Boreherding N, Kusner D, Liu GH, et al. ROR1, an embryonic protein with an emerging role in cancer biology [J]. Protein Cell. 2014, 5:496-502.
[3] Baskar S, K wong KY, .Hofer T, et al. Unique cell surface expression of receptor tyrosine kinase ROR1 in human B-cell chronic lymphocytic leukemia [J]. Clin Cancer Res. 2008, 14:396-404.
[4] Nicholas Borcherding, David Kusner, Guang-Hui Liu, et al. ROR1, an embryonic protein with an emerging role in cancer biology [J]. Protein Cell. 2014, 5(7):496–502.
[5] Mikels AJ, Nusse R. Purified Wnt5a protein activates or inhibits β-catenin–TCF signaling depending on receptor context [J]. PLoS Biol. 2006, 4:e115.
[6] Nomi M, Oishi I, Kani S, et al. Loss of mRor1 enhances the heart and skeletal abnormalities in mRor2-deficient mice: redundant and pleiotropic functions of mRor1 and mRor2 receptor tyrosine kinases [J]. Mol Cell Biol. 2001, 21:8329–8335.
[7] Wamg HY, Lie T, Malbon CC, et al. Structure-function analysis of Frizzleds [J]. Cell Signal. 2006, 18: 934-941.
[8] Zhang, S., Zhang, H., Ghia, E.M., et al. Inhibition of chemotherapy resistant breast cancer stem cells by a ROR1 specific antibody [J]. Proc. Natl. Acad. Sci. USA. 2019, 116, 1370–1377.
[9] Islam, S.S., Uddin, M., Noman, A.S.M., et al. Antibody-drug conjugate T-DM1 treatment for HER2+ breast cancer induces ROR1 and confers resistance through activation of Hippo transcriptional coactivator YAP1 [J]. EBioMedicine. 2019, 43, 211–224.
[10] Hanna Karvonen, Harlan Barker, Laura Kaleva, et al. Molecular Mechanisms Associated with ROR1-Mediated Drug Resistance: Crosstalk with Hippo-YAP/TAZ and BMI-1 Pathways [J]. Cells. 2019, 8, 812: 2-12.



